摘要:解析 在加热条件下.钠既能与硫化合生成.也能与空气中的氧气反应生成.而钠又是过量的.所以除生成外还有生成.答案 A.C例5 A.B.C.D.E五种物质都含有同一元素.它们按下图所示关系相互转化.已知A为单质.(1)写出A-E的化学式(2)分别写出有关反应的化学方程式.其中属于氧化还原反应的.请标出电子转移的方向和数目①A→B: ②A→C: ③A→D: ④C→D: ⑤C→E: ⑥D→E:
网址:http://m.1010jiajiao.com/timu_id_405484[举报]
溶液浓度常影响反应的发生,下列说法符合事实的是
A.常温下,铝片既可溶于足量浓H2SO4中,也可溶于足量稀H2SO4中
B.常温下,铜片与浓HNO3反应而不与稀HNO3反应
C.加热条件下,浓H2SO4有利于酯化反应进行而稀H2SO4有利于酯的水解
D.加热条件下,MnO2既能与浓盐酸又能与稀盐酸反应生成氯气
查看习题详情和答案>>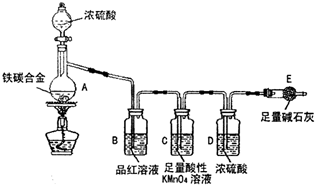 某化学兴趣小组为了测定某铁碳合金(看成铁和碳两种单质的混合物)中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的装置(夹持仪器已省略)和方案进行实验.
某化学兴趣小组为了测定某铁碳合金(看成铁和碳两种单质的混合物)中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的装置(夹持仪器已省略)和方案进行实验.请回答下列问题:
(1)在加热条件下,A中碳与浓硫酸发生反应的化学方程式是
(2)检查上述装置气密性的一种方法是:关闭分液漏斗的活塞,在E后面连上一根导管,然后
(3)若先称量E的质量,并将ag铁碳合金样品放入装置A中,再加入足量浓硫酸,待A中不再逸出气体时,停止加热,拆下E并称重,结果E增重bg.则铁碳合金中铁的质量分数为
(4)装置C的作用
(5)甲同学认为,依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,原因是空气中的CO2、H2O进入E.你认为改进的方法是
某校化学兴趣小组在加热条件下利用二氧化锰与浓盐酸反应来制取并收集氯气.
(1)写出该反应的离子方程式
(2)若要制取纯净干燥的氯气,应使气体依次通过装有
(3)该小组称取8.7g二氧化锰与足量10mol?L-1的浓盐酸反应,理论上可制得氯气的体积(标准状况)V1=
(4)若该小组量取了10mol?L-1的浓盐酸40mL,与足量的二氧化锰反应,理论上产生氯气的体积为V2(标准状况),则V1
查看习题详情和答案>>
(1)写出该反应的离子方程式
MnO2+4H++2C1-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2C1-
Mn2++Cl2↑+2H2O
.
| ||
(2)若要制取纯净干燥的氯气,应使气体依次通过装有
饱和食盐水
饱和食盐水
和浓硫酸
浓硫酸
的洗气瓶.(3)该小组称取8.7g二氧化锰与足量10mol?L-1的浓盐酸反应,理论上可制得氯气的体积(标准状况)V1=
2.24
2.24
L.(4)若该小组量取了10mol?L-1的浓盐酸40mL,与足量的二氧化锰反应,理论上产生氯气的体积为V2(标准状况),则V1
>
>
V2(填“=”、“>”、“<”).其原因是随着反应进行,反应物浓度减小,反应不再进行
随着反应进行,反应物浓度减小,反应不再进行
(不考虑装置的气密性及浓盐酸的挥发).