网址:http://m.1010jiajiao.com/timu_id_405383[举报]
一、1.AD 2.B 3.B 4.D 5.D 6.BC 7.C 8.A?
二、9.C4H10,C9H20或C10H8?
10.(1)CO、H2,物质的量相同,耗O2的量相同?
(2)C2H5OH,CH3―O―CH3,必须是同分异构体?
11.(1)CH≡CH,有机物分子式和结构式的确定.files/image071.jpg) ,(2)CH4,CH3OH
,(2)CH4,CH3OH
12.C5H12;设该烃的分子式为CxHy,则有有机物分子式和结构式的确定.files/image073.gif) =5/1则x/y=5/12所以分子式为C5H12
=5/1则x/y=5/12所以分子式为C5H12
13.(1)x=2,y=1 (2)C2H2O2 (3)18
14.(1)1≤V(O2)/V(C2H6)≤2.5?
当只有CO2与Na2O2反应时,则应通入的O2最多,由2C2H6+5O2+4Na2O2→4Na2CO3+6H2O(l)得V(O2)/V(C2H6)=5/2=2.5?
当C2H6燃烧后产生的CO2和H2O均全部与Na2O2反应时,则通入的O2应最少,由方程式C2H6+O2+5Na2O2→2Na2CO3+6NaOH得V(O2)/V(C2H6)=1/1
故O2与C2H6的体积比x的取值范围为1≤V(O2)/V(C2H6)≤2.5
(2)0.8?
n(Na2O2)=有机物分子式和结构式的确定.files/image075.gif) =0.02mol由
=0.02mol由
有机物分子式和结构式的确定.files/image077.gif) =
=有机物分子式和结构式的确定.files/image079.gif)
有机物分子式和结构式的确定.files/image081.gif) n(O2)=0.025mol故通入O2的质量不能超过
n(O2)=0.025mol故通入O2的质量不能超过
15.(1)n(H2O)=有机物分子式和结构式的确定.files/image083.gif) =0.6moln(CO2)=
=0.6moln(CO2)=有机物分子式和结构式的确定.files/image085.gif) =0.4mol?
=0.4mol?
CuO + CO = Cu + CO2 △m(减量)?
1mol
1mol
n(CO)
有机物分子式和结构式的确定.files/image081.gif)
有机物分子式和结构式的确定.files/image087.gif)
∴实际有机物燃烧产生的CO2为:0.4-0.2=0.2mol?
∴0.2mol有机物中含有机物分子式和结构式的确定.files/image087.gif)
有机物分子式和结构式的确定.files/image081.gif) 1mol有机物中C∶H∶O=2∶6∶2
1mol有机物中C∶H∶O=2∶6∶2
故有机物分子式为:C2H6O2?
(2)n(Na)=有机物分子式和结构式的确定.files/image090.gif) =0.4mol,0.2mol有机物能和0.4molNa反应
=0.4mol,0.2mol有机物能和0.4molNa反应
所以该有机物为二元醇,结构简式为HO―CH2―CH2―OH?
16.(1)有机物分子式和结构式的确定.files/image092.jpg)
2-甲基-1,3-丁二烯(或异戊二烯)?
(2)有机物分子式和结构式的确定.files/image094.jpg) ?聚异戊二烯?
?聚异戊二烯?
爆炸是气体体积在瞬间发生剧烈膨胀的过程.
(1)配平黑火药发生爆炸时的化学方程式:
____KNO3(s)+____C(s)+____S(s)→____K2S(s)+____CO2(g)+____N2(g)
(2)八硝基立方烷(化学式:C8N8O16,相对分子质量:464)是正在研制过程中的一种新型高能炸药,它的密度约为2g·cm-3.发生爆炸时反应的化学方程式为:
C8N8O16(s)→8CO2(g)+4N2(g)
试估算八硝基立方烷爆炸时,折算为标准状况时物质的体积是原物质的多少倍?(取整数值)
(3)等压条件下,一定量的气体体积与温度变化关系为:
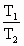 =
=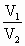 [式中T指绝对温标,T(K)=273+t C]
[式中T指绝对温标,T(K)=273+t C]
当炸药爆炸后气体的温度达到2730K时,气体的体积是标准状况下的多少倍?
(4)根据上述计算分析,你认为影响炸药的爆炸性能的因素是:
________.
查看习题详情和答案>>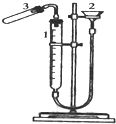 利用右图装置测定金属镁的相对原子质量.请根据要求回答有关问题:(所提供试剂有:0.48克镁带、18.4mol?L-1的H2SO4、2.0mol?L-1的H2SO4)
利用右图装置测定金属镁的相对原子质量.请根据要求回答有关问题:(所提供试剂有:0.48克镁带、18.4mol?L-1的H2SO4、2.0mol?L-1的H2SO4)实验方法如下:
(1)加药品前要检查该装置的气密性,较简便单的方法是:
(2)气密性检验后,按以下步骤进行实验,请回答有关问题:
①装硫酸.取下试管,加入
②放置镁条.为保证产生的氢气不泄漏,应将镁条放置在
③记下量气管起始读数V1. ④将试管竖直,使镁条滑到试管中与酸反应;
⑤记下镁条反应完后的量气管读数V2.如何读数才能减少误差
(3)经测定镁与酸反应产生H2的体积为V L(已折算成标准状况),则镁的相对原子质量的表达式为(相对原子质量用M表示):.
(4)如果测得的值比实际值偏大,请你分析产生误差偏大的可能原因(假设在测得外界温度、压强以及在换算、计算过程中都没有错误.至少写2条)①②.
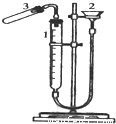
利用下图装置测定金属镁的相对原子质量。请根据要求回答有关问题:(所提供试剂有:0.48克镁带、18.4mol?L-1的H2SO4、2.0 mol?L-1的H2SO4)
 实验方法如下:
实验方法如下:
(1)加药品前要检查该装置的气密性,较简便单的方法是:
。
(2)气密性检验后,按以下步骤进行实验,请回答有关问题:
①装硫酸。取下试管,加入 mol/L的H2SO4且体积应大于 ml。
②放置镁条。为保证产生的氢气不泄漏,应将镁条放置在 。
③记下量气管起始读数V1。
④将试管竖直,使镁条滑到试管中与酸反应;
⑤记下镁条反应完后的量气管读数V2。如何读数才能减少误差 。
(3)经测定镁与酸反应产生H2的体积为V L(已折算成标准状况),则镁的相对原子质量的表达式为(相对原子质量用M表示): 。
(4)如果测得的值比实际值偏大,请你分析产生误差偏大的可能原因(假设在测得外界温度、压强以及在换算、计算过程中都没有错误。至少写2条)
① ② 。
查看习题详情和答案>>实验方法如下:
(1)加药品前要检查该装置的气密性,较简便单的方法是:______.
(2)气密性检验后,按以下步骤进行实验,请回答有关问题:
①装硫酸.取下试管,加入______mol/L的H2SO4且体积应大于______ml.
②放置镁条.为保证产生的氢气不泄漏,应将镁条放置在______.
③记下量气管起始读数V1. ④将试管竖直,使镁条滑到试管中与酸反应;
⑤记下镁条反应完后的量气管读数V2.如何读数才能减少误差______.
(3)经测定镁与酸反应产生H2的体积为V L(已折算成标准状况),则镁的相对原子质量的表达式为(相对原子质量用M表示):.
(4)如果测得的值比实际值偏大,请你分析产生误差偏大的可能原因(假设在测得外界温度、压强以及在换算、计算过程中都没有错误.至少写2条)①②.
 查看习题详情和答案>>
查看习题详情和答案>>
①同温同压条件下,测得它的密度是H2密度的43倍;
②将1.72克该烃完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收)。

实验前 | 实验后 | |
(干燥剂+U型管)的质量 | 101.1g | 103.62g |
(石灰水+广口瓶)的质量 | 312.0g | 317.28g |
(1) 根据上表数据确定该烃的相对分子质量和化学式;(写出计算过程)
(2) 写出该烃所有可能的结构简式.
查看习题详情和答案>>