网址:http://m.1010jiajiao.com/timu_id_405068[举报]
一、1.D 2.B?
3.解析:本题结合原电池原理考查实验现象。Fe作负极:Fe-2e-===Fe2+,C作正极:2H2O+O2+4e-===4OH-。
答案:B?
4.解析:本题要设计成原电池必须满足:①Fe作负极;②C、Pt或活动性比Fe弱的金属作正极;③电解质溶液中必须含Fe3+。
答案:CD?
5.C 6.D?
7.解析:正极反应MnO2+e-===MnO 。则n(MnO2)=n(e-)=
。则n(MnO2)=n(e-)=
答案:C?
8.BD 9.B?
二、10.(1)D (2)加CuSO4溶液后,构成Fe―Ag原电池,Fe溶解,质量减小;
Cu2+在银圈上得电子,沉积在Ag上,质量增加?
11.2CO2+O2+4e- 2CO
2CO 2CO+O2
2CO+O2 2CO2
2CO2
12.(1)H2 O2 2H2+4OH--4e-===4H2O?
O2+2H2O+4e-===4OH-?
(2)2H2-4e-===4H+ O2+4H++4e-===2H2O?
前者的pH变小,后者的pH变大。?
(3)CH4+10OH--8e-===CO +7H2O?
+7H2O?
4H2O+2O2+8e-===8OH-?
13.(1)反应速率可以用反应的消耗速率,也可以用产物的生成速率来表示?
(2)直线(y=0.05at)
抛物线(y′=bt )
)
(3)Ni 它的腐蚀速率随时间增长比镁慢?
14.(1)化学 电 离子 ①②③④?
(2)电解质 大 零?
(3)①二 ⅠA ②镉 负?
15.(1)Cu2++2H2O Cu(OH)2+2H+
Cu(OH)2+2H+
(2)因为Cu2++2e-===Cu,使Cu2+水解平衡向左移动,c(H+)减少,pH上升。
(3)pH降低 测定溶液pH?
(4)同意实验派观点;理由是CuCl2===Cu+Cl2↑
Cl2+H2O===HCl+HClO,使溶液酸性增强,pH降低。
 关于“电解氯化铜溶液时的pH变化”问题,化学界有以下两种不同的观点:观点一是:“理论派”认为电解氯化铜溶液后溶液的pH升高.观点二是:“实验派”经过反复、多次、精确的实验测定,证明电解氯化铜溶液时pH的变化如图曲线的关系.?请回答下列问题:
关于“电解氯化铜溶液时的pH变化”问题,化学界有以下两种不同的观点:观点一是:“理论派”认为电解氯化铜溶液后溶液的pH升高.观点二是:“实验派”经过反复、多次、精确的实验测定,证明电解氯化铜溶液时pH的变化如图曲线的关系.?请回答下列问题:(1)电解前氯化铜溶液的pH处在A点位置的原因是
| 水解 |
| 水解 |
(2)“理论派”所持观点的理论依据是
(3)你持何种观点?
| ||
| ||

(2)“理论派”所持观点的理论依据是________________________________ 。
(3)你持何种观点?___________(填“理论派”或“实验派”)理由是_________________________ (从化学原理加以简述)。
(1)电解前氯化铜溶液的pH处在A点位置的原因是______
 查看习题详情和答案>>
查看习题详情和答案>>
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.5kJ?mol-1
①在一体积为2L的密闭容器中,加入1mol C和2mol H2O(g),达平衡H2O(g)的转化率为20%,请计算此时的平衡常数
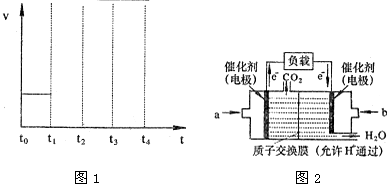
②若容器体积不变,反应在t0时达到平衡,平衡常数为K1;在t1时升高温度,t2重新达到平衡,平衡常数为K2;t3时充入水蒸气,t4时重新达到平衡;平衡常数为K3;请在下面的反应速率与时间关系图1中用直线画出t1到t4正反应速率的变化情况,并比较K1、K2、K3的数值 (用“>”、“<”或“=”)
③又知C(s)+CO2(g)?2CO(g)△H=+172.5kJ?mol-1,则CO(g)+H2O(g)?CO2(g)+H2(g)的焓变△H为
(2)CO与H2在一定条件下可反应生成甲醇,CO(g)+2H2(g)?CH3OH(g).甲醇是一种燃料,可用于设计燃料电池.图2是甲醇燃料电池的原理示意图,电解质溶液为稀硫酸.
①a处通入的是
②该电池工作过程中,H+的移动方向为从
(1)该实验缺少的仪器是
(2)酸液都取足量、相同体积,请你帮助完成以下面实验设计表:
| 实验编号 | 温度(K) | 盐酸浓度(mol?L-1) | 醋酸浓度(mol?L-1) | 实验目的 |
| ① | 298 | 0.20 | a.实验①和②是探究 不同温度 不同温度 对镁与盐酸反应速率的影响;b.实验①和③是探究 不同浓度 不同浓度 对镁与盐酸反应速率的影响;c.实验①和④是探究相同温度下,相同浓度的盐酸、醋酸与镁反应速率的区别. | |
| ② | 308 | 0.20 | ||
| ③ | 298 | 0.40 | ||
| ④ | 298 298 |
0.20 0.20 |
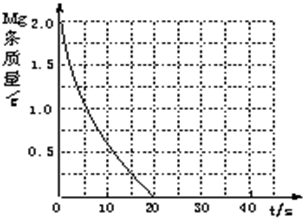
(4)若(2)中实验①镁条消失的时间是20s,则镁条剩余质量与时间关系图如右图.假设:该反应温度每升高10℃,反应速率是原来的2倍;温度相同、浓度相同时,醋酸的平均反应速度是盐酸的
| 1 |
| 2 |
(5)某温度下,醋酸的电离平衡常数K(CH3COOH)=1.0×10-5.若醋酸的起始浓度为0.10mol/L,则平衡时溶液的pH值是多少?(写出计算过程)