网址:http://m.1010jiajiao.com/timu_id_404408[举报]
一、1.B 2.A?
3.解析:v(NH3)∶v(O2)∶v(NO)∶v(H2O)=4∶5∶4∶6。
答案:D?
4.BC 5.B 6.B 7.D 8.BD?
9.解析:由①②组数据解得m=1,由②③组数据解得n= 。
。
答案:D
二、10.(1)0.013 (2)1.0 催化剂 (3)> >
(4)吸热 温度升高时,平衡向右移动?
11.①
12.④>③=②>①?
13.
 (
( -x)?mol?L-1?min-1
-x)?mol?L-1?min-1
14.(1)1∶50 根据勒夏特列原理,通入过量而廉价的氧气,可提高SO2的转化率
(2)废气中每小时排出的SO2的体积为:1
(3)SO2 ~ 2NH3 ~ (NH4)2SO4?
 mol?
mol?
 mol
mol
 mol
mol
故可得(NH4)2SO4: mol×1
mol×1
消耗氨气: mol×2×1
mol×2×1
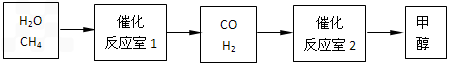
(1)在压强为0.1MPa条件下,反应室2(容积为VL)中a mol CO与2a mol H2在催化剂作用下反应生成甲醇:CO (g) +2H2(g)
 CH3OH (g),CO的平衡转化率与温度、压强的关系如图所示,则:
CH3OH (g),CO的平衡转化率与温度、压强的关系如图所示,则: 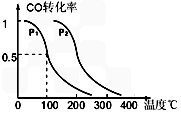
A.高温高压 B.加入催化剂 C.增加CO的浓度 D.增大氢气的浓度 E分离出甲醇
②在压强P1、100℃时,CH3OH(g)
 CO(g) + 2H2(g)反应的平衡常数为________(用含a、V的代数式表示)
CO(g) + 2H2(g)反应的平衡常数为________(用含a、V的代数式表示) ③将一定量的NO2与SO2置于绝热恒容密闭容器中发生NO2(g)+SO2(g)
 SO3(g)+NO(g)上述反应,正反应速率随时间变化的趋势如图所示。由图可知下列说法正确的是__________(填字母)。
SO3(g)+NO(g)上述反应,正反应速率随时间变化的趋势如图所示。由图可知下列说法正确的是__________(填字母)。 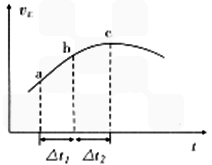
B.反应物浓度:a点小于b点
C.反应物的总能量高于生成物的总能量
D.△t1=△t2时,SO2的消耗量:a~b段大于b~c段
(2)据报道,科学家在实验室已研制出在燃料电池的反应容器中,利用特殊电极材料以H2和O2为原料制取过氧化氢的新工艺。原理如图所示:请写出甲电极的电极反应式:________________________。
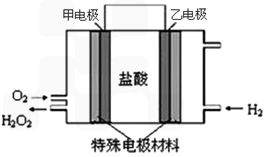
(4)已知在常温常压下:
①2CH3OH (l)+3O2(g) == 2CO2(g)+4H2O (g) ΔH1=-1275.6 kJ/mol
②2CO (g)+O2(g) == 2CO2(g) ΔH2=-566.0 kJ/mol
③H2O (g) = H2O (l) ΔH3=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:_____________________。
(10分)请回答下列问题:
(1)等温、等容下,已知2NO+O2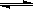 2NO2 △H<0,当该反应处于平衡状态时,下列措施中有利于提高NO的平衡转化率的是 (填字母)。
2NO2 △H<0,当该反应处于平衡状态时,下列措施中有利于提高NO的平衡转化率的是 (填字母)。
| A.升高温度 | B.降低温度 | C.加入O2 | D.减小压强 |
(2)若将l.00 molO2和2.00 mol NO混合充入容积为2 L的密闭容器中,3分钟后反应达到平衡。平衡后混合气体总物质的量为2.55mol,用O2表示的化学反应速率为 mol?L-1?min-1。
(3)容积均为2 L的四个密闭容器中均进行着(2)中的反应,某温度下,各物质物质的量(mol)及正逆反应速率关系如下表所示:
| 容器编号 | n(O2) | n(NO) | n (NO2) | v正与v逆的关系 |
| Ⅰ | 0.20 | 0.10 | 0.20 | v正=v逆 |
| Ⅱ | 0.20 | 0.40 | 1.00 | ②v正___v逆? |
| Ⅲ | 0.60 | 1.20 | 0.80 | ③v正___v逆? |
填写表中空格: ② ③ (填>或 <) 查看习题详情和答案>>
(10分)请回答下列问题:
(1)等温、等容下,已知2NO+O2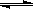 2NO2 △H<0,当该反应处于平衡状态时,下列措施中有利于提高NO的平衡转化率的是
(填字母)。
2NO2 △H<0,当该反应处于平衡状态时,下列措施中有利于提高NO的平衡转化率的是
(填字母)。
A.升高温度 B.降低温度 C.加入O2 D.减小压强
E.加入催化剂 F.增加NO的量
(2)若将l.00 molO2和2.00 mol NO混合充入容积为2 L的密闭容器中,3分钟后反应达到平衡。平衡后混合气体总物质的量为2.55mol,用O2表示的化学反应速率为 mol•L-1•min-1。
(3)容积均为2 L的四个密闭容器中均进行着(2)中的反应,某温度下,各物质物质的量(mol)及正逆反应速率关系如下表所示:
|
容器编号 |
n(O2) |
n(NO) |
n (NO2) |
v正与v逆的关系 |
|
Ⅰ |
0.20 |
0.10 |
0.20 |
v正=v逆 |
|
Ⅱ |
0.20 |
0.40 |
1.00 |
②v正___v逆? |
|
Ⅲ |
0.60 |
1.20 |
0.80 |
③v正___v逆? |
①若方程式系数为最简整数比,则该温度下的平衡常数K=
填写表中空格: ② ③ (填>或 <)
查看习题详情和答案>>
(1)等温、等容下,已知2NO+O2
 2NO2 △H<0,当该反应处于平衡状态时,下列措施中有利于提高NO的平衡转化率的是 (填字母)。
2NO2 △H<0,当该反应处于平衡状态时,下列措施中有利于提高NO的平衡转化率的是 (填字母)。| A.升高温度 | B.降低温度 | C.加入O2 | D.减小压强 |
(2)若将l.00 molO2和2.00 mol NO混合充入容积为2 L的密闭容器中,3分钟后反应达到平衡。平衡后混合气体总物质的量为2.55mol,用O2表示的化学反应速率为 mol?L-1?min-1。
(3)容积均为2 L的四个密闭容器中均进行着(2)中的反应,某温度下,各物质物质的量(mol)及正逆反应速率关系如下表所示:
| 容器编号 | n(O2) | n(NO) | n (NO2) | v正与v逆的关系 |
| Ⅰ | 0.20 | 0.10 | 0.20 | v正=v逆 |
| Ⅱ | 0.20 | 0.40 | 1.00 | ②v正___v逆? |
| Ⅲ | 0.60 | 1.20 | 0.80 | ③v正___v逆? |
填写表中空格: ② ③ (填>或 <)
在2 L 密闭容器内,800℃时反应2 NO(g)+O2(g)![]() 2 NO2(g)体系中,n(NO)随时间的变化如下表所示:
2 NO2(g)体系中,n(NO)随时间的变化如下表所示:
| 时间 (s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应 (填“是”或“不是”)可逆反应,第5 s 时,c(NO2)=
(2)如下图所示,表示NO2变化的曲线是 ;用O2表示从0 s — 2 s 内该反应的平均速率v(O2)=

(3)不能说明该反应已达到平衡状态的是
a. 容器内压强保持不变 b. v (NO2)=2v(O2)
c. 容器内密度保持不变 d. 2 v逆 (NO)=v正(O2)
查看习题详情和答案>>