摘要:(2)天然的和绝大部分人工制备的晶体都存在各种缺陷.例如在某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺.另有两个Ni2+被两个Ni3+所取代.其结果.晶体仍呈电中性.但化合物中Ni和O的比值却发生了变化.某氧化镍样品组成为Ni0.97O.试计算该晶体中Ni3+与Ni2+的离子数之比.?
网址:http://m.1010jiajiao.com/timu_id_404026[举报]
一、1.C 2.A 3.C?
4.解析:比较物质熔、沸点高低时,首先判断晶体类型。一般是,原子晶体>离子晶体>分子晶体;然后比较同一类型晶体中,粒子间的作用力。共价键比键长,离子键看离子半径和电荷数,分子间作用力主要比分子量的大小。(注意氢键的存在)?
答案:B?
5.D 6.D 7.B?
8.解析:每一个环内电子数为3×5+3×7=36,与石墨层中一个环内电子数6×6=36是相同的,故与石墨为“等电子体”,性质类似石墨。?
答案:B?
9.解析:每个碳原子为三个六元环所共有,则每个正六边形所占有的碳原子数为6× =
=
2个。
答案:D?
10.D 11.B?
二、12.6 109°28′ 2 W??

2Na2O2+2H2O===4NaOH+O2↑?
(5)离子 S2-+H2O HS-+OH- HS-+H2O
HS-+OH- HS-+H2O H2S+OH-?
H2S+OH-?
16.(1)密度= g?cm-3?
g?cm-3?
(2)6∶91
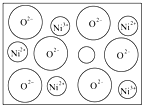 天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代.其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化.其氧化镍样品组成为Ni0.97O,试计算该晶体中Ni2+与Ni3+的离子数之比.
天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代.其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化.其氧化镍样品组成为Ni0.97O,试计算该晶体中Ni2+与Ni3+的离子数之比.
天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代.其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化.其氧化镍样品组成为Ni0.97O,试计算该晶体中Ni2+与Ni3+的离子数之比.
 查看习题详情和答案>>
查看习题详情和答案>>
 查看习题详情和答案>>
查看习题详情和答案>>
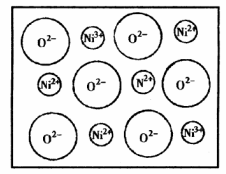
天然的和绝大部分人工制备的晶体都存在各种缺陷,例如,在某种![]() 晶体中就存在如下图所示的缺陷:一个
晶体中就存在如下图所示的缺陷:一个![]() 空缺,另有两个
空缺,另有两个![]() 被两个
被两个![]() 所取代.其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化.某氧化镍样品组成为
所取代.其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化.某氧化镍样品组成为![]() ,试计算该晶体中
,试计算该晶体中![]() 与
与![]() 的离子数之比.
的离子数之比.
 查看习题详情和答案>>
查看习题详情和答案>>

