摘要:在理解单一章节的同时.注意前后联系一轮复习特别要做好这方面准备.我们的学生多数是这样的情况:复习到前面.后面的内容记不得,复习到后面.前面的内容还给老师了.我早就在想能不能像华师一一样.一轮就进行综合练习.这样的前联后展最大的好处就是对知识中重要的或者共性的内容放在一起比较.强化记忆.例如:向某溶液中通CO2.变浑浊的溶液有哪些?初中学过澄清石灰水.碱金属族饱和Na2CO3.碳族的Na2SiO3.金属族的NaAlO2.有机物里面的浓苯酚钠.
网址:http://m.1010jiajiao.com/timu_id_403700[举报]
大量排放CO2会加重温室效应,影响地球大气环境.为减少CO2对环境的影响,世界各国在限制其排放量的同时加强了对CO2创新利用的研究,如致力于二氧化碳的“组合转化”技术研究,把过多的二氧化碳转化为有益于人类的物质,如甲醇、CH4、汽油 等.
I.目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作致冷剂已经成为一种趋势,这一做法的积极意义在于 .
II.有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经过化学反应后使之变为可再生燃料甲醇.“绿色自由”构想技术流程如下:
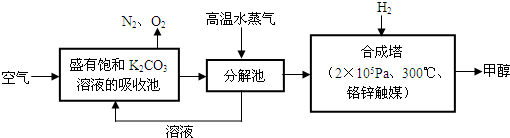
(1)吸收池中反应的化学方程式为: .
(2)在合成塔中,若有4.4kgCO2与足量H2恰好完全反应,可放出4947kJ的热量,试写出合成塔中发生反应的热化学方程式 .
(3)控制不同的反应条件,CO2和H2反应还可以得到其它有机物.如将CO2和H2以1:4的体积比混合,在适当条件下反应,可获得重要能源CH4:CO2+4H2=CH4+2H2O;如将CO2和H2以1:3的体积比混合,还可生成某种重要的化工原料和水,该化工原料可能是 .
A.烷烃 B.烯烃 C.炔烃 D.芳香烃
(4)已知在443~473K时,用钴(Co)作催化剂可使CO2和H2生成C5~C8的烷烃,这是人工合成汽油的方法之一.要达到汽油的要求,CO2和H2体积比的取值范围应是 .
Ⅲ.若在一密闭恒容容器中充入CO2和H2的物质的量分别为1mol和3mol,发生反应得到CH3OH(g)和H2O(g).测得CO2和CH3OH(g)的浓度随时间变化如图所示:
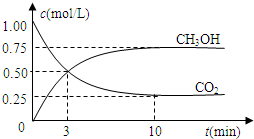
(1)从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L?min).
(2)下列措施中能使n(CH3OH)/n(CO2)增大的是 .
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2.
查看习题详情和答案>>
I.目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作致冷剂已经成为一种趋势,这一做法的积极意义在于
II.有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经过化学反应后使之变为可再生燃料甲醇.“绿色自由”构想技术流程如下:

(1)吸收池中反应的化学方程式为:
(2)在合成塔中,若有4.4kgCO2与足量H2恰好完全反应,可放出4947kJ的热量,试写出合成塔中发生反应的热化学方程式
(3)控制不同的反应条件,CO2和H2反应还可以得到其它有机物.如将CO2和H2以1:4的体积比混合,在适当条件下反应,可获得重要能源CH4:CO2+4H2=CH4+2H2O;如将CO2和H2以1:3的体积比混合,还可生成某种重要的化工原料和水,该化工原料可能是
A.烷烃 B.烯烃 C.炔烃 D.芳香烃
(4)已知在443~473K时,用钴(Co)作催化剂可使CO2和H2生成C5~C8的烷烃,这是人工合成汽油的方法之一.要达到汽油的要求,CO2和H2体积比的取值范围应是
Ⅲ.若在一密闭恒容容器中充入CO2和H2的物质的量分别为1mol和3mol,发生反应得到CH3OH(g)和H2O(g).测得CO2和CH3OH(g)的浓度随时间变化如图所示:

(1)从反应开始到平衡,氢气的平均反应速率v(H2)=
(2)下列措施中能使n(CH3OH)/n(CO2)增大的是
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2.
 (2013?绵阳模拟)为减小C02对环境的影响,在倡导“低碳”的同时,还需加强对C02创新利用的研究.T1℃时,将9molC02和12molH2充入3L密闭容器中,发生反 应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H<0,容器中CH3OH的物质的量随时间变化如曲线I所示,平衡时容器内压强为仍为P1.改变某一条件重新进行上述反应,CH3OH的物 质的量随时间变化如曲线II所示.下列说法错误的是( )
(2013?绵阳模拟)为减小C02对环境的影响,在倡导“低碳”的同时,还需加强对C02创新利用的研究.T1℃时,将9molC02和12molH2充入3L密闭容器中,发生反 应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H<0,容器中CH3OH的物质的量随时间变化如曲线I所示,平衡时容器内压强为仍为P1.改变某一条件重新进行上述反应,CH3OH的物 质的量随时间变化如曲线II所示.下列说法错误的是( ) (2013?红桥区二模)为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用的研究.
(2013?红桥区二模)为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用的研究.(1)①把含有较高浓度CO2的空气通入饱和K2CO3溶液.
②在①的吸收液中通高温水蒸气得到高浓度的CO2气体.
写出②中反应的化学方程式
2KHCO3
K2CO3+H2O+CO2↑
| ||
2KHCO3
K2CO3+H2O+CO2↑
.
| ||
(2)如将CO2与H2 以1:3的体积比混合.
①适当条件下合成某烃和水,该烃是
B
B
(填序号).A.烷烃 B.烯烃 C.炔烃 D.苯的同系物
②适当条件下合成燃料甲醇和水.在体积为2L的密闭容器中,充入 2mol CO2和6mol H2,一定条件下发生反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.
测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
从反应开始到平衡,v(H2)=
0.225mol/(L?min)
0.225mol/(L?min)
;氢气的转化率=75%
75%
;能使平衡体系中n(CH3OH)增大的措施有降低温度(或加压或增大H2的量等)
降低温度(或加压或增大H2的量等)
.(3)如将CO2与H2 以1:4的体积比混合,在适当的条件下可制得CH4.已知:
CH4 (g)+2O2(g)═CO2(g)+2H2O(l)△H1=-890.3kJ/mol
H2(g)+1/2O2(g)═H2O(l)△H2=-285.8kJ/mol
则CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式是
CO2(g)+4H2(g)═CH4(g)+2H2O(l)△H=-252.9kJ/mol
CO2(g)+4H2(g)═CH4(g)+2H2O(l)△H=-252.9kJ/mol
.(4)某同学用沉淀法测定含有较高浓度CO2的空气中CO2的含量,经查得一些物质在20℃的数据如下表.
| 溶解度(S)/g | 溶度积(Ksp) | ||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 |
吸收CO2最合适的试剂是
Ba(OH)2
Ba(OH)2
(填“Ca(OH)2”或“Ba(OH)2”)溶液,实验时除需要测定工业废气的体积(折算成标准状况)外,还需要测定BaCO3的质量
BaCO3的质量
.
SO2是造成空气污染及酸雨的有害气体,研究SO2的性质可使其变废为宝.
(1)某小组设计了如图1所示的实验装置(图中夹持和加热装置略去).
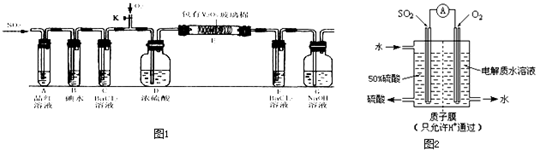
①若关闭K,通入SO2,装置A中发生的现象是 ;当装置B中溶液颜色逐渐退去时,其内发生反应的离子方程式为 ,此时装置C、D、E、F、G中均没有明显反应现象发生.
②若对装置E加热并通入SO2,同时打开K通入O2,装置F中产生白色浑浊,证明装置E中发生的反应(化学方程式表示): ;装置G的作用是 .
③反应结束后,若向试管C溶液中,加入足量下列溶液也可产生白色沉淀的是 .
A.氨水 B.稀盐酸 C.硝酸钾溶液
(2)根据原电池原理,设计了如图2所示装置,电极为含某催化剂、多孔吸附性的惰性材料,在用SO2发电的同时实现了硫酸制备.通入SO2的一极发生的反应: ;电池发生的总反应: .
查看习题详情和答案>>
(1)某小组设计了如图1所示的实验装置(图中夹持和加热装置略去).

①若关闭K,通入SO2,装置A中发生的现象是
②若对装置E加热并通入SO2,同时打开K通入O2,装置F中产生白色浑浊,证明装置E中发生的反应(化学方程式表示):
③反应结束后,若向试管C溶液中,加入足量下列溶液也可产生白色沉淀的是
A.氨水 B.稀盐酸 C.硝酸钾溶液
(2)根据原电池原理,设计了如图2所示装置,电极为含某催化剂、多孔吸附性的惰性材料,在用SO2发电的同时实现了硫酸制备.通入SO2的一极发生的反应: