网址:http://m.1010jiajiao.com/timu_id_4004553[举报]
 实验室制备少量硝基苯的主要步骤如下:
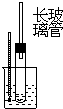
实验室制备少量硝基苯的主要步骤如下:①配制浓硫酸与浓硝酸的混和酸,加入如图所示反应器中.
②向室温下的混和酸中逐滴加入一定量的苯,充分振荡,混合均匀.
③在50-60℃下发生反应,直至反应结束.
④除去混和酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤.
⑤用无水CaCl2干燥、分离后得到纯硝基苯.回答下列问题:
(1)配制一定比例的浓硫酸与浓硝酸的混合酸时,操作的注意事项是
(2)装置中,长玻璃管的作用是
(3)步骤④中洗涤、分离粗硝基苯应使用的仪器是
(4)步骤⑤中的分离方法是

(1)写出上述流程中X物质的分子式
(2)使原料氯化钠的利用率从70%提高到90%以上,主要涉及了
(3)该实验得到的纯碱中含有氯化钠,甲同学设计如图3装置Ⅰ,拟通过测定烧杯中氢氧化钠溶液的增重来测定样品中碳酸钠的含量,但该实验存在明显不足,试举出该装置引起误差的两个主要原因:
①
②
(4)乙同学设计的测定样品中纯碱含量的方法如图3Ⅱ,试回答:
①检查该装置气密性的方法为:
②设滴定管的起始读数为V1mL,终了读数为V2mL,注射器收集的气体为V3mL(标准状况),称得样品质量为m g,则原样品中碳酸钠的质量分数的表达式为
| V3-(V2-V1) |
| 22400m |
| V3-(V2-V1) |
| 22400m |
(5)丙同学设计的测定样品中纯碱含量的方法如图3Ⅲ,并在广口瓶中的水上面滴加少量植物油,试回答:
①你认为植物油的作用是
②为减小误差,读取量筒中水的体积时的注意事项有:
甲组:将铜粉投入盛有稀硫酸的容器中,无反应.向容器底部缓缓鼓入氧气,溶液慢慢变蓝色,若在溶液中放置些铂丝,反应速率明显加快.
乙组:Cu
 CuO
CuO CuSO4
CuSO4 丙组:Cu
 Cu(NO3)2
Cu(NO3)2 Cu(OH)2
Cu(OH)2 CuSO4
CuSO4丁组:Cu
 CuSO4
CuSO4(1)甲组实验用一个化学反应方程式表示: ;使反应变快的可能原因是 ;从该反应器溶液(含有少量H2SO4以抑制水解)中取得产品的实验操作步骤应为 、 、过滤并洗涤晶体,取得产品后的残留物质可循环使用.
(2)可持续发展的原则要求化工生产①原理科学;②能量消耗低;③原料利用率高;④无污染.则在四组方案中, 组方案最好.
II.另一化学兴趣小组从化学手册上查得硫酸铜500℃以上按照下式分解:CuSO4
 CuO+SO2↑+SO3↑+O2↑为此他们设计了如图所示实验装置测定有关数据,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数.
CuO+SO2↑+SO3↑+O2↑为此他们设计了如图所示实验装置测定有关数据,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数.
实验测得数据及有关结果如下;
①准确称取4.80g无水CuSO4;②实验结束时干燥管D总质量增加1.92g;③测得量筒F中水的体积,得出气体在标准状况下的体积为224.0mL.试回答下列问题:
(3)装置B的作用是 .
(4)装置C的作用是 .
(5)为减少测量气体体积引起的误差,应注意的事项有:
①装置内气体的温度应恢复到室温,②调节量筒使其液面与E装置中的液面持平,③
(6)通过计算,推断出该条件下反应的化学方程式 . 查看习题详情和答案>>
(12分)I.下列是四组同学用铜制取硫酸铜晶体的方案:
甲组:将铜粉投入盛有稀硫酸的容器中,无反应。向容器底部缓缓鼓入氧气,溶液慢慢变蓝色,若在溶液中放置些铂丝,反应速率明显加快。
![]()
![]() 乙组: Cu CuO CuSO4
乙组: Cu CuO CuSO4
![]()
![]()
![]() 丙组: Cu Cu(NO3)2 Cu(OH)2 CuSO4
丙组: Cu Cu(NO3)2 Cu(OH)2 CuSO4
![]() 丁组: Cu CuSO4
丁组: Cu CuSO4
(1)甲组实验用一个化学反应方程式表示: ;
使反应变快的可能原因是 ;从该反应器溶液(含有少量H2SO4以抑制水解)中取得产品的实验操作步骤应为 、
过滤并洗涤晶体,取得产品后的残留物质可循环使用。
(2)可持续发展的原则要求化工生产①原理科学;②能量消耗低;③原料利用率高;④无污染。则在四组方案中, 组方案最好。
II.另一化学兴趣小组从化学手册上查得硫酸铜500℃以上按照下式分解:
CuSO4![]() CuO+SO2↑+SO3↑+O2↑
CuO+SO2↑+SO3↑+O2↑
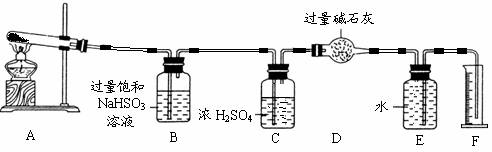 为此他们设计了如下图所示实验装置测定有关数据,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数。
为此他们设计了如下图所示实验装置测定有关数据,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数。
实验测得数据及有关结果如下;
①准确称取4.80g无水CuSO4;
②实验结束时干燥管D总质
量增加1.92g;③测得量筒F中水的体积,得出气体在标准状况下的体积为224.0mL。试回答下列问题:
(3)装置B的作用是 。
(4)装置C的作用是 。
(5)为减少测量气体体积引起的误差,应注意的事项有:
① 装置内气体的温度应恢复到室温,
② 调节量筒使其液面与E装置中的液面持平,
③ 。
(6)通过计算,推断出该条件下反应的化学方程式
查看习题详情和答案>>甲组:将铜粉投入盛有稀硫酸的容器中,无反应.向容器底部缓缓鼓入氧气,溶液慢慢变蓝色,若在溶液中放置些铂丝,反应速率明显加快.
乙组:Cu
| ||
| △ |
| ||
| △ |
丙组:Cu
| 硝酸银 |
| 氢氧化钠 |
| 稀H2SO4 |
丁组:Cu
| ||
| △ |
(1)甲组实验用一个化学反应方程式表示:______;使反应变快的可能原因是______;从该反应器溶液(含有少量H2SO4以抑制水解)中取得产品的实验操作步骤应为______、______、过滤并洗涤晶体,取得产品后的残留物质可循环使用.
(2)可持续发展的原则要求化工生产①原理科学;②能量消耗低;③原料利用率高;④无污染.则在四组方案中,______组方案最好.
II.另一化学兴趣小组从化学手册上查得硫酸铜500℃以上按照下式分CuSO4
| ||

实验测得数据及有关结果如下;
①准确称取4.80g无水CuSO4;②实验结束时干燥管D总质量增加1.92g;③测得量筒F中水的体积,得出气体在标准状况下的体积为224.0mL.试回答下列问题:
(3)装置B的作用是______.
(4)装置C的作用是______.
(5)为减少测量气体体积引起的误差,应注意的事项有:______
①装置内气体的温度应恢复到室温,②调节量筒使其液面与E装置中的液面持平,③______
(6)通过计算,推断出该条件下反应的化学方程式______.