摘要:21. 由几种离子化合物组成的混合物.含有以下离子中的若干种:K+.Cl-.NH.Mg2+.CO.Ba2+.SO.将该混合物溶于水后得澄清溶液.现取3份100 mL该溶液分别进行如下实验: 实验 序号 实验内容 实验结果 1 加AgNO3溶液 有白色沉淀生成 2 加足量NaOH溶液并加热 收集到气体1.12 L(已折算成标准状况下的体积) 3 加足量BaCl2溶液时.对所得沉淀进行洗涤.干燥.称量,再向沉淀中加足量稀盐酸.然后干燥.称量 第一次称量读数为6.27 g.第二次称量读数为2.33 g 试回答下列问题: (1)根据实验1对Cl-是否存在的判断是 (填“一定存在 “一定不存在 或“不能确定 ),根据实验1-3判断混合物中一定不存在的离子是 . (2)试确定溶液中一定存在的阴离子及其物质的量浓度: 阴离子符号 物质的量浓度 (3)试确定K+是否存在? .判断的理由是 .
网址:http://m.1010jiajiao.com/timu_id_4000943[举报]
 (2010?临沂一模)某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验以下实验:将pH═2的两种酸溶液HA,HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:
(2010?临沂一模)某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验以下实验:将pH═2的两种酸溶液HA,HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:(1)HA为
强
强
酸,HB为弱
弱
酸;(填“强“或“弱“)(2)若c=9,则稀释后的三种溶液中,由水电离的氢离子浓度的大小顺序为
MOH═HA>HB
MOH═HA>HB
(用酸、碱化学式表示);将稀释后的HA溶液利MOH溶液取等体积混合,则所得溶液中c(A-)与c(M+)的大小关系为等于
等于
;(填“大于“、“小于“或“等于“)(3)若b+c=14,则MQH为
弱
弱
碱(填“强“或“弱“).将稀释后的HB溶液和MOH溶液取等体积混合,所得很合溶液的pH等于
等于
7(填“大于“、“小于“或“等于“)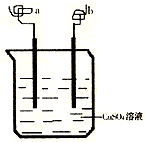 (2010?临沂一模)如图所示,a、b两电极材料分别为铁丝和铜丝.则以下说法不正确的是( )
(2010?临沂一模)如图所示,a、b两电极材料分别为铁丝和铜丝.则以下说法不正确的是( )


