网址:http://m.1010jiajiao.com/timu_id_3998364[举报]
2Na2O2+2CO2═2Na2CO3+O2 2Na2O2+2H2O=4NaOH+O2↑
然而,过氧化钠与其他非金属氧化物(如:NO、NO2等)的反应能否发生呢?为此,某校化学兴趣小组设计了以下实验进行探究:
步骤一:NO、NO2的制备
①本实验所用的NO由饱和硫酸亚铁溶液与浓硫酸和粉末状硝酸钾反应制备,在酸性环境中硝酸根离子被还原为NO,得到的NO的纯度约为98%;
反应的化学方程式为:
②NO2由硝酸铅受热分解得到:2Pb(NO3)2=2PbO+4NO2↑+O2↑使生成的气体通过
A.装有H2O的洗气瓶 B.置于冰水中的U形管(NO2沸点21℃)
C.装有浓硫酸的洗气瓶 D.装有Na2SO3溶液的洗气瓶
步骤二:操作(如图,b、c为弹簧夹)
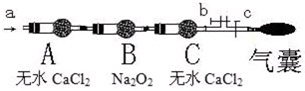
①先打开b关闭c,通入
A.空气 B.O2C.CO2 D.N2
②然后
现象:当通入NO时,B中靠近A侧浅黄色固体变成黄色,气囊未见鼓起;当通入NO2时,B中靠近A侧浅黄色固体变成白色,气囊也未见鼓起;
步骤三:产物检验
分别取出B中黄色固体或白色固体进行检验,得知两种固体均为盐.
结论:
请写出NO2与 Na2O2反应的化学方程式:
| A、反式脂肪酸甘油酯不能使酸性高锰酸钾溶液褪色 | B、油脂是人类的营养物质之一,进入人体后,在胃中水解产生高级脂肪酸和甘油 | C、天然动物脂肪中不含反式脂肪酸,可大量食用 | D、脂肪酸甘油酯顺式变反式,主要是在氢化过程中产生的变化 |
(12分)氧化锌为白色粉末,无臭、无味,广泛应用于橡胶、涂料、陶瓷、化工、医药、玻璃和电子等行业,为了变废为宝,综合应用资源,经常从锌冶炼、锌制品加工企业回收的废渣(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质)来制取氧化锌,其流程如下图所示:
有关氢氧化物沉淀完全的pH见下表
回答下列问题
(1)在酸浸过程中,经常要保持酸过量,而且要通入空气,理由是 。
(2)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有 。
(3)在“除杂Ⅰ”步骤中,经常使用酸性高锰酸钾溶液,并调节溶液的pH。将溶液调至pH=4的目的是 。
(4)在“碳化合成”中,生成的产物之一为碱式碳酸锌[Zn2(OH)2CO3],请写出碳化合成步骤的化学方程式 。
(5)在“洗涤”过程中,证明沉淀洗涤完全的标志是 。
(6)由于本工艺液固分离次数较多,明显的不足是 。
2010年11月6日,中央电视台《经济半小时》节目播放了有关氢化油和反式脂肪酸的内容,引起全国民众的持续关注,下列有关说法不正确的是 ( )
A.反式脂肪酸甘油酯不能使酸性高锰酸钾溶液褪色
B.油脂是人类的营养物质之一,进入人体后,在胃中水解产生高级脂肪酸和甘油
C.大豆油中也有反式脂肪酸甘油酯,只是含量相对较低
D.反式脂肪酸甘油酯顺式变反式,主要是在氢化过程中产生的变化
查看习题详情和答案>>
氧化锌粉末广泛应用于橡胶、涂料、陶瓷、化工、医药、玻璃等行业,为综合应用资源,常从冶炼锌、锌制品加工企业回收的锌渣(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质)来制取氧化锌,流程如图:

有关氢氧化物沉淀完全的pH见下表:

(1)在酸浸过程中,常将锌渣碎成粉末并通入空气,同时保持酸过量,理由是 。
(2)上述工艺多处涉及“过滤”,实验室中过滤需要使用的玻璃仪器有烧杯、 。
(3)①在“除杂Ⅰ”中,常用酸性KMnO4溶液,其目的是 ,KMnO4是该反应的 (氧化剂、还原剂)。将溶液的pH调至4,目的是 。
②在“除杂II”中,加入锌粉的目的是 。
(4)在“碳化合成”中,产物中有碱式碳酸锌[Zn2(OH)2CO3]和CO2等,请写出该反应的化学方程式 。
(5)本工艺中,过滤分离次数较多,其明显的缺陷是 。
查看习题详情和答案>>