网址:http://m.1010jiajiao.com/timu_id_399793[举报]
我国某大型电解铜生产企业,其冶炼工艺中铜、硫回收率达到97%、87%。下图表示其冶炼加工的流程:Ks5u
 |
冶炼中的主要反应:Cu2S + O2 ====== 2Cu + SO2
(1)烟气中的主要废气是________________,从提高资源利用率和减排考虑,其综合利用方式是制___________。
(2)电解法炼铜时,阳极是____________(填“纯铜板”或“粗铜板”);粗铜中含有的金、银以单质的形式在电解槽_______________(填“阳极”或“阴极”的槽底,阴极的电极反应式是_________________________________________。
(3)在精炼铜的过程中,电解质溶液中c(Fe2+)、c(Zn2+)会逐渐增大而影响进一步电解。
几种物质的溶度积常数(KSP):
| 物质 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
| KSP | 8.0×10-16 | 4.0×10-38 | 3.0×10-17 | 2.2×10-20 |
调节电解液的pH是除去杂质离子的常用方法。根据上表中溶度积数据判断,含有等物质的量浓度的Fe2+、Zn2+、Fe3+、Cu2+的溶液,随pH升高最先沉淀下来的离子是______________。
一种方案是先加入过量的H2O2,再调节pH到4左右。加入H2O2后发生反应的离子方程式为___________________________________________________________。
查看习题详情和答案>>1L0.1mol/L的![]() 溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极上增重2.16g时,下列判断正确的是
溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极上增重2.16g时,下列判断正确的是
[ ]
A.电解质溶液的浓度变为0.08mol/L
B.阳极上产生 112mL![]() (标准状况)
(标准状况)
C.转移电子数为12.04![]()
D.反应中有0.02mol的物质被氧化
查看习题详情和答案>>
 2Cu +SO2
2Cu +SO2 (1)烟气中的主要废气是___________,从提高资源利用率和减排考虑,其综合利用方式是__________。
(2)电解法精炼铜时,阳极是_____________(填“纯铜板” 或“粗铜板”);粗铜中含有的金、银以单质的形式沉积在电解槽__________(填“阳极”或“阴极”)的槽底,阴极的电极反应式是________。
(3)在精炼铜的过程中,电解质溶液中c(Fe2+ )、 c(Zn2+)会逐渐增大而影响进一步电解。 几种物质的溶度积常数(Ksp)

②一种方案是先加入过量的H2O2,再调节pH到4 左右,加入H2O2的目的是__________,加入 H2O2后发生反应的离子方程式为__________。
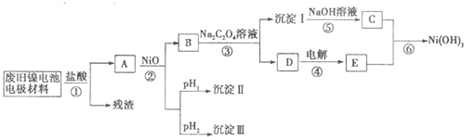
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+
②某温度下一些金属氢氧化物的Kap及沉淀析出的理论pH如下表所示:
| M(OH)n | Kap | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 1.9×10-23 | 3.43 | 4.19 |
| Fe(OH)3 | 3.8×10-38 | 2.53 | 2.94 |
| Ni(OH)2 | 1.6×10-14 | 7.60 | 9.75 |
(1)根据上表数据判断步骤②依次析出沉淀Ⅱ
A.pH试纸B.石蕊指示剂 C.pH计
(2)已知溶解度:NiC2O4>NiC2O4?H2O>NiC2O4?2H2O,则③的化学方程式是
(3)④中阳极反应产生的气体E为
(4)试写出⑥的离子方程式
 用惰性电极电解一定量的硫酸铜溶液,电解过程中的实验数据如图所示.横坐标表示转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).下列判断正确的是( )
用惰性电极电解一定量的硫酸铜溶液,电解过程中的实验数据如图所示.横坐标表示转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).下列判断正确的是( )