网址:http://m.1010jiajiao.com/timu_id_399727[举报]
(04年广东卷)海水的综合利用可以制备金属镁,其流程如下图所示:
|
(1)若在空气中加热MgCl2?6H2O,生成的是Mg(OH)Cl或MgO,写出相应反应的化学方程
式。
用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热MgCl2?6H2O时,能得到无水MgCl2,其原因是
。
(2)Mg(OH)2沉淀中混有的Ca(OH)2应怎样除去?写出实验步骤。
。
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到
玻璃棒,分别说明在这三种情况下使用玻璃棒的目的;
溶解时: 。
过滤时: 。
蒸发时: 。
查看习题详情和答案>>海水中镁的总储量约为2.1×1015 t,目前世界生产的镁60%来自海水.海水的综合利用可以制备金属镁,其流程如下图所示:

其步骤为:
①将海边大量存在的贝壳煅烧成生石灰,并将生石灰制成石灰乳;
②将石灰乳加入到经过蒸发浓缩并滤去粗盐后的海水中,过滤得到Mg(OH)2沉淀;
③向Mg(OH)2沉淀中加入盐酸得到MgCl2溶液,再经蒸发结晶得到MgCl2?6H2O;
④将MgCl2?6H2O在一定条件下加热得到无水MgCl2;
⑤电解熔融的MgCl2可得到Mg.
请回答下列问题:
(1)步骤①中煅烧贝壳时所发生反应的化学方程式为
(2)工业上采用电解MgCl2的方法制得金属镁,电解槽中阴极的电极反应式为
(3)步骤③中的蒸发是利用风吹日晒来完成的,而在实验室中进行蒸发操作需要的主要仪器有
(4)海水中的镁以Mg2+的形式存在,设计步骤②③将Mg2+转化为Mg(OH)2,然后又重新转化为Mg2+的目的是
(5)步骤④中的“一定条件”指的是
(6)在上述制取镁的流程中,所涉及到的基本反应类型有
a.化和反应b.分解反应c.置换反应d.复分解反应
(7)由海水得到的粗盐中常含有Ca2+、Mg2+、SO42-等杂质,为除去这些杂质可加入Na2CO3、NaOH和BaCl2,然后过滤,则所加入试剂的合理顺序为

(1)制取金属镁时,可以用电解MgCl2的方法,写出相应的反应的化学方程式
| ||
| ||
(2)电解无水氯化镁产物之一的Cl2可与氧气、甲烷起反应(产物为HCl、CO),再制得盐酸使用,写出该反应的化学方程式并标出电子转移的方向和数目.
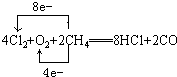
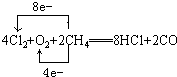
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:
溶解时:
过滤时:
蒸发时:

(1)上述流程中生成氢氧化镁沉淀的离子方程式为
(2)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明这三种情况下使用玻璃棒的作用:溶解时:
(1)某化学课外活动小组以海带为原料获得少量碘,其过程如下图所示:

则:操作①的名称是
(2)海水的综合利用可以制备金属钠和镁,其流程如图所示:

①上述流程中生成Mg(OH)2沉淀的离子方程式为
②实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明这三种情况下使用玻璃棒的作用:
溶解时:
③工业上把电解饱和食盐水称为“氯碱工业”.请你完成电解饱和食盐水的化学方程式
| ||
