摘要:8.铁的氢氧化物化学式 Fe(OH)2 Fe(OH)3 颜色 状态 溶解性 稳定性 与H+反应 转化关系 9.Fe2+和Fe3+的鉴别方法
网址:http://m.1010jiajiao.com/timu_id_399669[举报]
 已知Fe(OH)2是白色难溶于水的物质,很容易被空气中的氧气氧化为Fe(OH)3.如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时颜色的变化.实验时必须使用铁屑和6mol/L的硫酸,其它试剂自选.请填写下列空白:
已知Fe(OH)2是白色难溶于水的物质,很容易被空气中的氧气氧化为Fe(OH)3.如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时颜色的变化.实验时必须使用铁屑和6mol/L的硫酸,其它试剂自选.请填写下列空白:(1)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是
铁屑
铁屑
;(2)实验开始时应先将活塞E
打开
打开
(填“打开”或“关闭”),C中收集到的气体的主要成份是氢气
氢气
;(3)简述生成Fe(OH)2的操作过程
关闭活塞E,使FeSO4溶液被压入B瓶中进行反应
关闭活塞E,使FeSO4溶液被压入B瓶中进行反应
;(4)(3)操作后拔出装置B中的橡皮塞,使空气进入,写出有关反应的化学方程式
4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2+2H2O=4Fe(OH)3
.(12分)化学实验室通常用粗锌和稀硫酸反应制氢气,因此在制氢废液中含有大量的硫酸锌。同时,由于粗锌中还含有铁等杂质,使得溶液中混有一定量的硫酸亚铁,为了充分利用制氢废液,常用其制备皓矾(ZnSO4·7H2O)。某校化学兴趣小组的同学以制氢气的废液为原料来制取皓矾并探究其性质。 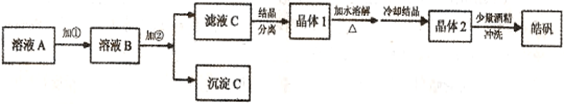 (l)制备皓矾的实验流程如下图所示。
(l)制备皓矾的实验流程如下图所示。
已知:下列氢氧化物开始生成沉淀到沉淀完全的pH范围分别为:
| | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Zn(OH)2 | 5.7 | 8.0 |
可供选择使用的有:氯水、20%的H2O2、氨水、NaOH溶液、Zn(OH)2、ZnO
① 加入的试剂①,应选用 ,作用: 。
② 加入的试剂②调节pH,可选用 或 ,用离子方程式表示其原理
。
③有同学提出,应将晶体1加入稀硫酸中溶解,原因是 。
④在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是 。
(2)检验皓矾中是否含有Fe元素的操作(试剂自选) 。 查看习题详情和答案>>
(12分)化学实验室通常用粗锌和稀硫酸反应制氢气,因此在制氢废液中含有大量的硫酸锌。同时,由于粗锌中还含有铁等杂质,使得溶液中混有一定量的硫酸亚铁,为了充分利用制氢废液,常用其制备皓矾(ZnSO4·7H2O)。某校化学兴趣小组的同学以制氢气的废液为原料来制取皓矾并探究其性质。
 (l)制备皓矾的实验流程如下图所示。
(l)制备皓矾的实验流程如下图所示。
已知:下列氢氧化物开始生成沉淀到沉淀完全的pH范围分别为:
回答下列问题:
可供选择使用的有:氯水、20%的H2O2、氨水、NaOH溶液、Zn(OH)2、ZnO
① 加入的试剂①,应选用 ,作用: 。
② 加入的试剂②调节pH,可选用 或 ,用离子方程式表示其原理
。
③有同学提出,应将晶体1加入稀硫酸中溶解,原因是 。
④在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是 。
(2)检验皓矾中是否含有Fe元素的操作(试剂自选) 。
 (l)制备皓矾的实验流程如下图所示。
(l)制备皓矾的实验流程如下图所示。已知:下列氢氧化物开始生成沉淀到沉淀完全的pH范围分别为:
| | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Zn(OH)2 | 5.7 | 8.0 |
可供选择使用的有:氯水、20%的H2O2、氨水、NaOH溶液、Zn(OH)2、ZnO
① 加入的试剂①,应选用 ,作用: 。
② 加入的试剂②调节pH,可选用 或 ,用离子方程式表示其原理
。
③有同学提出,应将晶体1加入稀硫酸中溶解,原因是 。
④在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是 。
(2)检验皓矾中是否含有Fe元素的操作(试剂自选) 。
(1)用NaCl固体配制100mL 1.00mol/L NaCl溶液的步骤为:计算;称量;溶解;洗涤;摇匀;装瓶贴签等.其中缺少的步骤名称有
(2)国际上规定,
(3)在水溶液里或
(4)酸、碱、盐在水溶液中发生的离子反应的条件是生成
(5)在化学反应中,如果反应前后元素化合价发生变化,就一定有
(6)离子反应特有的守恒关系为
(7)将
查看习题详情和答案>>
移液、定容
移液、定容
.(2)国际上规定,
0.012kg12C所含碳原子数
0.012kg12C所含碳原子数
叫做阿伏加德罗常数.(3)在水溶液里或
熔融状态
熔融状态
下能够导电的化合物
化合物
叫做电解质.(4)酸、碱、盐在水溶液中发生的离子反应的条件是生成
沉淀、气体或弱电解质
沉淀、气体或弱电解质
,只要具备上述条件之一,反应就能发生.(5)在化学反应中,如果反应前后元素化合价发生变化,就一定有
电子转移
电子转移
;元素化合价升高,该物质发生氧化还原
氧化还原
反应.(6)离子反应特有的守恒关系为
电荷
电荷
守恒;氧化还原反应特有的守恒关系为电子转移
电子转移
守恒.(7)将
饱和氯化铁溶液
饱和氯化铁溶液
滴入沸水
沸水
中可制备氢氧化铁胶体,反应的化学方程式为FeCl3+3H2O=Fe(OH)3(胶体)+3HCl
FeCl3+3H2O=Fe(OH)3(胶体)+3HCl
.(1)写出下列物质在水溶液中的电离方程式:氢氧化钡
(2)写出下列反应的离子方程式:硫酸钠和硝酸钡
(3)实验室制备氢氧化铁胶体的方法是:向沸水中逐滴加入5-6滴饱和的三氯化铁溶液,
查看习题详情和答案>>
Ba(OH)2=Ba2++2OH-
Ba(OH)2=Ba2++2OH-
;硫酸铁Fe2(SO4)3=2Fe3++3SO42-
Fe2(SO4)3=2Fe3++3SO42-
(2)写出下列反应的离子方程式:硫酸钠和硝酸钡
SO42-+Ba2+=BaSO4↓
SO42-+Ba2+=BaSO4↓
;碳酸钠与足量的盐酸CO32-+2H+=H2O+CO2↑
CO32-+2H+=H2O+CO2↑
(3)实验室制备氢氧化铁胶体的方法是:向沸水中逐滴加入5-6滴饱和的三氯化铁溶液,
呈现红褐色
呈现红褐色
,停止加热.(请补充完整)反应的化学方程式为FeCl3+3H2O
Fe(OH)3(胶体)+3HCl
| ||
FeCl3+3H2O
Fe(OH)3(胶体)+3HCl
.
| ||