摘要:离子键:(1)概念: .(2)形成过程(以MgCl2为例): .(3)影响离子键强弱的因素: .(4)离子键的强弱对物质性质的影响: .
网址:http://m.1010jiajiao.com/timu_id_398874[举报]
有下列八种晶体:①金刚石 ②汞 ③氯化钾 ④二氧化硅 ⑤晶体碘 ⑥溴化钠 ⑦镁 ⑧二氧化碳.(填序号,下同)
其中属于金属晶体的是 ,属于原子晶体的是 ,
属于离子晶体的是 ,属于分子晶体的是 .
下列物质在所述变化过程中克服的是:①分子间作用力 ②共价键 ③离子键.
(1)冰融化 ,
(2)液溴挥发 ,
(3)食盐熔化 ,
(4)电解熔融MgCl2制Mg ,
(5)H2S受热分解成S和H2 .
查看习题详情和答案>>
其中属于金属晶体的是
属于离子晶体的是
下列物质在所述变化过程中克服的是:①分子间作用力 ②共价键 ③离子键.
(1)冰融化
(2)液溴挥发
(3)食盐熔化
(4)电解熔融MgCl2制Mg
(5)H2S受热分解成S和H2
已知元素电负性的差值大于1.7时,原子间形成离子键,小于1.7时,原子间形成共价键,请指出下列原子之间形成的化学键是离子键还是共价键.
Be(1.5)和F(4.0):
查看习题详情和答案>>
Be(1.5)和F(4.0):
离子键
离子键
,Si(1.8)和Cl(3.0):共价键
共价键
.(2012?梧州模拟)有A、B、C、D、E、F、G、H、I九种常见物质,它们的转化关系(反应条件未注明)如图所示.其中B、C、D为单质,常温下D为固态,B、C、E、G为气态,F为淡黄色粉末,I的焰色反应为黄色.
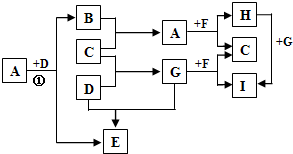
请回答:
(1)写出F的电子式
 ,其化学键类型有
,其化学键类型有
(2)I的溶液呈
(3)反应①的产物通常作为城镇居民的燃气,也可用于冶金工业.请展示它们在冶金工业上的一个应用(用化学反应方程式表示)
(4)在标准状况下,若将11.2L气体G通入350mL 2mol/L的H溶液中,反应后溶液中离子浓度由大到小的顺序依次是
查看习题详情和答案>>

请回答:
(1)写出F的电子式


离子键和(非极性)共价键
离子键和(非极性)共价键
;(2)I的溶液呈
碱
碱
性(填酸性、中性或碱性),原因用离子反应方程式表示为:CO32-+H2O?HCO3-+OH-
CO32-+H2O?HCO3-+OH-
;(3)反应①的产物通常作为城镇居民的燃气,也可用于冶金工业.请展示它们在冶金工业上的一个应用(用化学反应方程式表示)
3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
.
| ||
(4)在标准状况下,若将11.2L气体G通入350mL 2mol/L的H溶液中,反应后溶液中离子浓度由大到小的顺序依次是
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
.下表是某些短周期元素的电负性(x)值:
(1)根据表中数据归纳元素的电负性与原子吸引电子的能力的关系
(2)试推测,周期表所列元素中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物的电子式为
 .
.
(3)已知:Cl-Br+H-OH H-Cl+HO-Br.
H-Cl+HO-Br.
①若NCl3最初水解产物是NH3和HOCl,则x(Cl)的最小范围:
②PCl3水解的化学反应方程式是
(4)一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键,小于1.7通常形成共价键,结合问题(3)-①,分析BeCl2属于
请设计实验加以证明
查看习题详情和答案>>
| 元素符号 | Li | Be | N | O | F | Na | Mg | Al | P | S |
| X值 | 0.98 | 1.57 | 3.04 | 3.44 | 3.98 | 0.93 | 1.31 | 1.61 | 2.19 | 2.58 |
元素的电负性越大,原子吸引电子的能力越强
元素的电负性越大,原子吸引电子的能力越强
.(2)试推测,周期表所列元素中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物的电子式为


(3)已知:Cl-Br+H-OH
 H-Cl+HO-Br.
H-Cl+HO-Br.①若NCl3最初水解产物是NH3和HOCl,则x(Cl)的最小范围:
2.58~3.04
2.58~3.04
(填表中数值);②PCl3水解的化学反应方程式是
PCl3+3H2O=3HCl+H3PO3(或P(OH)3)
PCl3+3H2O=3HCl+H3PO3(或P(OH)3)
.(4)一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键,小于1.7通常形成共价键,结合问题(3)-①,分析BeCl2属于
共价化合物
共价化合物
.(填离子化合物或共价化合物)请设计实验加以证明
测定熔融态的BeCl2不导电
测定熔融态的BeCl2不导电
.