网址:http://m.1010jiajiao.com/timu_id_398727[举报]
 归纳整理是科学学习的重要方法之一.在学习了氧族元素的各种性质后,可归纳整理出如下表所示的表格(部分).
归纳整理是科学学习的重要方法之一.在学习了氧族元素的各种性质后,可归纳整理出如下表所示的表格(部分).| 性质\元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 217 | 450 |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
(1)碲的化合价可能有
(2)氢硒酸有较强的
(3)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
(4)已知在常温下,H2和S反应生成17g H2S放出56.1KJ的热量,试写出硫化氢分解的热化学方程式:
(5)右图所示为上述表格中氧族元素单质与H2反应过程中的能量变化示意图,其中a、b、c、d分别表示氧族中某一元素的单质,△H为相同物质的量的单质与H2反应的反应热.则:b代表
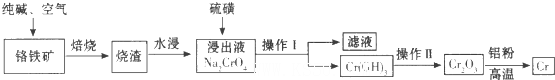
(l)实验室焙烧铬铁矿可选用的装置是
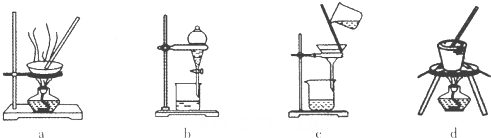
(2)完成下列化学方程式(在横线上填写物质的化学式及计量数):
4CrO42-+6S+7H2O=4Cr(OH)3↓+3S2O32-+
(3)操作I包括过滤与洗涤,简述实验室中洗涤沉淀的操作:
(4)Cr(0H)3和Al(OH)3类似,也是两性氢氧化物,写出Cr(OH)3溶于浓氢氧化钠溶液的离子方程式
(5)由Cr2O3冶炼Cr的化学方程式为
(6)目前有一种采用以铬酸钠(Na2CrO4)为原料,用电化学法制备重铬酸钠(Na2Cr2O7)的实验装置如下图所示(已知:2CrO42-+2H+?Cr2O72-+H2O).
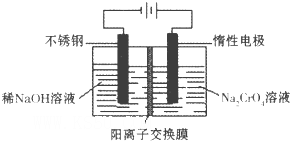
①出阴极的电极反应式为
②电解一段时间后,测得阳极区溶液中Na+物质的量由a mol变为b mol,则此时铬酸钠的转化率为
(8分)类推法是科学学习的重要方法之一。在学习了卤族元素的各种性质后,如下表所示,表格提供的是氧族元素的部分性质。请结合元素周期律完成下列问题:
| 元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | | 450 |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
(2)碲的化合价可能有 。
(3)氢硒酸有较强的还原性。因此放在空气中长期保存易变质,其可能发生的化学方程式为:
。
(4)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
Al2Te3+ →Al(OH)3↓+ H2Te↑ 查看习题详情和答案>>
元素 | O | S | Se | Te |
单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
(1)氧族元素形成的氢化物的稳定性由强到弱的顺序是___________________________。
(2)工业上Al2Te3可用来制备H2Te,完成下列化学方程式并配平:
( )Al2Te3+( )____________====( )Al(OH)3↓+( )H2Te↑
(3)在101 kPa时,
(8分)类推法是科学学习的重要方法之一。在学习了卤族元素的各种性质后,如下表所示,表格提供的是氧族元素的部分性质。请结合元素周期律完成下列问题:
|
元素 |
8O |
16S |
34Se |
52Te |
|
单质熔点(℃) |
-218.4 |
113 |
|
450 |
|
单质沸点(℃) |
-183 |
444.6 |
685 |
1390 |
|
主要化合价 |
-2 |
-2,+4,+6 |
-2,+4,+6 |
|
|
原子半径 |
逐渐增大 |
|||
|
单质与H2反应情况 |
点燃时易化合 |
加热化合 |
加热难化合 |
不能直接化合 |
(1)硒的熔点范围可能是 。
(2)碲的化合价可能有 。
(3)氢硒酸有较强的还原性。因此放在空气中长期保存易变质,其可能发生的化学方程式为:
。
(4)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
Al2Te3+ →Al(OH)3↓+ H2Te↑
查看习题详情和答案>>