网址:http://m.1010jiajiao.com/timu_id_3971662[举报]
(17分)金属镍具有优良的物理和化学特性,是高技术产业的重要原料。
(1)羰基法提纯镍涉及的反应为:Ni(s)+4CO(g) Ni(CO)4(g)
Ni(CO)4(g)
①当温度升高时,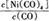 减小,则?H 0(填“>”或“<”)。
减小,则?H 0(填“>”或“<”)。
②一定温度下,将一定量的粗镍和CO加入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________(填代号)。
若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数 (填“增大”、“不变”或“减小”),反应进行3s后测得Ni(CO)4的物质的量为0.6mol,则0—3s内的平均反应速率v(CO)=____mol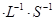 。
。
③要提高上述反应中CO的转化率,同时增大反应速率,可采取的措施为____________________(写出一条措施即可)。
(2)以NiS04溶液为电解质溶液进行粗镍(含Fe、Zn、Cu、Pt、Au等杂质)的电解精炼,下列说法正确的是____________(填代号)。(已知氧化性: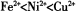 )
)
a.电解过程中,化学能转化为电能
b.粗镍作阳极,发生还原反应
c.利用阳极泥可回收Cu、Pt、Au等金属
d.粗镍精炼时通过的电量与阴极析出镍的质量成正比
(3)工业上用硫化镍(NiS)作为电极材料冶炼镍。电解时,硫化镍中的硫元素以单质形态沉积在某电极附近,镍元素以Ni2+形态进入电解液中,如图所示。硫化镍与电源的____________(填“正极”或“负极”)相接。写出阳极的电极反应式________________。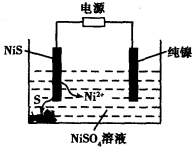
①准确称取2.3g样品,加入足量的浓硝酸充分溶解后过滤,得到滤液B.
②在B中通入过量的氨气,结果溶液呈深蓝色,同时得到1.07g红褐色沉淀.
③在②的滤液中加入足量盐酸,未见沉淀产生,再滴入足量氯化钡溶液,最后得到4.66g白色沉淀.
已知:Cu2O+2H+=Cu2++Cu+H2O,请回答下列问题:
(1)写出氨气的电子式:
(2)工业上常利用该矿物与氧气反应熔炼金属Cu,同时也得到气体C和炉渣(主要成分为Fe2O3).
①在新制的C水溶液中滴加一定量的BaCl2溶液,初始观察不到明显现象,充分振荡后,可观察到有白色沉淀产生,且逐渐增多,请解释其原因
②冶炼过程中的最后一步是氧化亚铜与硫化亚铜在高温下作用得到金属铜和气体C,写出该步骤发生反应的化学方程式
③炉渣中的氧化铁可用来制备高铁酸钾(K2FeO4).K2FeO4是一种集氧化、吸附、絮凝、杀菌、脱嗅于一体,具有绿色、环保、高效等特点的新型水处理剂.研究发现K2FeO4的氧化性比KMnO4、O3还要强,在中性、酸性溶液中稳定性较差,在碱性溶液中稳定性较好.请写出K2FeO4在强酸性溶液中释放出氧气的离子方程式
自然界中的硫
认识硫单质
(1)硫的物理性质
硫俗称________,它是一种________色或________色固体,很脆,易研成粉末,________溶于水,________溶于酒精,________溶于CS2;熔点和沸点________.
(2)硫的同素异形体
硫的同素异形体有多种,稳定存在的是斜方硫(S8)和单斜硫(S8).
(3)硫的化学性质
①硫与金属的反应
Fe+S![]()
![]() (Fe有+2、+3价)
(Fe有+2、+3价)
2Cu+S![]()
![]() (Cu有+1、+2价)
(Cu有+1、+2价)
Hg+S![]()
![]() (Hg有+1、+2价)
(Hg有+1、+2价)
②硫与非金属的反应
![]() +O2
+O2![]()
![]() (S是还原剂)
(S是还原剂)
H2+![]()
![]()
![]() (S是氧化剂)
(S是氧化剂)
C+![]()
![]()
![]() (S是氧化剂)
(S是氧化剂)
③黑火药爆炸
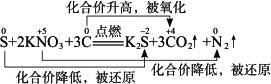
(4)硫的主要用途:制造硫酸、化肥、火柴、杀虫剂、火药、烟花爆竹、医药、硫化橡胶,硫还是酸性速效肥料,等等.
(1)W位于元素周期表第
W的气态氢化物稳定性比H2O(g)
(2)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
| ||
| ||
(3)Fe(s)+
| 1 |
| 2 |
2X(s)+
| 3 |
| 2 |
X的单质和FeO反应的热化学方程式是
| 1 |
| 4 |
| 1 |
| 2 |
| 1 |
| 4 |
| 1 |
| 2 |
(Ⅱ)已知X、Y和Z三种元素的原子序数之和等于42.X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子.X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子.请回答下列问题:
(1)X元素原子基态时的电子排布式为
(2)Y元素原子的价层电子的轨道表示式为
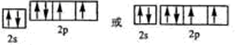
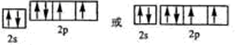
(3)X与Z可形成化合物XZ3,该化合物的空间构型为
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是

(1)写出A的化学式为
(2)I与F作用的离子方程式是
(3)G加入L后产生的白色沉淀到生成红褐色沉淀H的化学方程式:
(4)用两个最直接的离子方程式来证明Fe3+、Cu2+、Fe2+的氧化性强弱顺序是Fe3+>Cu2+>Fe2+
①