摘要:①用物质A表示的反应的平均速率为0.3mol?L-1?S-1,②用物质B表示的反应的平均速率为0.6mol?L-1?S-1,③2s时物质A的转化率为70%;④2s时物质B的浓度为0.7mol?L-1.其中正确的是 A.①③ B.①④ C.②③ D.③④
网址:http://m.1010jiajiao.com/timu_id_383268[举报]
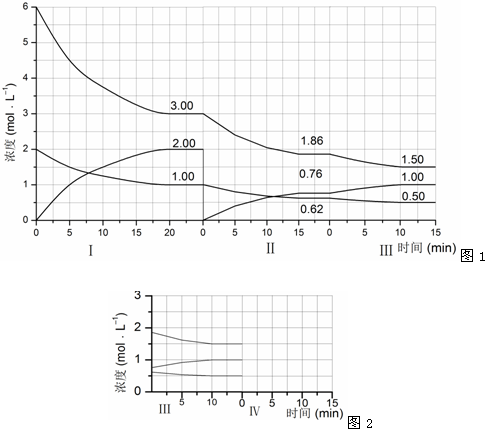
反应aA(g)+bB(g)
cC(g)(△H<0)在等容条件下进行.改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图1所示:回答问题:
(1)反应的化学方程式中,a:b:c为
(2)A的平均反应速率VⅠ(A)、VⅡ(A)、VⅢ(A)从大到小排列次序为
(3)B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是
(4)由第一次平衡到第二次平衡,平衡移动的方向是
(5)比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低:T2
(6)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图2中用曲线表示第IV阶段体系中各物质的浓度随时间变化的趋势如图2(曲线上必须标出A、B、C).
查看习题详情和答案>>
| 催化剂 |
(1)反应的化学方程式中,a:b:c为
1:3:2
1:3:2
;(2)A的平均反应速率VⅠ(A)、VⅡ(A)、VⅢ(A)从大到小排列次序为
vⅠ(A)>vⅡ(A)>vⅢ(A)
vⅠ(A)>vⅡ(A)>vⅢ(A)
;(3)B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是
αⅢ(B)
αⅢ(B)
,其值是19.4%
19.4%
;(4)由第一次平衡到第二次平衡,平衡移动的方向是
向正反应方向
向正反应方向
,采取的措施是从反应体系中移出产物C
从反应体系中移出产物C
;(5)比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低:T2
>
>
T3(填“>”“<”“=”),判断的理由是此反应为放热反应,降低温度,平衡向正反应方向移动,平衡的移动只能减弱改变,不能抵消改变
此反应为放热反应,降低温度,平衡向正反应方向移动,平衡的移动只能减弱改变,不能抵消改变
;(6)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图2中用曲线表示第IV阶段体系中各物质的浓度随时间变化的趋势如图2(曲线上必须标出A、B、C).

 物质(t-BuNO)2在正庚烷或CCl4中均可以发生反应:(t-BuNO)2?2(t-BuNO).在20℃时,向1L正庚烷中加入(t-BuNO)20.50mol,10min时反应达平衡,此时(t-BuNO)2的平衡转化率为65%(假设反应过程中溶液体积始终为1L).下列说法正确的是( )
物质(t-BuNO)2在正庚烷或CCl4中均可以发生反应:(t-BuNO)2?2(t-BuNO).在20℃时,向1L正庚烷中加入(t-BuNO)20.50mol,10min时反应达平衡,此时(t-BuNO)2的平衡转化率为65%(假设反应过程中溶液体积始终为1L).下列说法正确的是( )
查看习题详情和答案>>
反应![]() (△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
(△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
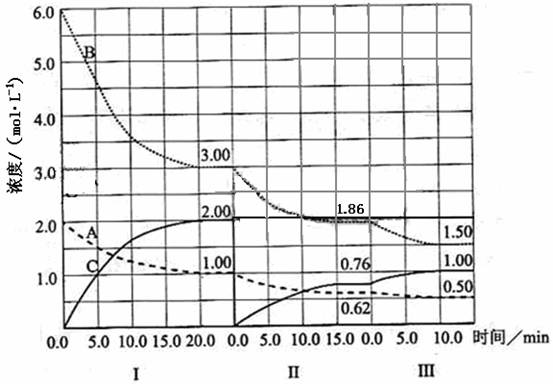 回答问题:
回答问题:
⑴反应的化学方程中a∶b∶c为 ;
 ⑵A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从大到小排列次序为 ;
⑵A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从大到小排列次序为 ;
⑶B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是 ,其值是 ;
⑷由第一次平衡到第二次平衡,平衡移动的方向是 ,采取的措施是 ;
⑸比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低;T2 T3(填“<”“>”“=”)判断的理由是 。
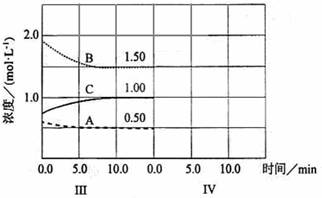
⑹达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图中用曲线表示第Ⅳ阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C)。
查看习题详情和答案>>