摘要:2.强酸弱碱盐的水解 [思考与交流]应用盐类水解的原理.分析NH4Cl溶液显酸性的原因.并写出有关的离子方程式. 归纳: (1)这种在溶液中盐电离出来的离子跟水所电离出来的H+或OH-结合生成弱电解质的反应.叫做盐类的水解. (2)只有弱酸的阴离子或弱碱的阳离子才能与H+或OH-结合生成弱电解质. (3)盐类水解使水的电离平衡发生了移动.并使溶液显酸性或碱性. 讨论: (4)盐类水解反应是酸碱中和反应的逆反应.水解的规律是:有弱才水解.无弱不水解.越弱越水解.都弱双水解.谁强显谁性.同强显中性.
网址:http://m.1010jiajiao.com/timu_id_3830289[举报]
(1)相同温度下,等浓度的CH3COONa和Na2CO3溶液,
(2)升高温度,使盐类的水解平衡向
(3)盐溶液的浓度越小,盐就越
(4)向CH3COONa溶液中加入NaOH溶液,则平衡向
(5)向NH4Cl溶液中加入CH3COONH4晶体,水解平衡向
查看习题详情和答案>>
Na2CO3
Na2CO3
溶液的碱性强.(2)升高温度,使盐类的水解平衡向
正反应方向
正反应方向
移动,即升高温度促进
促进
盐类的水解(填“促进”或“抑制”).(3)盐溶液的浓度越小,盐就越
容易
容易
水解,即加水促进
促进
盐类的水解(填“促进”或“抑制”).(4)向CH3COONa溶液中加入NaOH溶液,则平衡向
逆反应方向
逆反应方向
移动,即加酸能抑制
抑制
强酸弱碱盐的水解,加碱能抑制
抑制
强碱弱酸盐的水解(填“促进”或“抑制”).(5)向NH4Cl溶液中加入CH3COONH4晶体,水解平衡向
逆反应方向
逆反应方向
移动.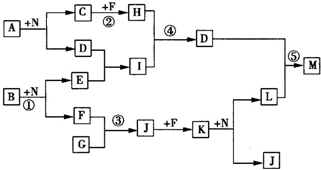 如右框图反应中所涉及的l4种物质都是由短周期元素组成的.已知:
如右框图反应中所涉及的l4种物质都是由短周期元素组成的.已知:(Ⅰ)F为单质;
(Ⅱ)A、B、C、G、H、J、K、N均是由两种元素组成的化合物,且C、G为同周期元素形成的简单气态氢化物;
(Ⅲ)D、E、I、L、M均是由3种元素组成的化合物,且D具有两性;
(Ⅳ)反应中生成的水均已略去.
请回答下列问题:
(1)写出化学式:B
Na2O2
Na2O2
,INaAlO2
NaAlO2
.(2)写出E的电子式:
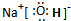
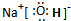
(3)反应③的化学方程式为
4NH3+5O2
6H2O+4NO
| ||
| △ |
4NH3+5O2
6H2O+4NO
.
| ||
| △ |
(4)解释反应⑤中生成的M的水溶液呈酸性的原因:
硝酸铝是强酸弱碱盐,铝离子水解而使其水溶液呈酸性,Al3++3H2O?Al(OH)3+3H+
硝酸铝是强酸弱碱盐,铝离子水解而使其水溶液呈酸性,Al3++3H2O?Al(OH)3+3H+
(请用化学方程式及必要的文字说明).(5)反应②中,每1.00g C与足量的F作用,恢复到25℃时放出55.6kJ的热量,写出反应②的热化学方程式:
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-889.6KJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-889.6KJ/mol
;反应②在KOH作介质的环境中可形成一个原电池,则该原电池的负极反应式为CH4-8e-+10OH-=CO32-+7H2O
CH4-8e-+10OH-=CO32-+7H2O
.