摘要:3.用黄铁矿可以制取 H2SO4.再用 H2SO4 可以制取化肥(NH4)2SO4.煅烧含 FeS2 80.2% 的黄铁矿 75.0 t.最终生产出 79.2 t(NH4)2SO4.已知 NH3 的利用率为 92.6%.H2SO4 的利用率为 89.8%.试求黄铁矿制取 H2SO4 时的损失率.
网址:http://m.1010jiajiao.com/timu_id_3812413[举报]
用黄铁矿可以制取 H2SO4,再用 H2SO4可以制取化肥(NH4)2SO4。煅烧含 FeS2 80.2%的黄铁矿 75.0 t,最终生产出 79.2 t(NH4)2SO4。已知 NH3的利用率为 92.6%,H2SO4的利用率为 89.8%,试求黄铁矿制取 H2SO4时的损失率。
查看习题详情和答案>>
用黄铁矿可以制取 H2SO4,再用 H2SO4 可以制取化肥(NH4)2SO4。煅烧含 FeS2 80.2% 的黄铁矿 75.0 t,最终生产出 79.2 t(NH4)2SO4。已知 NH3 的利用率为 92.6%,H2SO4 的利用率为 89.8%,试求黄铁矿制取 H2SO4 时的损失率。
查看习题详情和答案>>硫酸在国民经济中占有极其重要的地位,我国常以黄铁矿(主要成分FeS2)为原料生产硫酸。
| 成分 | 催化氧化前 | 催化氧化后 |
| O2 | 11% | 未测定 |
| SO2 | 7% | 未测定 |
| N2 | 82% | 84.8% |
| SO3 | —— | 6.9% |
⑴SO2的催化氧化是硫酸工业的主要反应。现有标准状态下5.6 L SO2气体,在500℃、V2O5催化下转化成SO3,若SO2转化率为a%,放出热量为QkJ。该反应的热化学方程式为 ▲ 。
⑵已知在SO2催化氧化前后混合气体中各成分的体积分数如表,
则SO2的转化率为 ▲ 。
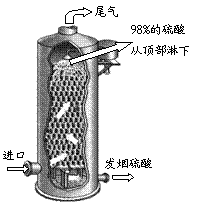 ⑶如右图所示,用98%的浓硫酸1.0t吸收SO3制得发烟硫酸(化学组成可表示为H2SO4·xSO3),可生产SO3质量分数为20%的发烟硫酸 ▲ t。
⑶如右图所示,用98%的浓硫酸1.0t吸收SO3制得发烟硫酸(化学组成可表示为H2SO4·xSO3),可生产SO3质量分数为20%的发烟硫酸 ▲ t。
⑷某硫酸厂在进行黄铁矿成分测定时,取0.1000 g样品充分灼烧,生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,再用0.02000 mol·L-1的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00mL。
已知:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
则样品中FeS2的质量分数是多少?(假设杂质不参加反应)
查看习题详情和答案>>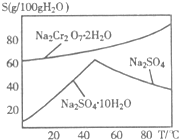 重铬酸钠(Na2Cr2O7)主要用于印染、制革、医药、电镀等.工业上以铬铁矿(主要成分FeO?Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7?2H2O)的主要反应如下:
重铬酸钠(Na2Cr2O7)主要用于印染、制革、医药、电镀等.工业上以铬铁矿(主要成分FeO?Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7?2H2O)的主要反应如下:①4FeO?Cr2O3+8Na2CO3+7O2
| ||
. |
②2Na2CrO4+H2SO4═Na2SO4+Na2Cr2O7+H2O
(1)反应①是在回转窑中进行,反应时需不断搅拌,其目的是
使反应物充分接触,加快反应速率
使反应物充分接触,加快反应速率
.(2)右图是红矾钠(Na2Cr2O7?2H2O)和Na2SO4的溶解度曲线.从Na2Cr2O7和Na2SO4的混合溶液中提取Na2Cr2O7晶体的操作:先将混合溶液蒸发浓缩,趁热过滤.趁热过滤的目的是
有利于硫酸钠结晶析出,可以防止Na2Cr2O7?2H2O结晶析出
有利于硫酸钠结晶析出,可以防止Na2Cr2O7?2H2O结晶析出
;然后将滤液冷却结晶
冷却结晶
,从而析出红矾钠.(3)Na2Cr2O7与KCl或K2SO4进行复分解反应可制取K2Cr2O7,现用Na2Cr2O7与KCl来制备K2Cr2O7,简述操作步骤(有关物质的溶解度见右表):
较高温度下将Na2Cr2O7与KCl配成饱和溶液后混合,再降低温度到0℃冷却结晶,过滤洗涤,可得K2Cr2O7
较高温度下将Na2Cr2O7与KCl配成饱和溶液后混合,再降低温度到0℃冷却结晶,过滤洗涤,可得K2Cr2O7
.
| 温度 | 0℃ | 100℃ |
| 溶解度 | ||
| 物质 | ||
| K2Cr2O7 | 4.6g | 94.1g |
| KCl | 28g | 55g |
| NaCl | 35g | 39g |
步骤1:将mg铁矿石加浓盐酸加热溶解
步骤2:加入SnCl2溶液将Fe3+还原至黄色消失
步骤3:将所得溶液冷却,加入HgC2溶液,将过量的Sn2+氧化为Sn4+
步骤4:加入15mL硫酸和磷酸的混合酸及5滴O.2%二苯胺磺酸钠指示剂
步骤5:立即用cmol?L.重铬酸钾溶液滴定至溶液呈稳定紫色,即为终点,消耗重铬酸钾溶液VmL
①写出SnCl2还原Fe3+的离子方程式
2Fe3++Sn2+=Sn4++2Fe2+
2Fe3++Sn2+=Sn4++2Fe2+
.②如省去步骤③,则所测定的铁的含量
偏高
偏高
(填“偏高”、“偏低”或“无影响”).③步骤5使用的玻璃仪器有
酸式滴定管、锥形瓶
酸式滴定管、锥形瓶
. (2011?泰州二模)硫酸在国民经济中占有极其重要的地位,我国常以黄铁矿(主要成分FeS2)为原料生产硫酸.
(2011?泰州二模)硫酸在国民经济中占有极其重要的地位,我国常以黄铁矿(主要成分FeS2)为原料生产硫酸.| 成分 | 催化氧化前 | 催化氧化后 |
| O2 | 11% | 未测定 |
| SO2 | 7% | 未测定 |
| N2 | 82% | 84.8% |
| SO3 | -- | 6.9% |
2SO2(g)+O2(g)?2SO3(g)△H=-
kJ/mol
| 800Q |
| a |
2SO2(g)+O2(g)?2SO3(g)△H=-
kJ/mol
.| 800Q |
| a |
(2)已知在SO2催化氧化前后混合气体中各成分的体积分数如表,则SO2的转化率为
95.3%
95.3%
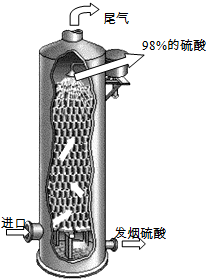
.(3)如图所示,用98%的浓硫酸1.0t吸收SO3制得发烟硫酸(化学组成可表示为H2SO4?xSO3),可生产SO3质量分数为20%的发烟硫酸
1.36
1.36
t.(4)某硫酸厂在进行黄铁矿成分测定时,取0.1000g样品充分灼烧,生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,再用0.02000mol?L-1的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00mL.
已知:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
则样品中FeS2的质量分数是多少?(假设杂质不参加反应).