网址:http://m.1010jiajiao.com/timu_id_3808812[举报]
(1)基态Ni原子的价电子(外围电子)排布式为
(2)金属镍能与CO形成配合物Ni(CO)4,写出与CO互为等电子体的一种分子和一种离子的化学式
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应.如①CH2=CH2、②HC≡CH、③
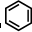 、④HCHO其中碳原子采取sp2杂化的分子有
、④HCHO其中碳原子采取sp2杂化的分子有(4)Ni2+和Fe2+的半径分别为69pm和78pm,则熔点NiO
(5)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如图1所示.该合金的化学式为
(6)丁二酮肟常用于检验Ni2+:在稀氨水中,丁二酮肟与Ni2+反应生成鲜红色沉淀,其结构如图2所示.该结构中,除共价键外还存在配位键和氢键,请在图中用箭头和“…”表示出配位键和氢键.

金属镍及其化合物在合金材料以及催化剂等方面应用广泛。
(1)基态Ni原子的价电子(外围电子)排布式为 _ 。
(2)金属镍能与CO形成配合物Ni(CO)4,写出与CO互为等电子体的一种分子和一种离子的化学式 _ 。
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应。
如①CH2=CH2、②HC≡CH、③![]()
![]() 、④HCHO其中碳原子采取sp2杂化的分子有
、④HCHO其中碳原子采取sp2杂化的分子有
_ (填物质序号),HCHO分子的立体结构为 _ 形。
(4)Ni2+和Fe2+的半径分别为69 pm和78 pm,则熔点NiO _ FeO
(填“<”或“>”)。
(5)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为 _ 。
(6)丁二酮肟常用于检验Ni2+:在稀氨水中,丁二酮肟与Ni2+反应生成鲜红色沉淀,其结构如右上图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用箭头和“…”表示出配位键和氢键。
 | |||
 | |||
|
查看习题详情和答案>>
金属镍及其化合物在合金材料以及催化剂等方面应用广泛.
(1)基态Ni原子的价电子(外围电子)排布式为________.
(2)金属镍能与CO形成配合物Ni(CO)4,写出与CO互为等电子体的一种分子和一种离子的化学式________.
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应.
如①CH2=CH2、②HC≡CH、③![]() 、④HCHO其中碳原子采取sp2杂化的分子有________(填物质序号),HCHO分子的立体结构为________形.
、④HCHO其中碳原子采取sp2杂化的分子有________(填物质序号),HCHO分子的立体结构为________形.
(4)Ni2+和Fe2+的半径分别为69 pm和78 pm,则熔点NiO________FeO(填“<”或“>”).
(5)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如下图所示.该合金的化学式为________.

(6)丁二酮肟常用于检验Ni2+:在稀氨水中,丁二酮肟与Ni2+反应生成鲜红色沉淀,其结构如下图所示.该结构中,除共价键外还存在配位键和氢键,请在图中用箭头和“…”表示出配位键和氢键.

(2)二氧化钛可作光催化剂,能将居室污染物甲醛、苯、二甲苯等有害物质转化为二氧化碳和水,达到无害化。下列有关甲醛、苯、二甲苯、二氧化碳及水的说法正确的是__。
A.苯与B3N3H6互为等电子体,分子中所有原子共平面,且都有三种二氯代物
B.二氧化碳、甲醛、氯仿( CHCl3)中的碳原子分别采取sp.sp2和sp3杂化
C.对二甲苯是非极性分子,邻二甲苯和间二甲苯都是极性分子
D.氨比甲醛易溶于水,是因为甲醛与水分子间不能形成氢键
(3)日常生活中广泛使用的不锈钢就是含铬的合金,铬原子中未成对电子数为___。
(4)①短周期的某主族元素M的逐级电离能情况如下图A所示,则M元素在形成化合物时,表现的主要化合价为___ 价。
②第三周期八种元素的单质熔点高低的情况如下图B所示,其中序号“8”代表___(填元素符号),其中电负性最大的是____(填图B中的序号)。


I、金属镍及其化合物在合金材料以及催化剂等方面应用广泛。
(1)基态Ni原子的价电子(外围电子)排布式为 ;
(2)金属镍能与CO形成配合物Ni(CO)4,写出与CO互为等电子体的一种分子和一种离子的化学式 、 ;
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应。
如①CH2=CH2、②HC≡CH、③
 、④HCHO其中碳原子采取sp2杂化的分子有
、④HCHO其中碳原子采取sp2杂化的分子有
(填物质序号),HCHO分子的立体结构为 形;
(4)Ni2+和Fe2+的半径分别为69 pm和78 pm,则熔点NiO FeO
(填“<”或“>”);
(5)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为 ;
(6)丁二酮肟常用于检验Ni2+:在稀氨水中,丁二酮肟与Ni2+反应生成鲜红色沉淀,其结构如右下图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用箭头和“…”表示出配位键和氢键。


查看习题详情和答案>>
