网址:http://m.1010jiajiao.com/timu_id_3803632[举报]
①在中性或弱酸性介质中先用过量的Br2,将试样中的I-氧化成![]() ;
;
②煮沸①所得溶液以除去过量的Br2,然后在酸性条件下加入过量的KI溶液,将![]() 还原为I2;
还原为I2;
③在②中加淀粉作指示剂,用Na2S2O3标准溶液滴定(2Na2S2O3+I2====2NaI+Na2S4O6)。
通过上述步骤可测得碘化物中I-的含量:
(1)写出步骤①②中发生反应的离子方程式:
①__________________________________________,
②__________________________________________。
(2)若样品中有1 mol I-,则最后耗用Na2S2O3的物质的量是多少?
(3)若在测定时,准确量取含KI的样品溶液25.00 mL,终点时耗用0.050 mol·L-1 Na2S2O3溶液20.06 mL,试计算样品溶液中KI的含量(g·L-1)。
查看习题详情和答案>>少量的碘化物可用以下方法进行测定,其步骤如下:
①在中性或弱酸性介质中先用过量的Br2,将试样中的I-氧化成![]() ;
;
②煮沸①所得溶液以除去过量的Br2,然后在酸性条件下加入过量的KI溶液,将![]() 还原为I2;
还原为I2;
③在②中加淀粉作指示剂,用Na2S2O3标准溶液滴定(2Na2S2O3+I2====2NaI+Na2S4O6)。
通过上述步骤可测得碘化物中I-的含量:
(1)写出步骤①②中发生反应的离子方程式:
①__________________________________________,
②__________________________________________。
(2)若样品中有1 mol I-,则最后耗用Na2S2O3的物质的量是多少?
(3)若在测定时,准确量取含KI的样品溶液25.00 mL,终点时耗用0.050 mol·L-1 Na2S2O3溶液20.06 mL,试计算样品溶液中KI的含量(g·L-1)。
查看习题详情和答案>>①在中性或弱酸性介质中先用过量的Br2将样品中的I-氧化成IO3-;
②煮沸①所得溶液以除去过量的Br2,然后在酸性条件下加入过量的KI溶液,将IO3- 还原为I2;
③在②中加淀粉作指示剂,用Na2S2O3标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)。
通过上述步骤可测得碘化物中I-的含量。
要求:
(1)写出步骤①②中发生反应的离子方程式。
(2)若样品中有1mol I-,则最后耗用Na2S2O3的物质的量是多少?
(3)若在测定时,准确量取含KI的样品溶液25.00mL,终点时耗用0.100mol/LNa2S2O3溶液20.06mL,试计算样品溶液中KI的含量(g/L)。
查看习题详情和答案>>
少量的碘化物可用以下方法进行测定:
①在中性或弱酸性介质中先用过量的
Br2将试样中的I-氧化成IO3-,对应的离子方程式为3Br2+I-+3H2O②煮沸①所得的溶液以除去过量的
Br2,然后在酸性条件下加入过量的KI溶液,将IO3-还原为I2,对应的离子方程式为6H++IO3-+5I-③在②中加入淀粉溶液,用
Na2S2O3标准溶液滴定(2Na2S2O3+I2(1)若样品中有1 mol I-,则最后消耗Na2S2O3的物质的量是________.
(2)若在测定时,准确量取含KI的样品溶液25.00 mL,终点时消耗0.100 mol/L Na2S2O3溶液20.1 mL,计算样品中KI的含量(g/L).
I.目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作致冷剂已经成为一种趋势,这一做法的积极意义在于
II.有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经过化学反应后使之变为可再生燃料甲醇.“绿色自由”构想技术流程如下:
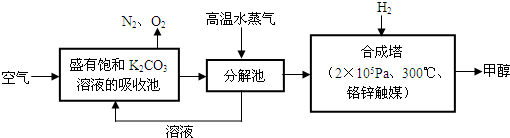
(1)吸收池中反应的化学方程式为:
(2)在合成塔中,若有4.4kgCO2与足量H2恰好完全反应,可放出4947kJ的热量,试写出合成塔中发生反应的热化学方程式
(3)控制不同的反应条件,CO2和H2反应还可以得到其它有机物.如将CO2和H2以1:4的体积比混合,在适当条件下反应,可获得重要能源CH4:CO2+4H2=CH4+2H2O;如将CO2和H2以1:3的体积比混合,还可生成某种重要的化工原料和水,该化工原料可能是
A.烷烃 B.烯烃 C.炔烃 D.芳香烃
(4)已知在443~473K时,用钴(Co)作催化剂可使CO2和H2生成C5~C8的烷烃,这是人工合成汽油的方法之一.要达到汽油的要求,CO2和H2体积比的取值范围应是
Ⅲ.若在一密闭恒容容器中充入CO2和H2的物质的量分别为1mol和3mol,发生反应得到CH3OH(g)和H2O(g).测得CO2和CH3OH(g)的浓度随时间变化如图所示:
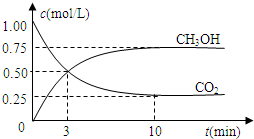
(1)从反应开始到平衡,氢气的平均反应速率v(H2)=
(2)下列措施中能使n(CH3OH)/n(CO2)增大的是
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2.