摘要:下列物质不存在共价键的是 ( ) A. CO2 B. NaOH C. BaCl2 D. NaNO3
网址:http://m.1010jiajiao.com/timu_id_3791400[举报]
下列说法正确的是( )
| A、由于铵盐中是有离子键构成的,因而化学性质相当稳定 | B、分子晶体中都存在分子间作用力,但可能不存在共价键 | C、在常见的四种晶体类型中,都有“原子(离子)半径越大,物质熔点越低”的规律 | D、常温下为气态或液态的物质,其固态时一定会形成分子晶体 |
(2012?株洲一模)已知A、B、C、D、E都是短周期主族元素,且原子序数依次增大.A、B原子的质子数之和等于C原子核内的质子数,D与B原子核外电子数之和为C原子核电荷数的两倍,D原子最外层电子数是其电子层数的3倍,A的单质是最轻的气体,E是所在周期原子半径最大的元素.请回答下列问题:
(1)E在周期表中的位置为
(2)化合物ABC是一种极弱的酸,分子中含有4个共价键,其电子式为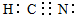
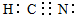 ;D、E形成的离子化合物中阴阳离子个数比为1:2,该化合物中是否存在共价键?为什么?
;D、E形成的离子化合物中阴阳离子个数比为1:2,该化合物中是否存在共价键?为什么?
(3)A、B、D、E可形成多种化合物,其中,甲、乙两种化合物的相对分子质量之比为42:41,则相同物质的量浓度的甲、乙水溶液碱性强弱顺序为:甲
(4)250C、1OlkPa下,BA4的燃烧热为a kJ/mol,9g液态水变为水蒸气吸热b kJ,则BA4燃烧生成二氧化碳和水蒸气的热化学方程式为
查看习题详情和答案>>
(1)E在周期表中的位置为
第三周期第ⅠA族
第三周期第ⅠA族
,C、D、E所形成的简单离子半径大小顺序为r(N3-)>r(O2- )>r(Na+)
r(N3-)>r(O2- )>r(Na+)
(用离子符号表示).(2)化合物ABC是一种极弱的酸,分子中含有4个共价键,其电子式为
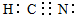
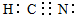
不一定存在共价键,如为Na2O2,O2-中存在共价键;如为Na2O,则不存在共价键
不一定存在共价键,如为Na2O2,O2-中存在共价键;如为Na2O,则不存在共价键
(3)A、B、D、E可形成多种化合物,其中,甲、乙两种化合物的相对分子质量之比为42:41,则相同物质的量浓度的甲、乙水溶液碱性强弱顺序为:甲
>
>
乙(填>、<或=),乙水解反应的离子方程式是CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-
 CH3COOH+OH-
CH3COOH+OH-CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-
. CH3COOH+OH-
CH3COOH+OH-(4)250C、1OlkPa下,BA4的燃烧热为a kJ/mol,9g液态水变为水蒸气吸热b kJ,则BA4燃烧生成二氧化碳和水蒸气的热化学方程式为
CH 4(g)+2O2(g)═CO 2(g)+2H2O(g);△H=-(a-4b)kJ/mol
CH 4(g)+2O2(g)═CO 2(g)+2H2O(g);△H=-(a-4b)kJ/mol
.