摘要:6.已知25℃时.电离常数Ka(HF)=3.6×10-4 mol/L.溶度积常数Ksp=1.46×10-10.现向1 L 0.2 mol/L HF溶液中加入1 L 0.2 mol/L CaCl2溶液.则下列说法中.正确的是 ( ) A.25℃时.0.1 mol/L HF溶液中pH=1 B.Ksp随温度和浓度的变化而变化 C.该体系中没有沉淀产生 D.该体系中HF与CaCl2反应产生沉淀 解析:A项.HF为弱酸.0.1 mol/L HF溶液pH>1,B项.Ksp只与温度有关,C项.混合后成0.1 mol/L HF溶液.设0.1 mol/L的HF溶液中c=x mol/L.则=3.6×10-4.x≈6×10-3 mol/L.混合后c=0.1 mol/L,0.1 mol/L×2=3.6×10-6>1.46×10-10.应有CaF2沉淀生成. 答案:D
网址:http://m.1010jiajiao.com/timu_id_3783959[举报]
|
已知25℃时,电离常数Ka(HF)=3.6×10-4 mol/L,溶度积常数Ksp(CaF2)=1.46×10-10 mol3/L3.现向1 L 0.2 mol/L HF溶液中加入1 L 0.2 mol/L CaCl2溶液,则下列说法中,正确的是 | |
| [ ] | |
A. |
25℃时,0.1 mol/L HF溶液中pH=1 |
B. |
Ksp(CaF2)随温度和浓度的变化而变化 |
C. |
该体系中,Ksp(CaF2)= |
D. |
该体系中有CaF2沉淀产生 |
已知25℃时,电离常数Ka(HF)=3.6×10-4 mol·L-1,溶度积常数KSP(CaF2)=1.46×10-10 mol3·L-3。现向1L 0.2 mol·L-1HF溶液中加入1L 0.2 mol·L-1CaCl2溶液,则下列说法中,正确的是( )
A.25℃时,0.1 mol·L-1HF溶液中pH=1 B.该体系中有CaF2沉淀产生
C.该体系中KSP(CaF2)= 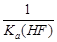 D.KSP(CaF2)随温度和浓度的变化而变化
D.KSP(CaF2)随温度和浓度的变化而变化
查看习题详情和答案>>
已知25℃时,电离常数Ka(HF)=3.6×10-4 mol/L.溶度积常数Ksp(CaF2)=1.46×10-10.现向1 L 0.2 mol/L HF溶液中加入1 L 0.2 mol/L CaCl2溶液.则下列说法不正确的是
[ ]
A.25℃时,0.1 mol/L HF溶液中pH>1
B.Ksp(CaF2)随温度的变化而变化
C.氟化钙和氟化氢都是弱电解质
D.该体系中有CaF2沉淀产生
查看习题详情和答案>>
B.Ksp(CaF2)随温度的变化而变化
C.氟化钙和氟化氢都是弱电解质
D.该体系中有CaF2沉淀产生
已知25℃时,电离常数Ka(HF)=3.6×10-4 mol·L-1,溶度积常数KSP(CaF2)=1.46×10-10 mol3·L-3。现向1L 0.2 mol·L-1HF溶液中加入1L 0.2 mol·L-1CaCl2溶液,则下列说法中,正确的是
[ ]
A.25℃时,0.1 mol·L-1HF溶液中pH=1
B.该体系中有CaF2沉淀产生
C.该体系中KSP(CaF2)=
D.KSP(CaF2)随温度和浓度的变化而变化
查看习题详情和答案>>
B.该体系中有CaF2沉淀产生
C.该体系中KSP(CaF2)=

D.KSP(CaF2)随温度和浓度的变化而变化
已知25℃时,电离常数Ka(HF)=3.6×10-4 mol·L-1,溶度积常数KSP(CaF2)=1.46×10-10 mol3·L-3。现向1L 0.2 mol·L-1HF溶液中加入1L 0.2 mol·L-1CaCl2溶液,则下列说法中,正确的是( )
| A.25℃时,0.1 mol·L-1HF溶液中pH=1 | B.该体系中有CaF2沉淀产生 |
C.该体系中KSP(CaF2)= | D.KSP(CaF2)随温度和浓度的变化而变化 |