摘要:1. C,2.C,3.A,4.D,5.D. 讲析:2.它比饱和的二十六酸C25H51COOH少12个H原子.故分子式为C25H39COOH.3.该有机物含有一个苯环.一个碳碳双键.两个碳氧双键.与氢气加成须6molH2.它含有一个酯基.须NaOH2mol.4.皂化完全时所得产物全部溶于水.5.根据题意可判断A是酯.B为醇.C是羧酸.D为醛.当它们分子中碳原子相等时.有M(D)<M(B)<M(C).
网址:http://m.1010jiajiao.com/timu_id_3778926[举报]
4-硫醚基喹唑啉类化合物是一种具有应用前景的抑菌药物,其合成路线如下:

已知:
(1)写出反应类型A→B
(2)满足下列条件的C的同分异构体的结构简式有
①苯的衍生物,且苯环上的一取代产物有两种;②苯环上有四个取代基,其中三个为甲氧基(-OCH3),其在苯环上位置与C相同;③含-COO-基团.
(3)写出C→D的化学方程式
 .由C→D的反应中还可能生成一种有机副产物,该副产物的结构简式为
.由C→D的反应中还可能生成一种有机副产物,该副产物的结构简式为
 .
.
(4)写出物质G的结构简式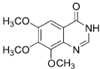
 .
.
(5)利用题给相关信息,以甲苯、HCONH2为原料,合成 .合成过程中无机试剂任选;合成路线流程图示例为:
.合成过程中无机试剂任选;合成路线流程图示例为:
提示:① ; ②
; ② ;③
;③

 .
.
查看习题详情和答案>>

已知:

(1)写出反应类型A→B
取代反应
取代反应
,E→F还原反应
还原反应
.(2)满足下列条件的C的同分异构体的结构简式有
4
4
种(不包含C).①苯的衍生物,且苯环上的一取代产物有两种;②苯环上有四个取代基,其中三个为甲氧基(-OCH3),其在苯环上位置与C相同;③含-COO-基团.
(3)写出C→D的化学方程式




(4)写出物质G的结构简式


(5)利用题给相关信息,以甲苯、HCONH2为原料,合成
 .合成过程中无机试剂任选;合成路线流程图示例为:
.合成过程中无机试剂任选;合成路线流程图示例为:
提示:①
 ; ②
; ② ;③
;③


A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显红色,它们相互转化关系如图所示.
请回答:
(1)写出B物质的化学式:
(2)写出第③步反应的化学方程式为
(3)第④步反应中溶液颜色的变化
(4)写出SO2和B反应的离子方程式
(5)F溶液中滴入NaOH溶液可能产生的实验现象是
查看习题详情和答案>>

请回答:
(1)写出B物质的化学式:
Cl2
Cl2
;F的名称:氯化亚铁
氯化亚铁
.(2)写出第③步反应的化学方程式为
Fe+2HCl=FeCl2+H2↑
Fe+2HCl=FeCl2+H2↑
.(3)第④步反应中溶液颜色的变化
溶液由黄色变为浅绿色
溶液由黄色变为浅绿色
;写出第④步反应的离子方程式2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
.(4)写出SO2和B反应的离子方程式
SO2+Cl2+2H2O=4H++SO42-+2Cl-
SO2+Cl2+2H2O=4H++SO42-+2Cl-
.(5)F溶液中滴入NaOH溶液可能产生的实验现象是
先生成灰白色沉淀,立即变成灰绿色,最后变成红褐色
先生成灰白色沉淀,立即变成灰绿色,最后变成红褐色
.A、B、C、D是四种常见单质,其对应元素的原子序数依次增大,其中B、D属于常见金属,其余均为常见化合物,J是一种黑色固体,I的浓溶液具有还原性,从A-I的所有物质之间有如下的转化关系: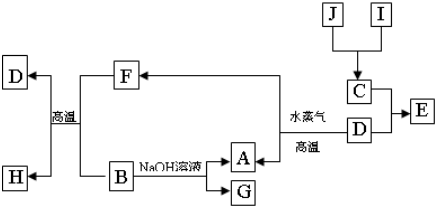
回答下列问题:
(1)写出物质C的构成元素在周期表中的位置
(2)写出B与F反应的化学方程式
(3)由E的饱和溶液可以制得胶体,具体制备方法是:
a.光束通过该液体时形成光亮的“通路”?
b.向液体中逐滴加入足量氢碘酸,先有沉淀产生,后沉淀逐渐溶解,再滴入几滴淀粉溶液,溶液变为蓝色
c.向该液体中加入硝酸银溶液,无沉淀产生?
d.将该液体加热、蒸干、灼烧,得红棕色固体?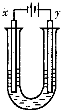
另取少量上述胶体置于U型管中,按如图装置图连接好装置.通电一小段时间后,X极附近的现象是
(4)取少量上述胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,可以看到溶液颜色逐渐变浅,最终得到黄色的溶液,发生此变化的离子方程式为
(5)G的水溶液显
(6)J在H2O2分解反应中作催化剂.若将适量J加入酸化的H2O2的溶液中,J溶解生成它的+2价离子,该反应的离子方程式是
查看习题详情和答案>>

回答下列问题:
(1)写出物质C的构成元素在周期表中的位置
第三周期、第ⅦA族
第三周期、第ⅦA族
.(2)写出B与F反应的化学方程式
8Al+3Fe3O4
9Fe+4Al2O3
| ||
8Al+3Fe3O4
9Fe+4Al2O3
.
| ||
(3)由E的饱和溶液可以制得胶体,具体制备方法是:
将饱和FeCl3溶液逐滴加入沸水中,继续加热至液体变为红褐色
将饱和FeCl3溶液逐滴加入沸水中,继续加热至液体变为红褐色
,用化学方程式表示该过程的原理:Fe3++3H2O
Fe(OH)3(胶体)+3H+
| ||
Fe3++3H2O
Fe(OH)3(胶体)+3H+
.若要提纯该胶体,采用的操作方法叫
| ||
渗析
渗析
.此液体具有的性质是abd
abd
(填写序号字母)a.光束通过该液体时形成光亮的“通路”?
b.向液体中逐滴加入足量氢碘酸,先有沉淀产生,后沉淀逐渐溶解,再滴入几滴淀粉溶液,溶液变为蓝色
c.向该液体中加入硝酸银溶液,无沉淀产生?
d.将该液体加热、蒸干、灼烧,得红棕色固体?

另取少量上述胶体置于U型管中,按如图装置图连接好装置.通电一小段时间后,X极附近的现象是
红褐色加深
红褐色加深
.(4)取少量上述胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,可以看到溶液颜色逐渐变浅,最终得到黄色的溶液,发生此变化的离子方程式为
Fe(OH)3+3H+=Fe3++3H2O
Fe(OH)3+3H+=Fe3++3H2O
.(5)G的水溶液显
碱
碱
性(填酸或碱);原因是(用离子方程式表 示)AlO2-+2H2O Al(OH)3+OH-
Al(OH)3+OH-
 Al(OH)3+OH-
Al(OH)3+OH-AlO2-+2H2O Al(OH)3+OH-
Al(OH)3+OH-
. Al(OH)3+OH-
Al(OH)3+OH-(6)J在H2O2分解反应中作催化剂.若将适量J加入酸化的H2O2的溶液中,J溶解生成它的+2价离子,该反应的离子方程式是
MnO2+H2O2+2H+═Mn2++O2↑+2H2O
MnO2+H2O2+2H+═Mn2++O2↑+2H2O
.A、B、C、D、E五种短周期元素,核电荷数依次增加,其中B的最外层电子数是内层电子总数的2倍,它们可形成含有非极性键的B2A2、A2C2、D2C2的化合物;E的单质在自然界中常在火山喷口附近出现.据此回答下列问题:
(1)写出D2C2的电子式:

(2)我国普遍采用一种方法制得含有A、C、E三种元素的某重要化工产品,其工业生成的第一步化学反应方程式为
(3)均由A、C、D、E四种元素组成的两种物质在溶液中反应的离子方程式为
(4)由A与C两种元素组成的一种化合物能使酸性高锰酸钾褪色,反应的离子方程式是
(5)单质B可与由A、C、E 三种元素组成的化合物在一定条件下反应生成EC2,该反应的化学方程式为
(6)B元素的氢化物有多种,1molB的某种氢化物中含有14mol电子,已知在25℃,101kPa下,1g该气态氢化物在足量氧气中完全燃烧生成液态水时放出热量为50kJ,写出该物质燃烧热的热化学方程式
查看习题详情和答案>>
(1)写出D2C2的电子式:


(2)我国普遍采用一种方法制得含有A、C、E三种元素的某重要化工产品,其工业生成的第一步化学反应方程式为
4FeS2+11O2
2Fe2O3+8SO2
| ||
4FeS2+11O2
2Fe2O3+8SO2
.
| ||
(3)均由A、C、D、E四种元素组成的两种物质在溶液中反应的离子方程式为
H++HSO3-=H2O+SO2↑
H++HSO3-=H2O+SO2↑
.(4)由A与C两种元素组成的一种化合物能使酸性高锰酸钾褪色,反应的离子方程式是
2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑
2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑
.(5)单质B可与由A、C、E 三种元素组成的化合物在一定条件下反应生成EC2,该反应的化学方程式为
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
| ||
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
.
| ||
(6)B元素的氢化物有多种,1molB的某种氢化物中含有14mol电子,已知在25℃,101kPa下,1g该气态氢化物在足量氧气中完全燃烧生成液态水时放出热量为50kJ,写出该物质燃烧热的热化学方程式
C2H2(g)+
O2(g)=2CO2(g)+H2O(l)△H=-1300kJ/mol
| 5 |
| 2 |
C2H2(g)+
O2(g)=2CO2(g)+H2O(l)△H=-1300kJ/mol
.| 5 |
| 2 |
A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去).请填空:
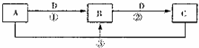
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式可能是
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为
(3)若D是氯碱工业的主要产品,B有两性,则反应②的离子方程式是
(4)若A、C、D都是常见气体,C是形成酸雨的主要气体,则反应③的化学方程式
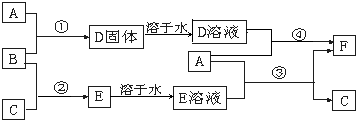
(5)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上.在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过.
 Ⅰ
Ⅰ
①图中X、Y分别是
②写出燃料电池B中负极上发生的电极反应
查看习题详情和答案>>

(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式可能是
FeCl3
FeCl3
;工业上制取A的离子方程式Ⅰ为2Cl-+2H2O
Cl2↑+H2↑+2OH-
| ||
2Cl-+2H2O
Cl2↑+H2↑+2OH-
.
| ||
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
(3)若D是氯碱工业的主要产品,B有两性,则反应②的离子方程式是
Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
.(4)若A、C、D都是常见气体,C是形成酸雨的主要气体,则反应③的化学方程式
2H2S+SO2=3S↓+H2O
2H2S+SO2=3S↓+H2O
.(5)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上.在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过.
 Ⅰ
Ⅰ①图中X、Y分别是
Cl2
Cl2
、H2
H2
(填化学式),分析比较图示中氢氧化钠质量分数a%>
>
b%(填“>”、“=”或“<”)②写出燃料电池B中负极上发生的电极反应
H2-2e-+2OH-=2H2O
H2-2e-+2OH-=2H2O
.