摘要:1.A 2.A 3.B.D 4.B 5.B
网址:http://m.1010jiajiao.com/timu_id_3778723[举报]
B、C、D、E是常见化合物或单质,有如下转化关系(略去条件和副产品).

(1)若A为Na,B为NaOH,C为Na2CO3,请写出A转化为B的离子方程式 .
(2)若B为Al2O3,C为钠盐,试写出B转化为C的化学方程式 .
(3)若A为气态单质,B为漂白粉的主要成份之一,C具有漂白性.试写A转化为B的化学方程式 .画出组成单质A的元素原子结构示意图 .
(4)若A、B、C均为钠盐的水溶液,B转化为C是海水中提取溴的原理,请写出B转化为C的离子方程式 .
(5)若A常温下为固态单质,化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,且D、E为同一物质,则B为 .
(6)若B、D为质子数小于18的元素原子形成的单质,且D所含元素原子的质子数是B的2倍,A转化为B,B转化为C两个反应均属置换反应,请写出A转化为B的化学方程式 .
查看习题详情和答案>>

(1)若A为Na,B为NaOH,C为Na2CO3,请写出A转化为B的离子方程式
(2)若B为Al2O3,C为钠盐,试写出B转化为C的化学方程式
(3)若A为气态单质,B为漂白粉的主要成份之一,C具有漂白性.试写A转化为B的化学方程式
(4)若A、B、C均为钠盐的水溶液,B转化为C是海水中提取溴的原理,请写出B转化为C的离子方程式
(5)若A常温下为固态单质,化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,且D、E为同一物质,则B为
(6)若B、D为质子数小于18的元素原子形成的单质,且D所含元素原子的质子数是B的2倍,A转化为B,B转化为C两个反应均属置换反应,请写出A转化为B的化学方程式
A.B.C.D.E、F是中学化学中常见的气体,它们均由短周期元素组成,具有如下性质:
①B能使湿润的红色石蕊试纸变蓝,D、F不能使湿润的石蕊试纸变色;
②A能使湿润的蓝色石蕊试纸先变红,后褪色;将红热的铜丝放入装有A的瓶中,瓶内充满棕黄色的烟;
③将点燃的镁条放入装有E的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
④D是最简单的有机物;F是空气中含量最多的气体.
⑤实验室中可用浓的C溶液与某黑色固体共热制A气体.
回答下列问题:
(1)B的化学式为
(2)③中发生反应的化学方程式是
(3)⑤中发生反应的化学方程式是
(4)已知标准状况下体积为1.12L的D完全燃烧生成E和液态水时,放出热量44.5kJ,写出表示1molD燃烧的热化学方程式
(5)一定条件下,向废水中加入CH3OH,将HNO3还原成F.若该反应消耗16gCH3OH转移3mol电子;该反应的化学方程式为
查看习题详情和答案>>
①B能使湿润的红色石蕊试纸变蓝,D、F不能使湿润的石蕊试纸变色;
②A能使湿润的蓝色石蕊试纸先变红,后褪色;将红热的铜丝放入装有A的瓶中,瓶内充满棕黄色的烟;
③将点燃的镁条放入装有E的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
④D是最简单的有机物;F是空气中含量最多的气体.
⑤实验室中可用浓的C溶液与某黑色固体共热制A气体.
回答下列问题:
(1)B的化学式为
NH3
NH3
,固态E可用作致冷剂
致冷剂
(写一种重要用途)(2)③中发生反应的化学方程式是
2Mg+CO2
2MgO+C
| ||
. |
2Mg+CO2
2MgO+C
;
| ||
. |
(3)⑤中发生反应的化学方程式是
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
;
| ||
(4)已知标准状况下体积为1.12L的D完全燃烧生成E和液态水时,放出热量44.5kJ,写出表示1molD燃烧的热化学方程式
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol
.(5)一定条件下,向废水中加入CH3OH,将HNO3还原成F.若该反应消耗16gCH3OH转移3mol电子;该反应的化学方程式为
5CH3OH+6HNO3═5CO2+3N2+13H2O
5CH3OH+6HNO3═5CO2+3N2+13H2O
.A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性.下述为相关实验步骤和实验现象:
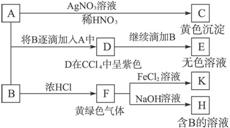
请回答:
(1)写出A、B和C的化学式:A
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:
(4)写出由F→H的化学方程式:
查看习题详情和答案>>

请回答:
(1)写出A、B和C的化学式:A
NaI
NaI
,BNaClO
NaClO
,CAgI
AgI
;(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
2I-+ClO-+H2O=I2+Cl-+2OH-
2I-+ClO-+H2O=I2+Cl-+2OH-
,I2+5ClO-+2OH-=2IO3-+5Cl-+H2O
I2+5ClO-+2OH-=2IO3-+5Cl-+H2O
;(3)写出将SO2气体通入K溶液中发生反应的离子方程式:
2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
;(4)写出由F→H的化学方程式:
Cl2+2NaOH=NaClO+NaCl+H2O
Cl2+2NaOH=NaClO+NaCl+H2O
.A、B、D、E、Y为5种短周期元素.
①A、B、D位于同一周期,D、Y位于同一主族.A的原子的最外层电子数是其次外层电子数的2倍.
②D的氢化物是最常用的溶剂,E的单质是一种生活中常见的金属.
请回答:
(1)AD2中具有的化学键的类型是
(2)高温时,6g A的单质与D的气态氢化物反应,生成两种还原性气体,吸收的热量为65.75kJ,其反应的热化学方程式是
(3)D与氢元素可组成含有10个电子的X-,与X-组成元素相同,原子数个数比也相同的分子的电子式是
 .
.
(4)将盛有一定量红棕色气体BD2的4L容器压缩至2L,待气体颜色不再变化时,容器内的压强(填“大于”、“等于”或“小于”)
(5)E的某种化合物可用作净水时的混凝剂,其原理是(用离子方程式表示)
(6)YD2气体通入足量BaCl2和B的最高价氧化物对应的水化物的混合溶液中,生成白色沉淀和无色气体,反应的离子方程式是
查看习题详情和答案>>
①A、B、D位于同一周期,D、Y位于同一主族.A的原子的最外层电子数是其次外层电子数的2倍.
②D的氢化物是最常用的溶剂,E的单质是一种生活中常见的金属.
请回答:
(1)AD2中具有的化学键的类型是
极性共价键
极性共价键
.(2)高温时,6g A的单质与D的气态氢化物反应,生成两种还原性气体,吸收的热量为65.75kJ,其反应的热化学方程式是
C(s)+H2O(g)=CO(g)+H2(g)△H=+131.5kJ/mol
C(s)+H2O(g)=CO(g)+H2(g)△H=+131.5kJ/mol
.(3)D与氢元素可组成含有10个电子的X-,与X-组成元素相同,原子数个数比也相同的分子的电子式是


(4)将盛有一定量红棕色气体BD2的4L容器压缩至2L,待气体颜色不再变化时,容器内的压强(填“大于”、“等于”或“小于”)
小于
小于
原来的2倍,原因是2NO2?N2O4为可逆反应,当将其体积压缩为原来的一半时,平衡向右移动,容器内气体分子总数减少,容器内压强小于原来的2倍
2NO2?N2O4为可逆反应,当将其体积压缩为原来的一半时,平衡向右移动,容器内气体分子总数减少,容器内压强小于原来的2倍
.(5)E的某种化合物可用作净水时的混凝剂,其原理是(用离子方程式表示)
Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
.(6)YD2气体通入足量BaCl2和B的最高价氧化物对应的水化物的混合溶液中,生成白色沉淀和无色气体,反应的离子方程式是
3Ba2++3SO2+2NO3-+2H2O=3BaSO4↓+2NO↑+4H+
3Ba2++3SO2+2NO3-+2H2O=3BaSO4↓+2NO↑+4H+
.A.B.C.D.E是中学化学常见单质,构成它们的元素的原子序数分别为α、b. c.d.е;且3 (a+b) = 2 (a+c) = 3 (d-a);X、Y、Z、M、N、W、H、K是常见化合物,X是B和C的化合产物,它们之间有如下转化关系(图中反应物和产物中的H2O已略去):
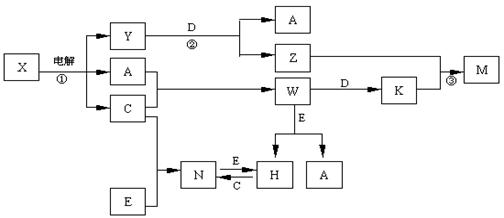
(1)Y的电子式为 ,构成D单质的元素在周期表中位于 周期 族。
(2)反应③的离子方程式为 E的氧化物与D在一定条件下反应的化学方程式为: 。
(3)固体N常温下即挥发,183℃升华,几乎溶于所有的有机溶剂和H2O中,据此判断
N为 型晶体。
(4)25℃时,PH=5的W和N的水溶液中由H2O电离出来的H+离子浓度之比为 。
查看习题详情和答案>>