网址:http://m.1010jiajiao.com/timu_id_3778558[举报]
 2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.
2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.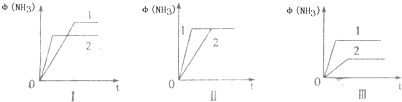
(1)在一容积固定的密闭容器中注入N2和H2两种气体,发生上述反应.在某温度下达到平衡时各物质的浓度分别为c(H2)=9.00mol/L,c(N2)=3.00mol/L,c(NH3)=4.00mol/L,此温度下该反应的平衡常数为
(2)三个相同容器中各充入1molN2和3molH2,在不同条件下反应并达到平衡,氨的体积分数随时间的变化如图所示.下列说法正确的是
A.图I可能是不同压强对反应的影响,且P2>P1
B.图Ⅱ可能是不同压强对反应的影响,且P1>P2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ一定是在同温同压下不同催化剂对反应的影响,且催化剂效果1>2
(3)将水蒸气通过红热的炭即产生水蒸气,化学方程式为:C(s)+H2O(g)
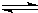 H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发
H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发(4)甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g).部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热(kJ?mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
(5)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池.请写出该电池的正极反应式
反应①:C(s)+H2O(g)=CO(g)+H2(g)△H1=akJ?mol-1,平衡常数为K1;
反应②:C(s)+CO2(g)=2CO(g)△H2=bkJ?mo1-1,平衡常数为K2;
又知反应CO(g)+H2O(g)=CO2(g)+H2(g)的平衡常数Kc随温度的变化如下表:
| 温度/ | 400 | 500 | 800 |
| 平衡常数Kc | 9.94 | 9 | 1 |
(1)上述反应中,a
(2)温度为800℃时,在一体积为10L的密闭容器中,通入一定量的CO和H2O (g),发生如下反应:CO(g)+H2O(g)=CO2(g)+H2(g),容器内各物质的浓度变化如下表.
800℃时物质的量浓度(mol?L-1)的变化
| 时间(min) | CO(g) | H2O(g) | CO2(g) | H2(g) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.120 | 0.220 | 0.080 | 0.080 |
| 3 | 0.080 | 0.180 | 0.120 | 0.120 |
| 4 | 0.100 | 0.200 | 0.100 | C1 |
| 5 | 0.067 | 0.267 | 0.133 | C2 |
②表中第3min反应处于
③表中3min~4min之间,平衡向
表中4min~5min之间数值发生变化,可能的原因是
a.正反应方向 b.逆反应方向 c.增加水蒸气
d.降低温度 e.使用催化剂 f.增加氢气浓度

(3)如图1、图2表示反应CO(g)+H2O(g)=CO2(g)+H2(g)在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:
①图1中时刻t2发生改变的条件是
②图2中时刻t2发生改变的条件是
 合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响.合成氨反应的化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ?mol-1.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷或焦炭与水蒸气反应制得.
合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响.合成氨反应的化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ?mol-1.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷或焦炭与水蒸气反应制得.(1)在一容积固定的密闭容器中注入N2和H2两种气体,发生上述反应.在某温度下达到平衡时,各物质的浓度分别是:c(H2)=9.00mol?L-1,c(N2)=3.00mol?L-1,c(NH3)=4.00mol?L-1,此温度下该反应的平衡常数K=
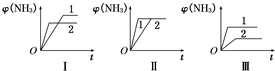
(2)在三个相同容器中各充入1mol N2和3mol H2,在不同条件下反应并达到平衡,氨的体积分数随时间变化的曲线如图所示.下列说法中正确的是
A.图Ⅰ可能是不同压强对反应的影响,且p2>p1
B.图Ⅱ可能是不同压强对反应的影响,且p1>p2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ可能是同温同压下不同催化剂对反应的影响,且催化剂性能1>2
(3)将水蒸气通过红热的炭即可产生水煤气,化学方程式为:
C(s)+H2O(g)═H2(g)+CO(g)△H=+131.3kJ?mol-1,△S=+133.7J?K-1?mol-1
该反应在常温下能否自发进行?
草酸是一种重要的试剂。下面是利用草酸探究浓度对反应速率影响的实验。
(1)为证明浓度对反应速率的影响,曾有教科书《化学反应原理》设计了如下实验:取两支试管,各加入4mL0.01mol·L-1的KMnO4酸性溶液,分别向其中加入0.1 mol·L-1、0.2 mol·L-1 H2C2O4溶液2mL,记录溶液褪色所需时间。
实验中发生反应的离子方程式为: ;
预期现象是:
①溶液的颜色由 色变为 色,
②其中加入 mol·L-1H2C2O4的那支试管中的溶液先变色。
然而实验结果并不尽如人意。实验过程颜色复杂,且褪色先缓慢,后逐渐加快;最大的问题是草酸浓度大,反应速率却更慢。
本实验能否作为课堂实验研究浓度对化学反应速率的影响?适宜的条件是怎样的?某校一研究小组对此进行了探究。下面是他们的实验报告的一部分:
表1 试验安排及结果
|
实验 编号 |
A(KMnO4溶液浓度/mol·L-1) |
B(草酸溶液浓度/mol·L-1) |
C(硫酸溶液浓度/mol·L-1) |
褪色时间/s |
|
1 |
3 |
3 |
1 |
336 |
|
2 |
1 |
2 |
3 |
82 |
|
3 |
3 |
1 |
3 |
76 |
|
4 |
1 |
3 |
2 |
133 |
|
5 |
2 |
3 |
3 |
102 |
|
6 |
3 |
2 |
2 |
156 |
|
7 |
2 |
2 |
1 |
300 |
|
8 |
2 |
1 |
2 |
115 |
|
9 |
1 |
1 |
1 |
200 |
应用SPSS16.0对正交试验结果进行方差分析,结果如下表
表2 各因素水平的数据处理结果
|
|
A(KMnO4溶液) |
B(草酸溶液) |
C(硫酸溶液) |
||||||
|
浓度/mol·L-1 |
0.005 |
0.010 |
0.015 |
0.1 |
0.5 |
0.9 |
6 |
12 |
18 |
|
平均褪色时间/s |
138.3 |
172.3 |
189.3 |
130.3 |
179.3 |
190.3 |
278.7 |
134.7 |
86.7 |
(2)由表2可知,三因素中, 的浓度(选填“A、B或C”,下空同)对反应速率影响显著,而 的浓度对反应速率的影响不显著。
(3)由表2可知,当高锰酸钾浓度为 mol·L-1、草酸浓度为 mol·L-1时,反应最快。即因素A、B的较适宜实验条件得以确定。
根据以上实验结果,该小组同学继续探究硫酸的浓度是怎样影响本反应速率的,测得如下实验结果:
表3 不同硫酸浓度下的褪色时间
|
c(H2SO4)/mol·L-1 |
18 |
16 |
14 |
12 |
10 |
8 |
6 |
|
褪色时间/s |
67 |
83 |
90 |
103 |
129 |
146 |
200 |
(4)根据课堂实验的合适时间,可选溶液的褪色时间约为1分钟和2分钟的两份溶液,即此时硫酸的浓度为 mol·L-1和 mol·L-1,这也有利于观察这两个反应速率的差异。
结论:草酸与酸性高锰酸钾溶液的反应,可作为课堂实验探究浓度对反应速率的影响。
查看习题详情和答案>>
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g) = CO2(g)+3H2(g);DH =+ 49.0 kJ·mol-1
②CH3OH(g)+1/2O2(g) = CO2(g)+2H2(g);DH =-192.9 kJ·mol-1 下列说法正确的是
A.CH3OH的燃烧热为192.9 kJ·mol-1
B.CH3OH的燃烧热为133.9 kJ·mol-1
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应:CH3OH(l) +1/2O2(g) = CO2(g) +2H2(g)的DH >-192.9 kJ·mol-1
查看习题详情和答案>>