摘要:(1)2Al+2OH-+2H2O=2AlO2-+3H2↑,AlO2-+H2O+H+=Al(OH)3↓; 343.2g 讲析:制得氢氧化铝的量(W2g)最少的原理为:铝与酸反应生成铝盐.铝与酸反应生成铝盐.再与适量的碱反应制得氢氧化铝,制得氢氧化铝的量(W3)最多的原理为:铝与碱反应生成偏铝酸盐.两者混合制得氢氧化铝.
网址:http://m.1010jiajiao.com/timu_id_3778348[举报]
 在稀硫酸、小苏打、二氧化碳、铜片、铝片、食盐、氢氧化钠、三氧化钨、铁片和木炭粉10种物质中,存在下面的相互关系,选择①~⑤为适当的物质,使有连线的两种物质能发生反应.
在稀硫酸、小苏打、二氧化碳、铜片、铝片、食盐、氢氧化钠、三氧化钨、铁片和木炭粉10种物质中,存在下面的相互关系,选择①~⑤为适当的物质,使有连线的两种物质能发生反应.(1)请推断出它们的化学式分别为:①
Al
Al
;③CO2
CO2
;⑤NaHCO3
NaHCO3
.(2)写出下列序号之间反应的离子方程式:
①和④:
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
;④和⑤:OH-+HCO3-=CO32-+H2O
OH-+HCO3-=CO32-+H2O
.现有金属单质A、B、H、I和气体甲、乙、丙及物质C、D、E、F、G.其中H是地壳中含量最多的金属,他们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:B
(2)写出反应①的离子方程式:
(3)写出反应④的离子方程式:
(4)实验室检验物质F中阳离子的常用试剂为
(5)H与C反应的化学方程式是
查看习题详情和答案>>

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:B
Fe
Fe
;乙Cl2
Cl2
.(2)写出反应①的离子方程式:
2Na+2H2O=2Na++2OH-+H2↑
2Na+2H2O=2Na++2OH-+H2↑
.(3)写出反应④的离子方程式:
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
.(4)实验室检验物质F中阳离子的常用试剂为
KSCN
KSCN
.(5)H与C反应的化学方程式是
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
.X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.请推断后回答下列问题:
(1)写出:W的原子结构示意图
 ,R离子的电子式
,R离子的电子式
 ,Y在周期表中的位置
,Y在周期表中的位置
(2)X、Y、Z三种元素形成的化合物属于
 .
.
(3)Z在Y单质中燃烧的产物电子式为
 ,其中含有的化学键类型为
,其中含有的化学键类型为
(4)Y、Z、W、R形成的简单离子半径由大到小顺序为
(5)W单质与Z的高价氧化物对应的水化物反应的离子方程式为
查看习题详情和答案>>
(1)写出:W的原子结构示意图




第二周期ⅥA族
第二周期ⅥA族
.(2)X、Y、Z三种元素形成的化合物属于
离子
离子
化合物(填“离子”或“共价”),其电子式为

(3)Z在Y单质中燃烧的产物电子式为


离子键、共价键
离子键、共价键
.(4)Y、Z、W、R形成的简单离子半径由大到小顺序为
S2->O2->Na+>Al3+
S2->O2->Na+>Al3+
.(5)W单质与Z的高价氧化物对应的水化物反应的离子方程式为
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
. 如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:①反应C+G
如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:①反应C+G| 高温 |
| ||
. |
(1)①中反映的化学方程式为
2Al+Fe2O3
2Fe+Al2O3
| ||
2Al+Fe2O3
2Fe+Al2O3
;
| ||
(2)化合物Ⅰ的电子式为
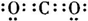
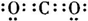
直线型
直线型
;(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量(写出离子方程式和计算过程);
(4)C与过量NaOH溶液反应的离子方程式为
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
,反应后溶液与过量化合物Ⅰ反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
;(5)E在I中燃烧观察到的现象是
镁条剧烈燃烧生成白色和黑色固体
镁条剧烈燃烧生成白色和黑色固体
.某固体混合物可能含Al、NH4Cl、MgCl2、Al2(SO4)3、FeCl2中的一种或几种,现对该混合物做如下实验.

已知气体经过碱石灰和浓硫酸时,二者质量均增大,气体A、B、C可能包含一种或几种气体.请回答:
(1)碱石灰的作用是
(2)混合物中是否存在NH4Cl,理由是
(3)混合物中是否存在FeCl2,理由是
(4)白色沉淀D为
(5)固体混合物中不能确定的物质是
查看习题详情和答案>>

已知气体经过碱石灰和浓硫酸时,二者质量均增大,气体A、B、C可能包含一种或几种气体.请回答:
(1)碱石灰的作用是
燥气体A,吸收其中的水蒸气
燥气体A,吸收其中的水蒸气
,固体混合物期中物质与浓NaOH 溶液反应生成气体C的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
.(2)混合物中是否存在NH4Cl,理由是
气体B经过浓硫酸后,浓硫酸质量增大,说明NH3被吸收,混合物中含有NH4Cl
气体B经过浓硫酸后,浓硫酸质量增大,说明NH3被吸收,混合物中含有NH4Cl
.(3)混合物中是否存在FeCl2,理由是
白色沉淀D久置颜色无明显变化,说明不存在FeCl2
白色沉淀D久置颜色无明显变化,说明不存在FeCl2
.(4)白色沉淀D为
Mg(0H)2
Mg(0H)2
(填化学式).(5)固体混合物中不能确定的物质是
Al2(SO4)3
Al2(SO4)3
(填化学式).