摘要:B 2.C 3.C. 4.A.C 5.D 6.C 7.C 8.A 9.B.10.A 11.A.12.A.D 讲析:1.等质量的Si和O2反应时Si过量.过量的Si也是固体.所以固体中氧的质量分数为50%. 4.反应1.2是氧化还原反应.不是可逆反应.根据能量守恒原理.正向反应是放热反应.逆向反应为吸热反应. 8. CO2是由分子构成的.是分子晶体.SiO2是由原子构成的.是原子晶体.物理性质不同.化学性质几乎相同. 9. SiO2不与盐酸反应.CaO.CaCO3与盐酸反应生成可溶性的物质. 10.活性炭有吸附性.能吸附有色物质使溶液褪色.没有发生化学反应.过氧化钠.漂白粉将有色物质氧化成无色物质具有漂白性.二氧化硫与有色物质结合成不稳定的无色物质. 12.该题为试剂的保存题.见光易分解的物质应避光保存.在空气中易氧化的物质应隔绝空气保存.碱性溶液不用玻璃塞.
网址:http://m.1010jiajiao.com/timu_id_3777877[举报]
A、B、C、D为按顺序排列的前四种卤素单质,仔细分析下表中的数据,回答有关问题.
(1)在标准状况下为液体的卤素单质是
(2)A的相对分子质量为
(3)写出B与水反应的化学方程式
(4)卤素单质B、C、D的氧化性由大到小的顺序为
查看习题详情和答案>>
| 卤素单质 | 密度(标准状况下) | 沸点/℃ | 熔点/℃ | 溶解度(标准状况下,100g水中) |
| A | 1.696 g?l-1 | -188.1 | -219.6 | -- |
| B | 3.214 g?l-1 | -34.6 | -101 | 226 cm3 |
| C | 3.119 g?cm-3 | 58.78 | -7.2 | 4.16 g |
| D | 4.93 g?cm-3 | 184.4 | 113.5 | 0.029 g |
C
C
(填字母,下同),为固体的卤素单质是D
D
.(2)A的相对分子质量为
38
38
(保留整数)(3)写出B与水反应的化学方程式
Cl2+H2O═HCl+HClO
Cl2+H2O═HCl+HClO
(4)卤素单质B、C、D的氧化性由大到小的顺序为
Cl2>Br2>I2
Cl2>Br2>I2
(用化学式表示)A、B、C、D、E是中学化学中五种常见元素,有关信息如下:
请回答下列问题:
(1)A的氢化物分子的电子式是
 ,其水溶液能使酚酞变红的原因用电离方程式解释为:
,其水溶液能使酚酞变红的原因用电离方程式解释为:
(2)A、D的氢化物相互反应,产生白色固体,对该固体中阳离子存在检验的操作方法是:
(3)B、C组成的某种化合物和B的某种氢化物反应可生成B的单质,则B、C组成的该化合物所含有的化学键为
(4)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(5)E制品通常在潮湿空气中发生电化学腐蚀,该过程的正极反应式为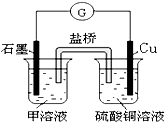
(6)若在D与E组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图所示,其反应中正极出现的现象是
查看习题详情和答案>>
| 元素 | 有关信息 |
| A | 最高价氧化物对应的水化物与其氢化物反应生成离子化合物 |
| B | 地壳中含量最多的元素 |
| C | 单质须保存在煤油中 |
| D | 单质与NaOH溶液反应可用于生产漂白液 |
| E | 单质是生活中用量最大的金属,其制品在潮湿空气中易被腐蚀或损坏 |
(1)A的氢化物分子的电子式是


NH3?H2O  NH4++OH-
NH4++OH-
 NH4++OH-
NH4++OH-NH3?H2O  NH4++OH-
NH4++OH-
. NH4++OH-
NH4++OH-(2)A、D的氢化物相互反应,产生白色固体,对该固体中阳离子存在检验的操作方法是:
取该白色固体少许于试管中,加入适量浓NaOH溶液并加热,用湿润的红色石蕊试纸接近试管口检验放出的气体,若试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生)
取该白色固体少许于试管中,加入适量浓NaOH溶液并加热,用湿润的红色石蕊试纸接近试管口检验放出的气体,若试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生)
,证明存在该阳离子.(3)B、C组成的某种化合物和B的某种氢化物反应可生成B的单质,则B、C组成的该化合物所含有的化学键为
离子键和共价键
离子键和共价键
.(4)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:
①③
①③
.①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(5)E制品通常在潮湿空气中发生电化学腐蚀,该过程的正极反应式为
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.
(6)若在D与E组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图所示,其反应中正极出现的现象是
黄色溶液慢慢变为浅绿色
黄色溶液慢慢变为浅绿色
,负极的反应式为:Cu-2e-=Cu2+
Cu-2e-=Cu2+
.
A、B、C、D、E五种元素,A元素的周期数、主族数、原子序数相同;B的基态原子核外有3种能量不同的原子轨道,且每种轨道中的电子数相同;C元素的电离能如图所示;D元素的价电子构型为nsnnpn+2;E是第4周期的过渡金属元素,血红蛋白中的E元素与BD形成的配位键比与D2形成的配位键强.E单质与BD形成的配合物E(BD)5,常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂.

(1)E(BD) 5晶体属于 (填晶体类型).
(2)A元素和B元素组成的化合物分子之间 (填“有”或“没有”)形成氢键.
(3)基态E原子的电子排布式为 .
(4)B、C、D三种元素的电负性由大到小的顺序是 (填元素符号).
(5)C2和B2A2的分子中根据电子云重叠的方式不同,都包含的共价键类型有 .
(6)已知原子数和电子数相同的微粒叫等电子体,等电子体的结构相似.根据下表数据,说明BD分子比C2分子活泼的原因 .
查看习题详情和答案>>

(1)E(BD) 5晶体属于
(2)A元素和B元素组成的化合物分子之间
(3)基态E原子的电子排布式为
(4)B、C、D三种元素的电负性由大到小的顺序是
(5)C2和B2A2的分子中根据电子云重叠的方式不同,都包含的共价键类型有
(6)已知原子数和电子数相同的微粒叫等电子体,等电子体的结构相似.根据下表数据,说明BD分子比C2分子活泼的原因
| X-Y | X=Y | X≡Y | |
| BD的键能(kJ?mol-1) | 357.7 | 798.9 | 1071.9 |
| C2的键能(kJ?mol-1) | 154.8 | 418.4 | 941.7 |
A、B、C、D、E、F、G、H、I、J 均为有机化合物,其转化关系如图所示.已知B 和 C 均为有支链的有机化合物;C在反应③中只能生成一种有机产物;G能使溴的四氯化碳溶液褪色.回答问题: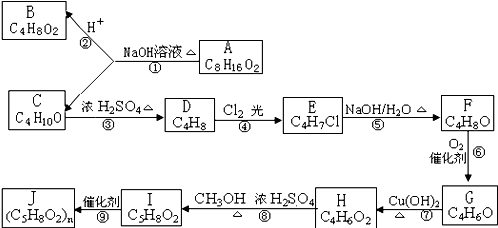
(1)G的结构简式: .⑦的反应类型 .
(2)步骤⑤的化学方程式 .
(3)A在隔绝加热条件下可发生消去反应得到D,请写出该消去反应中除D外的另一个产物的结构简式 .
(4)步骤④中的“Cl2、光”能否改为“饱和氯水”?请说明原因:
(5)写出与H 具有相同官能团的同分异构体的结构简式
(6)在一定条件下,酯与醇会发生酯交换,生成新的酯和醇.请尝试书写I与F发生的酯交换反应方程式: .
(7)一定条件下,G和H发生1:1聚合,聚合产物有多种.写出其中两种聚合产物的结构简式: .
查看习题详情和答案>>

(1)G的结构简式:
(2)步骤⑤的化学方程式
(3)A在隔绝加热条件下可发生消去反应得到D,请写出该消去反应中除D外的另一个产物的结构简式
(4)步骤④中的“Cl2、光”能否改为“饱和氯水”?请说明原因:
(5)写出与H 具有相同官能团的同分异构体的结构简式
(6)在一定条件下,酯与醇会发生酯交换,生成新的酯和醇.请尝试书写I与F发生的酯交换反应方程式:
(7)一定条件下,G和H发生1:1聚合,聚合产物有多种.写出其中两种聚合产物的结构简式:
A、B、C、D四种短周期元素的原子半径依次减小,D能分别与A、B、C形成电子总数为10的分子X、Y、Z.C原子的最外层电子排布为nsnnp2n.E的原子序数为29.
(1)A、B、C的第一电离能由小到大的顺序为 (用元素符号表示).
(2)X是含有 键(填“非极性”或“极性”,下同)的 分子.
(3)A的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为 .
(4)Y分子的空间构型为 ,其中心原子采取 杂化.
(5)一种由B、C组成的化合物与AC2互为等电子体,其化学式为 .
(6)Y是一种易液化的气体,请简述其易液化的原因 .
(7)写出E2+的电子排布式 ,并写出E2+在Z中通入足量Y得到深蓝色溶液的离子方程式 .
查看习题详情和答案>>
(1)A、B、C的第一电离能由小到大的顺序为
(2)X是含有
(3)A的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为
(4)Y分子的空间构型为
(5)一种由B、C组成的化合物与AC2互为等电子体,其化学式为
(6)Y是一种易液化的气体,请简述其易液化的原因
(7)写出E2+的电子排布式