摘要:B.D 2.B 3.B 4.B 5.C 6.B 7.B.D 8.D 9.C 讲析:1. C60为单质.是碳的同素异形体.2. CaCO3溶于盐酸产生气体.CaO溶于盐酸.SiO2不溶于盐酸.加足量盐酸有气体放出的有CaCO3.不能全部溶解的有SiO2.3. CO2与BaCl2溶液不反应,CO2与Na2SiO3反应生成H2SiO3沉淀,CO2与Ca(ClO)2反应生成CaCO3沉淀.CO2继续与CaCO3沉淀反应生成可溶的Ca(HCO3)2,CO2与饱和Na2CO3溶液反应生成NaHCO3沉淀.4. 10gCaCO3与盐酸反应生成4.4g CO2.根据平均值原理.10g 杂质生成的CO2应该大于4.4g.所以固体一定含MgCO3.有残留物不溶于盐酸.一定有SiO2.固体中可能有K2CO3.8. Ca(HCO3)2在加热条件下分解成CaCO3.CO2.H2O.CaCO3高温下分解成CaO.CO2.Ca(HCO3)2完全分解是余固体质量是原试样的50/81.大于50%.说明有CaCO3分解了.所以Ca(HCO3)2的分解率为100%.
网址:http://m.1010jiajiao.com/timu_id_3777861[举报]
A、B、C、D、E是中学化学中五种常见元素,有关信息如下:
请回答下列问题:
(1)A的氢化物分子的电子式是
 ,其水溶液能使酚酞变红的原因用电离方程式解释为:
,其水溶液能使酚酞变红的原因用电离方程式解释为:
(2)A、D的氢化物相互反应,产生白色固体,对该固体中阳离子存在检验的操作方法是:
(3)B、C组成的某种化合物和B的某种氢化物反应可生成B的单质,则B、C组成的该化合物所含有的化学键为
(4)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(5)E制品通常在潮湿空气中发生电化学腐蚀,该过程的正极反应式为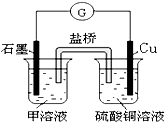
(6)若在D与E组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图所示,其反应中正极出现的现象是
查看习题详情和答案>>
| 元素 | 有关信息 |
| A | 最高价氧化物对应的水化物与其氢化物反应生成离子化合物 |
| B | 地壳中含量最多的元素 |
| C | 单质须保存在煤油中 |
| D | 单质与NaOH溶液反应可用于生产漂白液 |
| E | 单质是生活中用量最大的金属,其制品在潮湿空气中易被腐蚀或损坏 |
(1)A的氢化物分子的电子式是


NH3?H2O  NH4++OH-
NH4++OH-
 NH4++OH-
NH4++OH-NH3?H2O  NH4++OH-
NH4++OH-
. NH4++OH-
NH4++OH-(2)A、D的氢化物相互反应,产生白色固体,对该固体中阳离子存在检验的操作方法是:
取该白色固体少许于试管中,加入适量浓NaOH溶液并加热,用湿润的红色石蕊试纸接近试管口检验放出的气体,若试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生)
取该白色固体少许于试管中,加入适量浓NaOH溶液并加热,用湿润的红色石蕊试纸接近试管口检验放出的气体,若试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生)
,证明存在该阳离子.(3)B、C组成的某种化合物和B的某种氢化物反应可生成B的单质,则B、C组成的该化合物所含有的化学键为
离子键和共价键
离子键和共价键
.(4)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:
①③
①③
.①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(5)E制品通常在潮湿空气中发生电化学腐蚀,该过程的正极反应式为
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.
(6)若在D与E组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图所示,其反应中正极出现的现象是
黄色溶液慢慢变为浅绿色
黄色溶液慢慢变为浅绿色
,负极的反应式为:Cu-2e-=Cu2+
Cu-2e-=Cu2+
.有4组同一族元素所形成的不同物质,在101kPa时测定它们的沸点(℃)如下表所示:
下列各项判断正确的是( )
| 第一组 | He-268.8 | (a)-249.5 | Ar-185.8 | Kr-151.7 |
| 第二组 | F2 -187.0 | Cl2 -33.6 | (b) 58.7 | I2 184.0 |
| 第三组 | (c) 19.4 | HCl-84.0 | HBr-67.0 | HI-35.3 |
| 第四组 | H2O 100.0 | H2S-60.2 | (d) 42.0 | H2Te-1.8 |
| A、abc的化学式分别为Ne2、Br2、HF |
| B、第三组与第四组相比较,化合物的稳定顺序为:HBr>d |
| C、第三组物质溶于水后,溶液的酸性:c>HCl>HBr>HI |
| D、第四组物质中H2O的沸点最高,是因为H2O分子内存在氢键 |
甲、乙、丙三位同学分别用如下甲、乙、丙三套实验装置及化学药品(其中碱石灰为固体氢氧化钠和生石灰的混合物)制取氨气.请你参与探究,并回答下列问题:
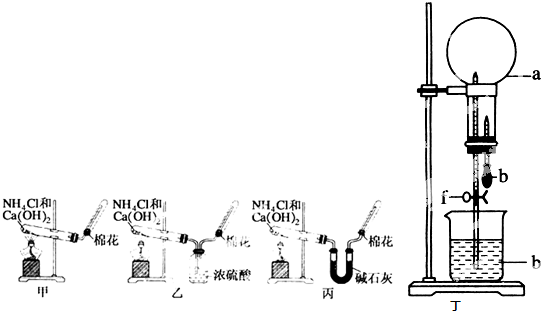
(1)三位同学制取氨气的化学方程式为: .
(2)三位同学都用向下排空气法收集氨气,而不用排水法,其原因是
A.氨气难溶于水 B.氨气极易溶于水
C.氨气密度比空气大 D.氨气密度比空气小
E.氨气密度比水大 F.氨气密度比水小
(3)三位同学用上述装置制取氨气时,其中乙同学没有收集到氨气,收集不到氨气的主要原因是 (用化学方程式表示).
(4)检验氨气是否收集满的方法是 .
A.闻到有氨气逸出
B.棉花被气体冲出
C.用湿润的红色石蕊试纸在试管口检验,发现试纸变蓝
D.用湿润的蓝色石蕊试纸在试管口检验,发现试纸变红
(5)三位同学都认为他们的实验装置也可用于加热碳酸氢铵固体制取纯净的氨气,你判断能够达到实验目的是 (填“甲”、“乙”或“丙”).
(6)要得到干燥的氨气可选用 作干燥剂.
A.碱石灰(CaO和NaOH的混合物)
B.浓硫酸
C.浓硝酸
D.氢氧化钠溶液
(7)用如图丁装置进行喷泉实验,烧瓶中已装满干燥氨气(标准状况),引发水向上喷的操作是 .
查看习题详情和答案>>

(1)三位同学制取氨气的化学方程式为:
(2)三位同学都用向下排空气法收集氨气,而不用排水法,其原因是
A.氨气难溶于水 B.氨气极易溶于水
C.氨气密度比空气大 D.氨气密度比空气小
E.氨气密度比水大 F.氨气密度比水小
(3)三位同学用上述装置制取氨气时,其中乙同学没有收集到氨气,收集不到氨气的主要原因是
(4)检验氨气是否收集满的方法是
A.闻到有氨气逸出
B.棉花被气体冲出
C.用湿润的红色石蕊试纸在试管口检验,发现试纸变蓝
D.用湿润的蓝色石蕊试纸在试管口检验,发现试纸变红
(5)三位同学都认为他们的实验装置也可用于加热碳酸氢铵固体制取纯净的氨气,你判断能够达到实验目的是
(6)要得到干燥的氨气可选用
A.碱石灰(CaO和NaOH的混合物)
B.浓硫酸
C.浓硝酸
D.氢氧化钠溶液
(7)用如图丁装置进行喷泉实验,烧瓶中已装满干燥氨气(标准状况),引发水向上喷的操作是
Q、R、X、Y、Z五种元素的原子序数依次递增.已知:①Z的原子序数为29,其余的均为短周期主族元素;②Y原子价电子(外围电子)排布msnmpn;③R原子核外L层电子数为奇数;④Q、X原子p轨道的电子数分别为2和4.请回答下列问题:
(1)Z2+的核外电子排布式是 .
(2)在[Z(NH3)4]2+离子中,Z2+的空轨道接受NH3分子提供的 形成配位键.
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 .
a.稳定性:甲>乙,沸点:甲>乙 b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙 d.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小到大的顺序为 (用元素符号作答)
(5)Q的一种氢化物相对分子质量为26,其中分子中的σ键与π键的键数之比为 ,其中心原子的杂化类型是 .
(6)若电子由3d能级跃迁至4p能级时,可通过光谱仪直接摄取 .
A.电子的运动轨迹图象 B.原子的吸收光谱
C.电子体积大小的图象 D.原子的发射光谱
(7)某元素原子的价电子构型为3d54S1,该元素属于 区元素,元素符号是 .
查看习题详情和答案>>
(1)Z2+的核外电子排布式是
(2)在[Z(NH3)4]2+离子中,Z2+的空轨道接受NH3分子提供的
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是
a.稳定性:甲>乙,沸点:甲>乙 b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙 d.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小到大的顺序为
(5)Q的一种氢化物相对分子质量为26,其中分子中的σ键与π键的键数之比为
(6)若电子由3d能级跃迁至4p能级时,可通过光谱仪直接摄取
A.电子的运动轨迹图象 B.原子的吸收光谱
C.电子体积大小的图象 D.原子的发射光谱
(7)某元素原子的价电子构型为3d54S1,该元素属于
A、B、C、D、E、F、G、H、I、J 均为有机化合物,其转化关系如图所示.已知B 和 C 均为有支链的有机化合物;C在反应③中只能生成一种有机产物;G能使溴的四氯化碳溶液褪色.回答问题: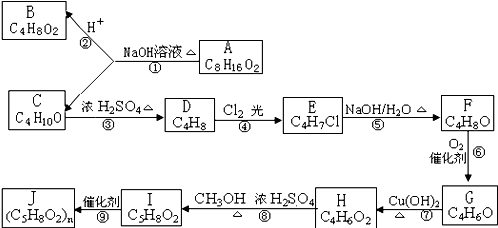
(1)G的结构简式: .⑦的反应类型 .
(2)步骤⑤的化学方程式 .
(3)A在隔绝加热条件下可发生消去反应得到D,请写出该消去反应中除D外的另一个产物的结构简式 .
(4)步骤④中的“Cl2、光”能否改为“饱和氯水”?请说明原因:
(5)写出与H 具有相同官能团的同分异构体的结构简式
(6)在一定条件下,酯与醇会发生酯交换,生成新的酯和醇.请尝试书写I与F发生的酯交换反应方程式: .
(7)一定条件下,G和H发生1:1聚合,聚合产物有多种.写出其中两种聚合产物的结构简式: .
查看习题详情和答案>>

(1)G的结构简式:
(2)步骤⑤的化学方程式
(3)A在隔绝加热条件下可发生消去反应得到D,请写出该消去反应中除D外的另一个产物的结构简式
(4)步骤④中的“Cl2、光”能否改为“饱和氯水”?请说明原因:
(5)写出与H 具有相同官能团的同分异构体的结构简式
(6)在一定条件下,酯与醇会发生酯交换,生成新的酯和醇.请尝试书写I与F发生的酯交换反应方程式:
(7)一定条件下,G和H发生1:1聚合,聚合产物有多种.写出其中两种聚合产物的结构简式: