网址:http://m.1010jiajiao.com/timu_id_3777767[举报]
1-乙氧基萘是一种无色液体,密度比水大,不溶于水,易溶于乙醇,熔点5.5℃,沸点267℃。1-萘酚(性质与苯酚相似)熔点96℃,沸点278℃,微溶于水,易溶于乙醇,乙醇的沸点为78.5℃。1-乙氧基萘常用作香料,也可合成其他香料。实验室制备1-乙氧基萘的过程如下:
 +C2H5OH
+C2H5OH
 +H2O
+H2O
1-萘酚 1-乙氧基萘
(1)将72g1-萘酚溶于100mL无水乙醇中,加入5mL浓硫酸混合。将混合液置于如图所示的容器中加热充分反应。实验中使用过量乙醇的原因是 。烧瓶上连接长直玻璃管的主要作用是 。

(2)反应结束,将烧瓶中的液体倒入冷水中,经处理得到有机层。为提纯产物有以下四步操作:①蒸馏;②水洗并分液;③用10%的NaOH溶液碱洗并分液;④用无水氯化钙干燥并过滤。正确的顺序是 (填序号)。
A.③②④① B.①②③④ C.②①③④
(3)实验测得1-乙氧基萘的产量与反应时间、温度的变化如图所示,时间延长、温度升高,1-乙氧基萘的产量下降的原因可能是 、 。

(4)某同学推测经提纯的产品可能还含有1-萘酚、乙醇、硫酸和水等杂质,设计了如下方案进行检验,请在答题卡上完成表中内容。
|
实验目的 |
实验操作 |
预期现象和结论 |
|
①用金属钠检验1-乙氧基萘是否纯净 |
取少量经提纯的产品于试管A中,加入金属钠 |
若 ,则产品纯净; 若 ,则产品不纯。 |
|
②检验经提纯的产品是否含有1-萘酚 |
|
若 ,则含有1-萘酚; 若 ,则不含1-萘酚。 |
查看习题详情和答案>>
1-乙氧基萘是一种无色液体,密度比水大,不溶于水,易溶于乙醇,熔点5.5℃,沸点267℃。1-萘酚(性质与苯酚相似)熔点96℃,沸点278℃,微溶于水,易溶于乙醇,乙醇的沸点为78.5℃。1-乙氧基萘常用作香料,也可合成其他香料。实验室制备1-乙氧基萘的过程如下: +C2H5OH
+C2H5OH
 +H2O
+H2O
1-萘酚 1-乙氧基萘
(1)将72g1-萘酚溶于100mL无水乙醇中,加入5mL浓硫酸混合。将混合液置于如图所示的容器中加热充分反应。实验中使用过量乙醇的原因是 。烧瓶上连接长直玻璃管的主要作用是 。 
(2)反应结束,将烧瓶中的液体倒入冷水中,经处理得到有机层。为提纯产物有以下四步操作:①蒸馏;②水洗并分液;③用10%的NaOH溶液碱洗并分液;④用无水氯化钙干燥并过滤。正确的顺序是 (填序号)。
A.③②④① B.①②③④ C.②①③④
(3)实验测得1-乙氧基萘的产量与反应时间、温度的变化如图所示,时间延长、温度升高,1-乙氧基萘的产量下降的原因可能是 、 。
(4)某同学推测经提纯的产品可能还含有1-萘酚、乙醇、硫酸和水等杂质,设计了如下方案进行检验,请在答题卡上完成表中内容。
| 实验目的 | 实验操作 | 预期现象和结论 |
| ①用金属钠检验1-乙氧基萘是否纯净 | 取少量经提纯的产品于试管A中,加入金属钠 | 若 ,则产品纯净; 若 ,则产品不纯。 |
| ②检验经提纯的产品是否含有1-萘酚 | | 若 ,则含有1-萘酚; 若 ,则不含1-萘酚。 |
二氧化硫是一种无色、有刺激性气味的气体。空气中二氧化硫的浓度只有百万分之一时,我们就会感到胸部有一种被压迫的不适感。当浓度达到百万分之八时,人就会感到呼吸困难。二氧化硫的危害还在于它常常跟大气中的飘尘结合在一起,进入人和其他动物的肺部,或在高空中与水蒸气结合成酸雨而降落下来,对人和其他动植物造成危害。目前,我国的能源结构主要以煤为主,因此,我国的大气污染是以烟尘和二氧化硫为代表的典型的煤烟型污染。1989年,科学研究人员对北京的两个居民区进行了大气污染与死亡率的关系研究。研究结果表明,大气中二氧化硫的浓度每增加1倍,总死亡率就增加11%。所以我们要时刻警惕二氧化硫污染。
据统计,世界各国每年排入大气中的二氧化硫的总量达1.5亿吨以上,而且呈逐年上升趋势。这些二氧化硫主要是过度燃烧煤和石油生成的。中国是燃煤大国,随着燃煤量的增加,排放的二氧化硫的量也不断增加。二氧化硫的大量排放使城市的空气污染不断加重,并导致我国出现大面积的酸雨。我国的酸雨主要是硫酸型的,要治理酸雨污染,就要控制二氧化硫的排放量。
为了保护环境,变废为宝,我们可以采用多种方法进行烟道气脱硫,以防止空气污染并回收和利用二氧化硫。
方法一:冶金厂利用一氧化碳还原二氧化硫。
SO2+2CO
 S+2CO2
S+2CO2方法二:硫酸厂通常用氨水吸收二氧化硫。
SO2+2NH3+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3
当吸收液达到一定浓度时,再用质量分数为93%的浓硫酸酸化:
2NH4HSO3+H2SO4(浓)=(NH4)2SO4+2SO2↑+2H2O
(NH4)2SO3+H2SO4(浓)=(NH4)2SO4+SO2↑+H2O
放出的二氧化硫经液化得到液态二氧化硫,可用于制取漂白剂、消毒剂,也可用于生产硫酸(前苏联曾用烟道气生产了百万吨硫酸)。硫酸铵溶液经过结晶、分离、干燥,可用于制化肥(硫铵)。
方法三:用纯碱溶液吸收二氧化硫。
2Na2CO3+SO2+H2O=2NaHCO3+Na2SO3
2NaHCO3+SO2=Na2SO3+2CO2+H2O
Na2SO3+SO2+H2O=2NaHSO3
方法四:用石灰水处理低浓度的二氧化硫烟道气也具有重要的意义。
其原理是将烟道气经水洗、冷却、除尘后,在吸收塔内用质量分数为10%的石灰乳浆吸收,再将吸收后的浆液用加压空气氧化,生成石膏。缺少石膏的日本、美国、瑞典大都采用此法处理烟道气。
思考题:
1.上述处理和回收二氧化硫的措施分别利用了SO2的什么性质?
2.你能写出方法四的化学方程式吗? 查看习题详情和答案>>
实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如下图所示:
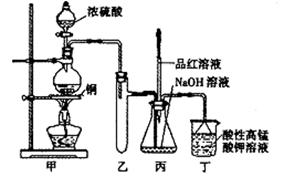
请回答:
(1)实验中取一定量Cu片和一定量浓H2SO4放在圆底烧瓶中共热,至反应结束后,发现烧瓶中还有少量Cu剩余,有人认为还有一定量的H2SO4剩余,原因是
,在不增加浓H2SO4的前提下,若使剩余铜片溶解可再加入 (填写两种属于不同类别的物质)。
(2)向反应后的溶液中加入足量的CuO,使剩余的H2SO4全部转化为CuSO4,过滤后将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4·XH2O)某小组同学采用加热法测定该晶体里结晶水X的值;
①在他们的实验操作中至少称量 次。
②下面是其中一次实验的数据
| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.6g |
根据上表数据计算判断x的实测值比理论值(x=5) (填“偏大”或“偏小”)。
(3)装置乙的作用是: ;
(4)下列说法正确的是: (填序号)。
a.甲装置使用的玻璃仪器有:酒精灯、玻璃管、长颈漏斗、圆底烧瓶
b.KMnO4溶液用于尾气处理
c.当把品红溶液滴入到锥形瓶中,若品红不褪色,说明无NaHSO3产生
d.当把品红溶液滴入到锥形瓶中,若品红褪色,说明NaOH已完全转化为NaHSO3
e.若把品红溶液换成酸性高锰酸钾溶液,并滴入到锥形瓶中,不显紫红色,说明NaOH已完全转化为NaHSO3
f.此装置换上其它药品后,不能制取和收集少量纯净的氯气
查看习题详情和答案>>(14分)实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如下图所示:

请回答:
(1)实验中取一定量Cu片和一定量浓H2SO4放在圆底烧瓶中共热,至反应结束后,发现烧瓶中还有少量Cu剩余,有人认为还有一定量的H2SO4剩余,原因是
,在不增加浓H2SO4的前提下,若使剩余铜片溶解可再加入 (填写两种属于不同类别的物质)。
(2)向反应后的溶液中加入足量的CuO,使剩余的H2SO4全部转化为CuSO4,过滤后将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4·XH2O)某小组同学采用加热法测定该晶体里结晶水X的值;
①在他们的实验操作中至少称量 次。
②下面是其中一次实验的数据
| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.6g |
根据上表数据计算判断x的实测值比理论值(x=5) (填“偏大”或“偏小”)。
(3)装置乙的作用是: ;
(4)下列说法正确的是: (填序号)。
a.甲装置使用的玻璃仪器有:酒精灯、玻璃管、长颈漏斗、圆底烧瓶
b.KMnO4溶液用于尾气处理
c.当把品红溶液滴入到锥形瓶中,若品红不褪色,说明无NaHSO3产生
d.当把品红溶液滴入到锥形瓶中,若品红褪色,说明NaOH已完全转化为NaHSO3
e.若把品红溶液换成酸性高锰酸钾溶液,并滴入到锥形瓶中,不显紫红色,说明NaOH已完全转化为NaHSO3
f.此装置换上其它药品后,不能制取和收集少量纯净的氯气
查看习题详情和答案>>