摘要:SO2的漂白性与氧化性无关.5.H2S03酸性比H2C03强.SO2通到NaHCO3溶液中发生化学反应:SO2+2NaHC3=Na2SO3+2C02+H20.除去SO2.将气体干燥后再通过加热的铜网除02.6.由氧化还原反应规律知:H2SeO4的氧化性强于Cl2.亚硒酸的氧化性强于亚硫酸.A.C均错.而D中物质的量关系错误.7.此反应过氧化氢中被氧化成氧气.8.用“电子守恒法 解题.9.从反应现象可知:单质的氧化性Br2>I2>S.则还原性S2-> I-> Br-.元素的非金属性Br>I>S.10.与Na化合时.硫显-2价.氯显-1价这与元素原子的最外层电子数有关.与非金属性无关.
网址:http://m.1010jiajiao.com/timu_id_3777761[举报]
Ⅰ:某兴趣小组欲在绿色环保的条件下探究大气污染物SO2的性质,设计如图实验装置.请回答:
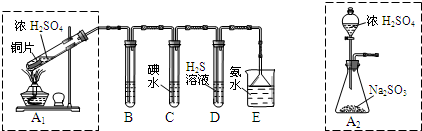
(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为 ;C中反应的离子方程式为 .
(2)为了实现绿色环保的目标,某同学设计了上图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是 (写2点).
Ⅱ:用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO
、SO
、HSO
等阴离子.请回答:
(3)氨水吸收过量SO2的反应的离子方程式为 .
(4))已知亚硫酸氢盐一般易溶于水,SO2也易溶于水.现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、2mol/L HNO3、1mol/L BaCl2溶液、1mol/L Ba(OH)2溶液、品红溶液、蒸馏水.请设计实验证明“吸收液”中存在SO
、HSO
,完成下表的实验操作、预期现象和结论:
查看习题详情和答案>>

(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为
(2)为了实现绿色环保的目标,某同学设计了上图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是
Ⅱ:用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO
2- 3 |
2- 4 |
- 3 |
(3)氨水吸收过量SO2的反应的离子方程式为
(4))已知亚硫酸氢盐一般易溶于水,SO2也易溶于水.现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、2mol/L HNO3、1mol/L BaCl2溶液、1mol/L Ba(OH)2溶液、品红溶液、蒸馏水.请设计实验证明“吸收液”中存在SO
2- 3 |
- 3 |
| 实验操作 | 预期现象与结论 | ||||
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取1mol/L BaCl2溶液向小烧杯滴加直至过量. | 若出现白色浑浊,则溶液中存在 SO
| ||||
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体 |
|||||
| 步骤3: |
(2013?广东模拟)SO2是一种大气污染物,某兴趣小组欲探究SO2的性质及绿色实验方法,设计如下方案:

(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性.其中C、D分别为碘水和硫化氢的水溶液,则B中所盛试剂为
(2)为了实现绿色实验的目标,某同学重新设计了如图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是:
(3)E中用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO32-、SO42-、HSO3-等阴离子.已知亚硫酸氢盐一般易溶于水,SO2也易溶于水.现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、2mol/L HNO3、1mol/L BaCl2溶液、1mol/L Ba(OH)2溶液、品红溶液、蒸馏水.请设计实验证明“吸收液”中存在SO32-和HSO3-,完成下表的实验操作、预期现象和结论:
查看习题详情和答案>>

(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性.其中C、D分别为碘水和硫化氢的水溶液,则B中所盛试剂为
品红溶液
品红溶液
,C中反应的离子方程式为:SO2+I2+2H2O=SO42-+2I-+4H+
SO2+I2+2H2O=SO42-+2I-+4H+
.(2)为了实现绿色实验的目标,某同学重新设计了如图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是:
①不用加热,安全性能高.②易于控制反应进行,反应更充分.
①不用加热,安全性能高.②易于控制反应进行,反应更充分.
(任写一点即可).(3)E中用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO32-、SO42-、HSO3-等阴离子.已知亚硫酸氢盐一般易溶于水,SO2也易溶于水.现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、2mol/L HNO3、1mol/L BaCl2溶液、1mol/L Ba(OH)2溶液、品红溶液、蒸馏水.请设计实验证明“吸收液”中存在SO32-和HSO3-,完成下表的实验操作、预期现象和结论:
| 实验操作 | 预期现象与结论 |
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取1mol/L BaCl2溶液向小烧杯滴加直至过量. | 若出现白色浑浊,则溶液中存在SO32-或 SO42-. |
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体 滴入1滴(或少量)品红 滴入1滴(或少量)品红 再滴入过量2mol/L盐酸,振荡 再滴入过量2mol/L盐酸,振荡 . |
若品红褪色(或有气泡),则“吸收液”中存在 SO32-. 若品红褪色(或有气泡),则“吸收液”中存在 SO32-. 若品红不褪色(或无有气泡),则“吸收液”中不存在 SO32- 若品红不褪色(或无有气泡),则“吸收液”中不存在 SO32- |
| 步骤3: 用试管取适量滤液 用试管取适量滤液 向其中滴入过量的1mol/LBa(OH)2溶液[或滴入1滴(或少量)品红溶液,再滴入2-3滴(或过量)的2mol/L盐酸],振荡 向其中滴入过量的1mol/LBa(OH)2溶液[或滴入1滴(或少量)品红溶液,再滴入2-3滴(或过量)的2mol/L盐酸],振荡 . |
若出现白色沉淀(或品红溶液褪色,或有气泡),则“吸收液”中存在 HSO3-. 若出现白色沉淀(或品红溶液褪色,或有气泡),则“吸收液”中存在 HSO3-. 若不出现白色沉淀(或品红溶液不褪色,或没有气泡),则“吸收液”中不存在 HSO3-. 若不出现白色沉淀(或品红溶液不褪色,或没有气泡),则“吸收液”中不存在 HSO3-. |