网址:http://m.1010jiajiao.com/timu_id_3777164[举报]
A.用托盘天平称量50.56 g氯化钾
B.用50 mL量筒量取5.0 mL稀H2SO4
C.用碱式滴定管量取18.5 mL 1 mol·L-1的NaOH溶液
D.用250 mL容量瓶配制200 mL 0.1 mol·L-1的Na2CO3溶液
E.欲在烧杯中加热配制50 mL某溶液,应选用的烧杯规格是250 mL
F.用50 mL酸式滴定管量取25 mL稀盐酸的操作是:将盐酸加入酸式滴定管使其凹液面正好与25 mL刻度相切,将溶液全部放入烧杯,可准确量取25 mL稀盐酸
G.用pH试纸检验溶液酸碱性的操作是:先取一块试纸放在表面皿或玻璃片上,用沾有待测液的玻璃棒点在试纸中部,观察颜色的改变并在半分钟内与标准比色卡对比,确定溶液的pH
(2)请选用下列试剂:酚酞、石蕊、稀氨水、氯化铵溶液、浓盐酸、熟石灰粉末、醋酸铵晶体和蒸馏水,设计实验证明NH3·H2O在水中存在电离平衡,请简述实验方法及现象。
查看习题详情和答案>>⑴下列实验不能达到预期目的的是( )
A. 用托盘天平称量50.56 g氯化钾
B. 用50 mL量筒取5.0 mL稀H2SO4
C. 用碱式滴定管量取18.5 mL 1 mol•L-1的NaOH溶液
D. 用250 mL容量瓶配制200 mL 0.1 mol•L-1的Na2CO3溶液
E. 欲在烧杯中加热配制50 mL某溶液,应选用的烧杯规格是250 mL
F. 用50 mL酸式滴定管量取25 mL稀盐酸的操作是:将盐酸加入酸式滴定管使其凹液面正好与25 mL刻度相切,将溶液全部放入烧杯,可准确量取25 mL稀盐酸
G.. 用pH试纸检验溶液酸碱性的操作是,先取一块试纸放在表面皿或玻璃片上,用沾有待测液的玻璃棒点在试纸中部,观察颜色的改变并在半分钟内与标准比色卡对比,确定溶液的pH
⑵请选用下列试剂:酚酞、石蕊、稀氨水、氯化铵溶液、浓盐酸、熟石灰粉末、醋酸铵晶体和蒸馏水,设计实验证明NH3•H2O在水中存在电离平衡,请简述实验方法及现象。
查看习题详情和答案>>
A. 用托盘天平称量50.56 g氯化钾
B. 用50 mL量筒取5.0 mL稀H2SO4
C. 用碱式滴定管量取18.5 mL 1 mol•L-1的NaOH溶液
D. 用250 mL容量瓶配制200 mL 0.1 mol•L-1的Na2CO3溶液
E. 欲在烧杯中加热配制50 mL某溶液,应选用的烧杯规格是250 mL
F. 用50 mL酸式滴定管量取25 mL稀盐酸的操作是:将盐酸加入酸式滴定管使其凹液面正好与25 mL刻度相切,将溶液全部放入烧杯,可准确量取25 mL稀盐酸
G.. 用pH试纸检验溶液酸碱性的操作是,先取一块试纸放在表面皿或玻璃片上,用沾有待测液的玻璃棒点在试纸中部,观察颜色的改变并在半分钟内与标准比色卡对比,确定溶液的pH
⑵请选用下列试剂:酚酞、石蕊、稀氨水、氯化铵溶液、浓盐酸、熟石灰粉末、醋酸铵晶体和蒸馏水,设计实验证明NH3•H2O在水中存在电离平衡,请简述实验方法及现象。
查看习题详情和答案>>
 常温下有下列四种溶液:
常温下有下列四种溶液:| ① | ② | ③ | ④ | |
| 溶液 | pH=4的NH4Cl | pH=4的盐酸 | 0.1mol?L-1的醋酸 | 0.1mol?L-1的NaOH |
(1)用④的标准液滴定③宜选用
(2)将②③④三种溶液分别加水稀释10倍,pH变化最小的是
(3)在溶液①中加入少量镁粉,可闻到一股刺激性气味.该反应的离子方程式为
(4)取适量溶液③滴定20mL溶液④,滴定曲线如图所示,则a点时溶液中各离子浓度的大小关系为
①蓝色石蕊试纸(检验气体性质)
②容量瓶
③托盘天平
(2)下列有关化学实验操作中“先”与“后”的说法正确的是
A.用排水法收集气体后,先移出导管,后熄灭酒精灯
B.点燃可燃性气体(如CH4、H2、CO等)时,都要先检验气体纯度,后点燃
C.碱液流到桌子上,先用稀醋酸溶液中和,后用水洗
D.给试管加热时,先均匀加热,后局部加热
II.实验室利用SO2和一定浓度的NaOH溶液反应制备少量NaHSO3.实验装置如图所示:
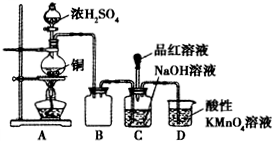
请回答下列问题:
(1)写出圆底烧瓶中发生反应的化学方程式
| ||
| ||
(2)反应结束后发现烧瓶中还有少量的铜片剩余,有人认为还有一定的硫酸剩余,原因是
(3)装置B的作用是
(4)证明C装置中NaOH溶液全部转化为NaHSO3的实验操作和现象是