网址:http://m.1010jiajiao.com/timu_id_3773249[举报]
(1)下列反应中,属于吸热反应的是______(填选项序号).a.Ba(OH)2?8H2O与NH4Cl混合搅拌 b.生石灰加入水中c.盐酸与NaOH溶液反应 d.H2在O2中燃烧
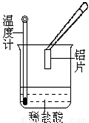
(2)某同学进行如右图所示实验,测量铝与盐酸反应中的能量变化.实验表明:反应温度升高,由此判断铝与盐酸反应是______(填“吸热”或“放热”)反应,其离子方程式是______,其中还原剂是______(填化学式).
(3)电能是现代社会应用最广泛的能源之一.下图所示为锌、铜和稀硫酸组成的原电池,其负极是______,正极的电极反应式是______.若电路中有1mol电子转移,则在标准状况下产生H2的体积为______L.


(1)下列反应中,属于吸热反应的是______(填选项序号).a.Ba(OH)2?8H2O与NH4Cl混合搅拌 b.生石灰加入水中c.盐酸与NaOH溶液反应 d.H2在O2中燃烧
(2)某同学进行如右图所示实验,测量铝与盐酸反应中的能量变化.实验表明:反应温度升高,由此判断铝与盐酸反应是______(填“吸热”或“放热”)反应,其离子方程式是______,其中还原剂是______(填化学式).
(3)电能是现代社会应用最广泛的能源之一.下图所示为锌、铜和稀硫酸组成的原电池,其负极是______,正极的电极反应式是______.若电路中有1mol电子转移,则在标准状况下产生H2的体积为______L.

 查看习题详情和答案>>
查看习题详情和答案>>
 能源是现代社会发展的支柱之一,化学能是重要的能源.
能源是现代社会发展的支柱之一,化学能是重要的能源.(1)下列反应中,属于吸热反应的是
(2)某同学进行如右图所示实验,测量铝与盐酸反应中的能量变化.实验表明:反应温度升高,由此判断铝与盐酸反应是
(3)电能是现代社会应用最广泛的能源之一.下图所示为锌、铜和稀硫酸组成的原电池,其负极是

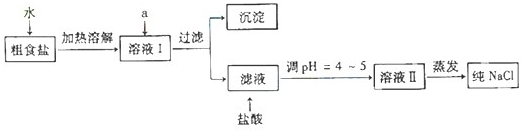
(1)粗食盐常含有少量Ca2+、Mg2+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液
①欲除去溶液Ⅰ中的Ca2+、Mg2+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为
②过滤之前,怎样检验SO42-已除去:
③过滤所需要的玻璃仪器有
④若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是
(2)用提纯的NaCl配制250mL 2.00mol?L-1NaCl溶液.
①所用仪器除药匙及上面过滤涉及到的外,还有
②计算后,需称出NaOH质量为
③下列操作的正确顺序是(用字母表示)
A.摇匀 B.称量 C.洗涤 D.定容 E.溶解 F.移液 G.装瓶
④下列操作对所得溶液浓度有何影响,在横线上填写“偏高”“偏低”或“无影响”.
A 定容时仰视容量瓶刻度线:
(1)航天技术上使用的氢―氧燃料电池具有高能、轻便和不污染环境等优点。氢―氧燃料电池有酸式和碱式两种,它们放电时的电池总反应为: 2H2 + O2 = 2 H2O 。酸式氢―氧燃料电池的电解质是酸,其负极反应可表示为: 2H2 4e- = 4 H+,其正极反应表示为___________ ;碱式氢―氧燃料电池中的电解质是碱,其正极反应表示为: O2 +2H2O+4e-=4OH-,则其负极反应可表示为:
(2)铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,正极板上覆盖PbO2,
负极板上覆盖Pb,电解质是硫酸。电池总反应式为:
Pb+PbO2+4H++2SO42-![]() 2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题(不考虑氢、氧的氧化还原):
放电时:正极的电极反应式是__________________________
充电时:阴极的电极反应式是
(3)现代工业上主要采用离子交换膜法电解饱和食盐水制取H2、Cl2、NaOH。请
回答下列问题:
①该过程总的离子反应方程式为:
电解之前,食盐水需要精制,目的是除去粗盐中的Ca2+、Mg2+、SO42-等杂质离子,使
用的试剂有:a.Na2CO3溶液,b.Ba(OH)2溶液,c.稀盐酸, 其合理的加入顺序为
_________________(填试剂序号)。
②离子交换膜的作用是 。
 ③现设计一电解装置如右图,用离子交换膜A和B将电解槽分为I、II、
③现设计一电解装置如右图,用离子交换膜A和B将电解槽分为I、II、
Ⅲ三个区域,A为“阳离子交换膜”,它有一特殊的功能――只允许阳
离子通过,但阻止阴离子和气体通过,而B是“阴离子交换膜”,它只
允许阴离子通过,可阻止阳离子和气体通过,电极均为惰性电极。若在I区投入Na2SO4
溶液,通电电解。阴极的电极反应式为_____________________________,
查看习题详情和答案>>