摘要:MgCl2水溶液加热蒸发结晶后的最终产物为MgO.从而有FeCl2水溶液加热蒸发结晶后的最终产物为FeO. 错因:没有考虑到FeCl2水解过程中生成的Fe(OH)2要与空气中的O2反应生成Fe(OH)3. 实际应为:Fe2O3
网址:http://m.1010jiajiao.com/timu_id_3768932[举报]
海水是宝贵的自然资源,从海水中可以提取多种化工原料,某工厂对海水综合利用的示意图如下所示:
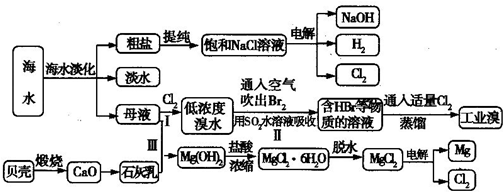
(1)在粗盐中含有SO42-、Ca2+、Mg2+等杂质,电解精制时所用的试剂有①盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液,则加入试剂的先后顺序是
(2)工业上电解饱和食盐水的离子方程式为
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是
步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,写出有关反应的离子方程式:
(4)从步骤Ⅲ得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是向沉淀中加入
(5)在制取无水氯化镁时需要在干燥的HCl气流中加热MgCl2?6H20的原因:
(6)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气冷却剂的是
A.H2 B.CO2 C.空气 D.O E.水蒸气.
查看习题详情和答案>>

(1)在粗盐中含有SO42-、Ca2+、Mg2+等杂质,电解精制时所用的试剂有①盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液,则加入试剂的先后顺序是
②④③①或③②④①或②③④①
②④③①或③②④①或②③④①
(填编号).(2)工业上电解饱和食盐水的离子方程式为
2Cl-+2H2O
Cl2↑+H2↑+2OH-
| ||
2Cl-+2H2O
Cl2↑+H2↑+2OH-
.
| ||
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是
富集溴元素;
富集溴元素;
.步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,写出有关反应的离子方程式:
Br2+SO2+2H2O=4H++SO42-+2Br-
Br2+SO2+2H2O=4H++SO42-+2Br-
.(4)从步骤Ⅲ得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是向沉淀中加入
氯化镁
氯化镁
溶液,充分搅拌后经过滤
过滤
(填操作方法)可得纯净的Mg(OH)2.(5)在制取无水氯化镁时需要在干燥的HCl气流中加热MgCl2?6H20的原因:
在干燥的HCl气流中,抑制了MgCl2水解,且带走MgCl2?6H2O受热产生的水汽,故能得到无水MgCl2
在干燥的HCl气流中,抑制了MgCl2水解,且带走MgCl2?6H2O受热产生的水汽,故能得到无水MgCl2
.(6)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气冷却剂的是
A
A
(填序号).A.H2 B.CO2 C.空气 D.O E.水蒸气.
甲、乙、丙、丁四种易溶于水的物质在水溶液中分别电离出N
、Ba2+、Mg2+、H+、OH-、Cl-、HC
、S
中的不同阳离子和阴离子,已知:
①甲溶液分别与其他三种溶液混合,均有白色沉淀生成;
②0.1mol/L 乙溶液中c(H+)=0.2mol/L;
③向丙溶液中滴入AgNO3溶液,有不溶于稀HNO3的白色沉淀生成.
请回答下列问题:
(1)丙的电离方程式为
(2)丙中阴离子结构示意图为

(3)加热丁的固体生成三种气体,其化学方程式为
(4)甲、乙反应的离子方程式为
(5)乙、丁反应的离子方程式为
(6)甲、丁以物质的量比1:1反应的离子方程式为
查看习题详情和答案>>
| H | + 4 |
| O | - 3 |
| O | 2- 4 |
①甲溶液分别与其他三种溶液混合,均有白色沉淀生成;
②0.1mol/L 乙溶液中c(H+)=0.2mol/L;
③向丙溶液中滴入AgNO3溶液,有不溶于稀HNO3的白色沉淀生成.
请回答下列问题:
(1)丙的电离方程式为
MgCl2═Mg2++2Cl-
MgCl2═Mg2++2Cl-
(2)丙中阴离子结构示意图为


(3)加热丁的固体生成三种气体,其化学方程式为
NH4HCO3
NH3↑+CO2↑+H2O
| ||
NH4HCO3
NH3↑+CO2↑+H2O
| ||
(4)甲、乙反应的离子方程式为
Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O
Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O
(5)乙、丁反应的离子方程式为
HCO3-+H+═H2O+CO2↑
HCO3-+H+═H2O+CO2↑
(6)甲、丁以物质的量比1:1反应的离子方程式为
Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3↑+2H2O
Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3↑+2H2O
.海水是人类宝贵的自然资源,从海水中可以提取多种化工原料,下图是某工厂对海水资源综合利用的示意图:

(1)请列举海水淡化的两种方法
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是:
(3)在制取无水氯化镁时需要在干躁的HCl气流中加热MgCl2?6H2O的原因
(4)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用做镁蒸气的冷却剂的是
A.H2 B.CO2 C.空气 D.O2 E.水蒸气
(5)从各种经营综合开发,打造大而强的现代企业以及本厂生产所需要的原料等方面来看,你认为该化工厂还可以再增加的生产项目的
(6)上述工艺中可以得到金属Mg,请写出工业上制备金属铝的化学方程式
查看习题详情和答案>>

(1)请列举海水淡化的两种方法
蒸馏法
蒸馏法
、电渗析法
电渗析法
.(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是:
富集溴元素
富集溴元素
.步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式Br2+SO2+2H2O=4H++SO42-+2Br-
Br2+SO2+2H2O=4H++SO42-+2Br-
(3)在制取无水氯化镁时需要在干躁的HCl气流中加热MgCl2?6H2O的原因
在干燥的HCl气流中,抑制了MgCl2水解,且带走MgCl2?6H2O受热产生的水汽,故能得到无水MgCl2
在干燥的HCl气流中,抑制了MgCl2水解,且带走MgCl2?6H2O受热产生的水汽,故能得到无水MgCl2
(4)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用做镁蒸气的冷却剂的是
A
A
A.H2 B.CO2 C.空气 D.O2 E.水蒸气
(5)从各种经营综合开发,打造大而强的现代企业以及本厂生产所需要的原料等方面来看,你认为该化工厂还可以再增加的生产项目的
建一个盐酸厂
建一个盐酸厂
.(6)上述工艺中可以得到金属Mg,请写出工业上制备金属铝的化学方程式
2Al2O3(熔融)
4Al+3O2↑
| ||
2Al2O3(熔融)
4Al+3O2↑
.
| ||
(2013?哈尔滨模拟)[化学--选修化学与技术]
沿海地区有着丰富的海水资源,海水占地球总储水量的97.4%,海水是人类宝贵的自然资源,若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海水资源,从海水中可以提取多种化工原料,如图是某工厂对海水资源综合利用的示意图:
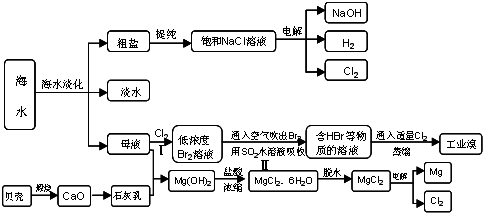
(1)请列举海水淡化的两种方法
(2)使用离子交换树脂与水中的离子进行交换也是常用的水处理技术.聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br -,其目的是:
步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式
(4)在制取无水氯化镁时需要在干躁的HCl气流中加热MgCl2.6H2O的原因
(5)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用做镁蒸气的冷却剂的是
A.H2 B.CO2 C.空气 D.O2 E.水蒸气
(6)苦卤(海水蒸发结晶分离出食盐后的母液)中含有较多的NaCl、MgCl2、KCl、MgSO4等物质.用沉淀法测定苦卤中MgCl2的含量(g/L),测定过程中应获取的数据有
查看习题详情和答案>>
沿海地区有着丰富的海水资源,海水占地球总储水量的97.4%,海水是人类宝贵的自然资源,若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海水资源,从海水中可以提取多种化工原料,如图是某工厂对海水资源综合利用的示意图:

(1)请列举海水淡化的两种方法
蒸馏法
蒸馏法
、电渗析法
电渗析法
.(2)使用离子交换树脂与水中的离子进行交换也是常用的水处理技术.聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式
CH2=CHCOONa
CH2=CHCOONa
.(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br -,其目的是:
富集溴元素
富集溴元素
.步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式
Br2+SO2+2H2O═4H++SO2-4+2Br-
Br2+SO2+2H2O═4H++SO2-4+2Br-
(4)在制取无水氯化镁时需要在干躁的HCl气流中加热MgCl2.6H2O的原因
在干燥的HCl气流中,抑制了MgCl2水解,且带走MgCl2,6H2O受热产生的水汽,故能得到无水MgCl2
在干燥的HCl气流中,抑制了MgCl2水解,且带走MgCl2,6H2O受热产生的水汽,故能得到无水MgCl2
.(5)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用做镁蒸气的冷却剂的是
A
A
A.H2 B.CO2 C.空气 D.O2 E.水蒸气
(6)苦卤(海水蒸发结晶分离出食盐后的母液)中含有较多的NaCl、MgCl2、KCl、MgSO4等物质.用沉淀法测定苦卤中MgCl2的含量(g/L),测定过程中应获取的数据有
苦卤样品体积、加入NaOH溶液后生成Mg(OH)2的质量、加入BaCl2溶液后生成BaSO4的质量
苦卤样品体积、加入NaOH溶液后生成Mg(OH)2的质量、加入BaCl2溶液后生成BaSO4的质量
.