摘要:21.0.4≤a≤1.3
网址:http://m.1010jiajiao.com/timu_id_3756602[举报]
A、B、C三个烧杯中分别盛有200mL相同物质的量浓度的稀硫酸

(1)A中反应的离子方程式为
(2)一段时间后,B中Sn极附近溶液的pH
(3)一段时间后,C中产生了3.36L(标准状况)气体时,硫酸恰好全部被消耗,则原稀硫酸溶液的物质的量浓度=
(4)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是
查看习题详情和答案>>

(1)A中反应的离子方程式为
Fe+2H+=Fe2++H2↑
Fe+2H+=Fe2++H2↑
.(2)一段时间后,B中Sn极附近溶液的pH
增大
增大
(填“增大”、“减小”、“不变”).(3)一段时间后,C中产生了3.36L(标准状况)气体时,硫酸恰好全部被消耗,则原稀硫酸溶液的物质的量浓度=
0.75
0.75
mol?L-1.(4)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是
BAC
BAC
(填写序号).A、B、C、D、E五种溶液分别是NaOH、NH3?H2O、CH3COOH、HCl、NH4HSO4中的一种.常温下进行下列实验:
①将1L pH=3的A溶液分别与0.001mol/L x L B溶液、0.001mol/L y L D溶液充分反应至中性,x、y的大小关系式y<x;
②浓度均为0.1mol/L A和E溶液,pH:A<E
③浓度均为0.1mol/L C和D溶液等体积混合,溶液呈酸性.
回答下列问题:
(1)C是
(2)用水稀释0.1mol/L B溶液时,溶液中随水量的增加而减小的是
A.
B.
C.c (H+)?c (OH-) D.n (OH-)
(3)等pH、等体积的两份溶液A和E,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出的氢气的质量相同.则
(4)常温下,向0.01mol/L C溶液中滴加0.01mol/L D溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为
(5)已知常温下Mg(OH)2在pH=12的D溶液中Mg2+的浓度为1.8×10-7mol/L,则 Ksp[Mg(OH)2]=
查看习题详情和答案>>
①将1L pH=3的A溶液分别与0.001mol/L x L B溶液、0.001mol/L y L D溶液充分反应至中性,x、y的大小关系式y<x;
②浓度均为0.1mol/L A和E溶液,pH:A<E
③浓度均为0.1mol/L C和D溶液等体积混合,溶液呈酸性.
回答下列问题:
(1)C是
NH4HSO4
NH4HSO4
溶液,D是NaOH
NaOH
溶液.(2)用水稀释0.1mol/L B溶液时,溶液中随水量的增加而减小的是
AB
AB
.A.
| c(B) |
| c(OH-) |
| c(OH-) |
| c(H+) |
(3)等pH、等体积的两份溶液A和E,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出的氢气的质量相同.则
HCl
HCl
(填化学式)溶液中锌粉有剩余.(4)常温下,向0.01mol/L C溶液中滴加0.01mol/L D溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为
c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-)
c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-)
.(5)已知常温下Mg(OH)2在pH=12的D溶液中Mg2+的浓度为1.8×10-7mol/L,则 Ksp[Mg(OH)2]=
1.8×10-11(mol/L)3
1.8×10-11(mol/L)3
.A、B、C、D为同一周期的四种元素,原子序数依次增大,已知0.2摩A与酸充分反应时,在标况下可生成2.24升氢气;B的氧化物既可溶于强酸又可溶于强碱溶液;C、D阴离子的电子层结构与氩原子相同,C的气态氢化物与C的低价氧化物反应,又可得到C的单质.试回答:
(1)A、B、C、D的元素符号分别为
(2)用电子式表示A与C形成化合物的过程:
 .
.
(3)写出B的氧化物与A的氢氧化物反应的离子方程式:
(4)写出实验室制备D的单质的化学反应方程式:
查看习题详情和答案>>
(1)A、B、C、D的元素符号分别为
Na
Na
、Al
Al
、S
S
、Cl
Cl
.(2)用电子式表示A与C形成化合物的过程:


(3)写出B的氧化物与A的氢氧化物反应的离子方程式:
Al2O3+2OH-=AlO-+H2O
Al2O3+2OH-=AlO-+H2O
.(4)写出实验室制备D的单质的化学反应方程式:
MnO2+4HCl(浓)
MnCl2+Cl2↑+H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+H2O
.
| ||
A、B、C、D、E五种元素,它们的质子数依次递增,但都小于18.A元素原子核外只有1个电子.B元素原子和C元素原子最外层电子数之差为2.B元素原子最外层上的电子数为次外层电子数的2倍.B、C、D三种元素可以形成化学式为D2BC3的化合物,其焰色反应为黄色.0.5mol E元素的单质与足量的酸反应有9.03×1023个电子发生转移.在E和C的化合物中,E的质量占52.94%,又已知E的原子核中有14个中子.
(1)以下三种元素分别是:
A
(2)画出D原子结构示意图、E阳离子结构示意图
(3)写出A2C、BC2、D2C2的电子式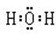
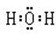 、
、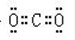
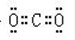 、
、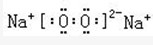
 .
.
(4)写出D2C2与A2C反应的化学方程式
查看习题详情和答案>>
(1)以下三种元素分别是:
A
氢H
氢H
,B碳C
碳C
,C氧O
氧O
.(2)画出D原子结构示意图、E阳离子结构示意图
Na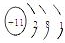
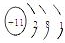
Na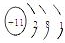
、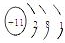
Al3+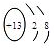
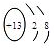
Al3+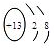
.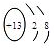
(3)写出A2C、BC2、D2C2的电子式
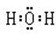
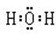
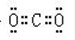
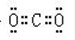


(4)写出D2C2与A2C反应的化学方程式
2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑
.A、B、C、D四种元素原子的核电荷数依次增大(均小于20),其单质及相应的化合物能发生如下反应关系:

(1)写出F的电子式
 .
.
(2)气体H有毒,可用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为:
(3)加热E的水溶液后并灼烧,最终得到的固体为
(4)室温下,向F的水溶液中加入等体积等浓度的盐酸反应后所得溶液的PH>7,则此溶液中离子浓度由小到大的顺序为:
(5)将气体H放在空气中充分燃烧可得到气体氧化物BO2,BO2可与氧气继续反应:2BO2+O2 2BO3,在一个固定容积为2L的密闭容器中充入0.20mol的BO2和0.10mol的O2,半分钟后达到平衡,测得容器中含BO3为0.18mol,则v(o2 )=
2BO3,在一个固定容积为2L的密闭容器中充入0.20mol的BO2和0.10mol的O2,半分钟后达到平衡,测得容器中含BO3为0.18mol,则v(o2 )=
查看习题详情和答案>>

(1)写出F的电子式


(2)气体H有毒,可用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为:
H2S+Na2CO3=NaHS+NaHCO3
H2S+Na2CO3=NaHS+NaHCO3
.(3)加热E的水溶液后并灼烧,最终得到的固体为
Al2O3
Al2O3
,原因为AlCl3+3H2O?Al(OH)3+3HCl
AlCl3+3H2O?Al(OH)3+3HCl
,2Al(OH)3
Al2O3+2H2O
| ||
2Al(OH)3
Al2O3+2H2O
.(用化学反应方程式来表示)
| ||
(4)室温下,向F的水溶液中加入等体积等浓度的盐酸反应后所得溶液的PH>7,则此溶液中离子浓度由小到大的顺序为:
[S2-]<[H+]<[OH-]<[HS-]<[Cl-]<[K+]
[S2-]<[H+]<[OH-]<[HS-]<[Cl-]<[K+]
.(5)将气体H放在空气中充分燃烧可得到气体氧化物BO2,BO2可与氧气继续反应:2BO2+O2
 2BO3,在一个固定容积为2L的密闭容器中充入0.20mol的BO2和0.10mol的O2,半分钟后达到平衡,测得容器中含BO3为0.18mol,则v(o2 )=
2BO3,在一个固定容积为2L的密闭容器中充入0.20mol的BO2和0.10mol的O2,半分钟后达到平衡,测得容器中含BO3为0.18mol,则v(o2 )=0.09
0.09
mol?L-1?min-1.若继续通入0.20mol BO2和0.10mol O2,再次达到新平衡后,BO3的物质的量介于0.36mol和0.40mol
0.36mol和0.40mol
之间.