摘要:8.用物质的量浓度均是0.1mol·L-1的CH3COOH和CH3COONa配成1L溶液.c(Na+) <c(CH3COO-)下列判断正确的是( ) A.c(OH-)<c(H+) B.c(CH3COOH)+c(CH3COO-)=0.2mol·L-1 C.c(CH3COOH)>c(CH3COO-) D.c(CH3COO-)+c(OH-)=0.1mol·L-1
网址:http://m.1010jiajiao.com/timu_id_3755323[举报]
(1)下列盐溶液中能发生水解的用离子方程式表示,不能发生水解的请写上“不发生水解”字样,并说明溶液的酸碱性:
K2CO3
K2SO4
NH4Cl
(2)物质的量浓度均为0.1mol/L的下列溶液:①KNO3、②Na2CO3、③NaHCO3、④NaHSO4、⑤CH3COOH、⑥NaOH、⑦Ba(OH)2、⑧NH4Cl,pH由大到小的顺序为:
(3)现有常温下的0.1mol?L-1 Na2CO3溶液:
①你认为该溶液呈碱性的原因是(用离子方程式表示)
②为证明你的上述观点,请设计一个简单的实验,简述实验过程
查看习题详情和答案>>
K2CO3
CO32-+H2O?HCO3-+OH-
CO32-+H2O?HCO3-+OH-
,溶液呈碱
碱
性;K2SO4
不发生水解
不发生水解
,溶液呈中性
中性
性;NH4Cl
NH4++H2O?NH3?H2O+H+
NH4++H2O?NH3?H2O+H+
,溶液呈酸
酸
性.(2)物质的量浓度均为0.1mol/L的下列溶液:①KNO3、②Na2CO3、③NaHCO3、④NaHSO4、⑤CH3COOH、⑥NaOH、⑦Ba(OH)2、⑧NH4Cl,pH由大到小的顺序为:
⑦>⑥>②>③>①>⑧>⑤>④
⑦>⑥>②>③>①>⑧>⑤>④
(填数字代号)(3)现有常温下的0.1mol?L-1 Na2CO3溶液:
①你认为该溶液呈碱性的原因是(用离子方程式表示)
CO32-+H2O?HCO3-+OH-
CO32-+H2O?HCO3-+OH-
;②为证明你的上述观点,请设计一个简单的实验,简述实验过程
向Na2CO3溶液中加酚酞试液,溶液变红色,说明溶液显碱性,证明Na2CO3水解
向Na2CO3溶液中加酚酞试液,溶液变红色,说明溶液显碱性,证明Na2CO3水解
.甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动.实验方案如下:
甲:取纯度相同,质量、大小相等的锌粒于两只试管中,同时加入0.1mol?L-1的 HA、HCl溶液各10mL,按图1装好,观察现象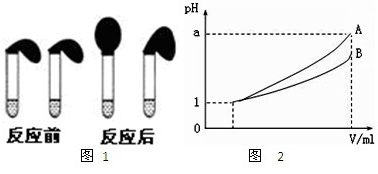
乙:①用pH计测定物质的量浓度均为0.1mol?L-1HA和HCl溶液的pH;
②再取0.1mol?L-1的HA和HCl溶液各2滴(1滴约为1/20mL)分别稀释至100mL,再用pH计测其pH变化
(1)乙方案中说明HA是弱电解质的理由是:测得0.1mol?L-1的HA溶液的pH
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后,试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第
A.NaA固体(可完全溶于水) B.1mol.L-2NaOH溶液 C.1mol.L-2H2SO2 D.2mol.L-2-HA
(3)pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图2所示,则下列说法不正确的有
A.两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸.
查看习题详情和答案>>
甲:取纯度相同,质量、大小相等的锌粒于两只试管中,同时加入0.1mol?L-1的 HA、HCl溶液各10mL,按图1装好,观察现象

乙:①用pH计测定物质的量浓度均为0.1mol?L-1HA和HCl溶液的pH;
②再取0.1mol?L-1的HA和HCl溶液各2滴(1滴约为1/20mL)分别稀释至100mL,再用pH计测其pH变化
(1)乙方案中说明HA是弱电解质的理由是:测得0.1mol?L-1的HA溶液的pH
>
>
1(填“>”、“<”或“=”);甲方案中,说明HA是弱电解质的实验现象是:B
B
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后,试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第
②
②
步,能证明改变条件弱电解质平衡发生移动.甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:①使HA的电离程度和C(H-)都减小,C(A-)增大,可在0.1mol.L-2的HA溶液中,选择加入A
A
试剂(选填“A”“B”“C”“D”.下同);②使HA的电离程度减小,C(H-)和C(A-)都增大,可在0.1mol.L-2的HA溶液中,选择加入D
D
试剂.A.NaA固体(可完全溶于水) B.1mol.L-2NaOH溶液 C.1mol.L-2H2SO2 D.2mol.L-2-HA
(3)pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图2所示,则下列说法不正确的有
A
A
A.两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸.
某化工厂用氯气与氢氧化钙生产漂白粉.该厂出厂产品说明书如下:

(1)漂白粉的有效成分是 (填化学式).
(2)化工生产中Cl2来源于电解食盐水.电解过程中,阳极反应为2Cl--2e-=Cl2↑,阴极反应为2H2O+2e-=2OH-+H2↑.则电解时阳极发生 (填“氧化”或“还原”)反应.
(3)生产漂白粉原理是(用化学方程式表示) .
(4)“密封避光保存于阴凉处,随用随配”是因为漂白粉有效成份与空气中CO2、H2O反应生成不稳定的次氯酸而易失效.生成次氯酸的化学方程式为 .
(5)某次配制中,取一定质量漂白粉溶解于1000g水中,所得溶液次氯酸钙和氯化钙的物质的量浓度均为0.01mol/L.假设漂白粉不含其它杂质,且所得溶液的体积仍为1L,则此次溶液配制中,所加漂白粉的质量为 g.
查看习题详情和答案>>

(1)漂白粉的有效成分是
(2)化工生产中Cl2来源于电解食盐水.电解过程中,阳极反应为2Cl--2e-=Cl2↑,阴极反应为2H2O+2e-=2OH-+H2↑.则电解时阳极发生
(3)生产漂白粉原理是(用化学方程式表示)
(4)“密封避光保存于阴凉处,随用随配”是因为漂白粉有效成份与空气中CO2、H2O反应生成不稳定的次氯酸而易失效.生成次氯酸的化学方程式为
(5)某次配制中,取一定质量漂白粉溶解于1000g水中,所得溶液次氯酸钙和氯化钙的物质的量浓度均为0.01mol/L.假设漂白粉不含其它杂质,且所得溶液的体积仍为1L,则此次溶液配制中,所加漂白粉的质量为
电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:
(1)已知25℃时,①HF(aq)+OH-(aq)=F-(aq)+H2O(l)△H=-67.7kJ/mol,②H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,氢氟酸的电离方程式及热效应可表示为 .
(2)将浓度为0.1mol/LHF溶液加水稀释一倍(假设温度不变),下列各量增大的是 .
A.c(H+) B.c(H+)?c(OH-) C.
D.
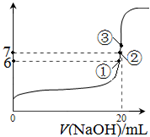
(3)25℃时,在20mL0.1mol/L氢氟酸中加入VmL0.1mol/LNaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是 .
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol/L
(4)物质的量浓度均为0.1mol/L的下列四种溶液:①Na2CO3溶液②NaHCO3溶液③NaF溶液④NaClO溶液.
依据数据判断pH由大到小的顺序是 .
(5)Na2CO3溶液显碱性是因为CO32-水解的缘故,请设计简单的实验事实证明之 .
(6)长期以来,一直认为氟的含氧酸不存在.1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H-O-F.HFO与水反应得到HF和化合物A,每生成1molHF转移 mol电子.
查看习题详情和答案>>
| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数 (Ka) |
7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 |
3.0×10-8 |
(2)将浓度为0.1mol/LHF溶液加水稀释一倍(假设温度不变),下列各量增大的是
A.c(H+) B.c(H+)?c(OH-) C.
| c(H+) |
| c(HF) |
| c(OH-) |
| c(H+) |

(3)25℃时,在20mL0.1mol/L氢氟酸中加入VmL0.1mol/LNaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol/L
(4)物质的量浓度均为0.1mol/L的下列四种溶液:①Na2CO3溶液②NaHCO3溶液③NaF溶液④NaClO溶液.
依据数据判断pH由大到小的顺序是
(5)Na2CO3溶液显碱性是因为CO32-水解的缘故,请设计简单的实验事实证明之
(6)长期以来,一直认为氟的含氧酸不存在.1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H-O-F.HFO与水反应得到HF和化合物A,每生成1molHF转移
 甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动.实验方案如下:
甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动.实验方案如下:甲:取纯度相同,质量、大小相等的锌粒于两只试管中,同时加入0.1mol?L-1的 HA、HCl溶液各10mL,按图1装好,观察现象;
乙:①用pH计测定物质的量浓度均为0.1mol?L-1HA和HCl溶液的pH;
②再取0.1mol?L-1的HA和HCl溶液各2滴(1滴约为
| 1 | 25 |
(1)乙方案中说明HA是弱电解质的理由是:测得0.1mol?L-1的HA溶液的pH
>
>
1(填“>”、“<”或“=”);甲方案中,说明HA是弱电解质的实验现象是:B
B
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后,试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第
②
②
步,能证明改变条件弱电解质平衡发生移动.甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:①使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1mol?L-1的HA溶液中,选择加入
A
A
试剂(选填“A”“B”“C”“D”,下同);②使HA的电离程度减小,c(H+)和c(A-)都增大,可在0.1mol?L-1的HA溶液中,选择加入
D
D
试剂.A.NaA固体(可完全溶于水)
B.1mol?L-1NaOH溶液
C.1mol?L-1H2SO4
D.2mol?L-1HA
(3)pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图2所示,则下列说法不正确的有
AE
AE
A.两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸
E.稀释后A溶液中水的电离程度比B溶液中水的电离程度小.