摘要:4.反应2E(g) 2F,ΔH>0达平衡时.要使逆反应速率增大.E的浓度降低.应采取的措施是 ( ) A.加压 B.减压 C.增加G的浓度 D.升温
网址:http://m.1010jiajiao.com/timu_id_3739705[举报]
 如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:①反应C+G
如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:①反应C+G| 高温 |
| ||
. |
(1)①中反映的化学方程式为
2Al+Fe2O3
2Fe+Al2O3
| ||
2Al+Fe2O3
2Fe+Al2O3
;
| ||
(2)化合物Ⅰ的电子式为
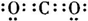
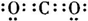
直线型
直线型
;(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量(写出离子方程式和计算过程);
(4)C与过量NaOH溶液反应的离子方程式为
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
,反应后溶液与过量化合物Ⅰ反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
;(5)E在I中燃烧观察到的现象是
镁条剧烈燃烧生成白色和黑色固体
镁条剧烈燃烧生成白色和黑色固体
.图中A、B、C、D、E为单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:
①C+G→B+H,放出大量的热,该反应曾应用于铁轨的焊接,G物质是磁铁矿的主要成分;
②I是一种常见的温室气体,它和E发生反应:2E+I→2F+D,F中E元素的质量分数为60%.

回答下列问题.
(1)反应①的化学方程式是 .
(2)化合物I中所存在的化学键是 键(填“离子”或“极性”或“非极性”).
(3)称取11.9g B、C、E的混合物,用过量的NaOH溶液溶解后,过滤、称量剩余固体质量为9.2g,另取等质量的B、C、E的混合物用足量的稀硝酸完全溶解,共收集到标况下气体6.72L,向剩余的混合液中加入过量的NaOH溶液,所得沉淀的质量为 .
A.27.2g B.7.8g C.2.7g D.19.4g
(4)C与过量的NaOH溶液反应的离子方程式是: .
(5)将G溶于过量的稀盐酸中,欲检验其中的Fe3+的方案是 (从下面的选项中选择正确选项,下同),欲检验其中的Fe2+的方案是 .
A.滴加KSCN溶液,溶液变血红色
B.加铁粉,溶液变浅绿色
C.滴入酸性KMnO4溶液,迅速褪色
D.滴加NaOH溶液,有白色沉淀且迅速变成灰绿色最后转化为红褐色.
查看习题详情和答案>>
①C+G→B+H,放出大量的热,该反应曾应用于铁轨的焊接,G物质是磁铁矿的主要成分;
②I是一种常见的温室气体,它和E发生反应:2E+I→2F+D,F中E元素的质量分数为60%.

回答下列问题.
(1)反应①的化学方程式是
(2)化合物I中所存在的化学键是
(3)称取11.9g B、C、E的混合物,用过量的NaOH溶液溶解后,过滤、称量剩余固体质量为9.2g,另取等质量的B、C、E的混合物用足量的稀硝酸完全溶解,共收集到标况下气体6.72L,向剩余的混合液中加入过量的NaOH溶液,所得沉淀的质量为
A.27.2g B.7.8g C.2.7g D.19.4g
(4)C与过量的NaOH溶液反应的离子方程式是:
(5)将G溶于过量的稀盐酸中,欲检验其中的Fe3+的方案是
A.滴加KSCN溶液,溶液变血红色
B.加铁粉,溶液变浅绿色
C.滴入酸性KMnO4溶液,迅速褪色
D.滴加NaOH溶液,有白色沉淀且迅速变成灰绿色最后转化为红褐色.
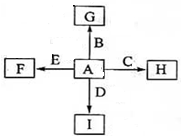 如图中,A、B、C、D、E是常见单质,G、H、I、F是B、C、D、E分别和A形成的化合物.已知:①反应2C+G
如图中,A、B、C、D、E是常见单质,G、H、I、F是B、C、D、E分别和A形成的化合物.已知:①反应2C+G
| ||
| ||
回答问题:
(1)①中反应的化学方程式为
(2)单质A的分子式为
(3)C与NaOH溶液反应的离子方程式为
 A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:
A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:①反应C+G
| 高温 |
②I是一种常见的温室气体,它和E可以发生反应:2E+I
| ||
(1)①中反应的化学方程式为
2Al+Fe2O3
Al2O3+2Fe
| ||
2Al+Fe2O3
Al2O3+2Fe
;
| ||
(2)化合物Ⅰ的电子式为


(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量
0.64g
0.64g
;(4)C与过量NaOH溶液反应的化学方程式为
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
,反应后溶液与过量化合物Ⅰ反应的化学方程式为AlO2-+CO2+2H2O=HCO3-+Al(OH)3↓
AlO2-+CO2+2H2O=HCO3-+Al(OH)3↓
;(5)E在I中燃烧可能观察到的现象是
镁条剧烈燃烧,生成白色粉末,反应器内壁附着有黑色的碳
镁条剧烈燃烧,生成白色粉末,反应器内壁附着有黑色的碳
. 如图所示中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:
如图所示中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:①反应C+G
| ||
②I是一种常见的温室气体,它和E可以发生反应:
2E+I
| ||
(1)①中反应的化学方程式为
2Al+Fe2O3
2Fe+Al2O3
| ||
2Al+Fe2O3
2Fe+Al2O3
;
| ||
(2)化合物I的电子式为
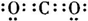
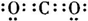
直线形
直线形
;(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量(写出离子方程式和计算过程).
(4)C与过量NaOH溶液反应的离子方程式为
2Al+2OH-+2H2O═2AlO2-+3H2↑
2Al+2OH-+2H2O═2AlO2-+3H2↑
,反应后溶液与过量化合物I反应的离子方程式为AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-
AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-
.