网址:http://m.1010jiajiao.com/timu_id_3736825[举报]
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
(1)目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作冷剂已成为一种趋势,这一做法对环境的积极意义在于 。
(2)将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
a.6CO2+6H2O  C6H12O6+6O2 b .CO2+3H2?
C6H12O6+6O2 b .CO2+3H2?  CH3OH+H2O
CH3OH+H2O
c.CO2+CH4  CH3COOH d. 2CO2+6H2
CH3COOH d. 2CO2+6H2  CH2==CH2+4H2O
CH2==CH2+4H2O
以上反应中,最节能的是 ,原子利用率最高的是 。
(3)为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:
在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)△H=-49.0kJ/mol
CH3OH(g)+H2O(g)△H=-49.0kJ/mol
|
①从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)
②该反应的平衡常数表达式为 ,升高温度,平衡常数的数值将
(填“增大”、“减小”或“不变”)。
③下列措施中能使n(CH3OH)/n(CO2)增大的是 .
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1molCO2和3molH2
(4)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
N2(g)+3H2(g) ![]() 2NH3(g) △H=-93.4kJ/mol
2NH3(g) △H=-93.4kJ/mol
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如下图所示。
|
图t1时引起平衡移动的条件可能是 。
其中表示平衡混合物中NH3含量最高的一段时间是 。
②温度为T°C时,将3amolH2和amolN2放入带有活塞的密闭容器中,如果活塞能自由移动,充分反应后测得N2的转化率为50%。如果在相同温度下将3amolH2、amolN2和2amolNH3气体放入该容器中,平衡时H2的转化率为 。
查看习题详情和答案>>2I-+2Fe3+ƒ2Fe2++I2(aq)
(1)该反应的平衡常数K的表达式为:K=________,当上述反应达到平衡后,加入CCl4萃取I2,且温度不变,上述平衡________移动(填“向右”、“向左”或“不”)。
(2)上述反应的正反应速率和I-、Fe3+的浓度关系为v=kcm(I-)×cn(Fe3+)(k为常数)
浓度与反应速率的关系
c(I-)/mol×L-1 c(Fe3+)/mol×L-1 v/
mol×L-1
(1) 0.20 0.80 0.032k
(2) 0.60 0.40 0.144k
(3) 0.80 0.20 0.128k
通过所给的数据计算可知:
在v=kcm(I-)×cn(Fe3+)中,m、n的值为( )
A.m=1,n=1 B.m=1,n=2
C.m=2,n=1 D.m=2,n=2
I-浓度对反应速率的影响________Fe3+浓度对反应速率的影响(填“大于”、“小于”或“等于”)。
查看习题详情和答案>>
对于反应aA+bBƒcC+dD,反应达到平衡时,K=c(C)c×c(D)d/c(A)a×c(B)b(K为平衡常数),Fe3+和I-在水溶液中的反应如下:
2I-+2Fe3+ƒ2Fe2++I2(aq)
(1)该反应的平衡常数K的表达式为:K=________,当上述反应达到平衡后,加入CCl4萃取I2,且温度不变,上述平衡________移动(填“向右”、“向左”或“不”)。
(2)上述反应的正反应速率和I-、Fe3+的浓度关系为v=kcm(I-)×cn(Fe3+)(k为常数)
浓度与反应速率的关系
c(I-)/mol×L-1 c(Fe3+)/mol×L-1 v/ mol×L-1×s-1
(1) 0.20 0.80 0.032k
(2) 0.60 0.40 0.144k
(3) 0.80 0.20 0.128k
通过所给的数据计算可知:
在v=kcm(I-)×cn(Fe3+)中,m、n的值为( )
A.m=1,n=1 B.m=1,n=2
C.m=2,n=1 D.m=2,n=2
I-浓度对反应速率的影响________Fe3+浓度对反应速率的影响(填“大于”、“小于”或“等于”)。
查看习题详情和答案>>
已知反应:
![]()
(1)写出反应的平衡常数表达式K= ;
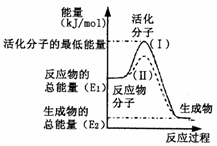
(2)右图表示反应过程中有关物质的能量,则反应的![]() 0(填“>”、“<”或“=”);
0(填“>”、“<”或“=”);
(Ⅰ)、(Ⅱ)两线中,使用催化剂的是 线;
(3)反应中发生反应的I-与被氧化的I-的物质的量比为 ;
(4)反应的速率可以用![]() 与加入的淀粉溶液反应显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,记录的数据如下:
与加入的淀粉溶液反应显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,记录的数据如下:
实验编号 | ① | ② | ③ | ④ | ⑤ |
c(I-)/mol·L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
c( | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
t/s | 88 | 44 | 22 | 11 | t1 |
则:该实验的目的是 ,
显色时间t1= s,
分析表中数据,得出的结论是 。
查看习题详情和答案>>(13分)在一定体积的密闭容器中,进行如下可逆反应:
CO(g)+H2O(g)==CO2(g)+H2(g),其化学平衡常数K和温度k的关系如
下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。该反应为 反应(选填“吸热”、“放热”)。
(2)能判断该反应是否达到化学平衡状态的依据是
(a)容器中压强不变 (b)混合气体中c(CO)不变
(c)![]() 逆(H2)=
逆(H2)=![]() 正(H2O) (d)c(CO2)=c(CO)
正(H2O) (d)c(CO2)=c(CO)
(3)830℃时,容器中的反应已达到平衡。在其他条件不变的情况下,缩小容器的体积。平衡 移(选填“向正反应方向”、“向逆反应方向”、“不”)
(4)若830℃时,向容器中充入1mol CO、5mol H2O,反应达到平衡后,CO的转化率为 。
查看习题详情和答案>>
