网址:http://m.1010jiajiao.com/timu_id_3733165[举报]
甲、乙、丙、丁四种无色(或白色)盐,它们的阳离子可能是![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,阴离子可能是
,阴离子可能是![]() 、
、![]() 进行如下实验:①四种盐均溶于水,且溶液为无色;②甲溶液呈中性,丙溶液呈碱性,其余溶液呈酸性;③丙的焰色反应呈黄色;④各取四种溶液于试管中,加入
进行如下实验:①四种盐均溶于水,且溶液为无色;②甲溶液呈中性,丙溶液呈碱性,其余溶液呈酸性;③丙的焰色反应呈黄色;④各取四种溶液于试管中,加入![]() 溶液,只有甲溶液不产生沉淀;⑤取四种溶液于试管中,分别加入氨水,丁溶液生成沉淀,氨水过量时,沉淀仍不消失;⑥将甲溶液分别加到其它三种溶液中,都有沉淀生成.则甲、乙、丙、丁是
溶液,只有甲溶液不产生沉淀;⑤取四种溶液于试管中,分别加入氨水,丁溶液生成沉淀,氨水过量时,沉淀仍不消失;⑥将甲溶液分别加到其它三种溶液中,都有沉淀生成.则甲、乙、丙、丁是
[ ]
|
甲 |
乙 |
丙 |
丁 |
|
A.Ba(NO3)2 |
CuSO4 |
Na2CO3 |
AgNO3 |
|
B.BaCl2 |
(NH4)2SO4 |
Na2CO3 |
Al2(SO4)3 |
|
C.Fe(NO3)3 |
(NH4)2SO4 |
Na2CO3 |
Al2(SO4)3 |
|
D.BaCl2 |
(NH4)2SO4 |
Na2CO3 |
AgNO3 |
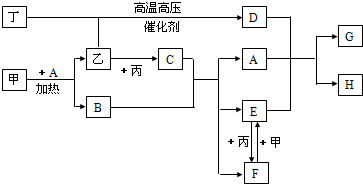
(1)D的化学式为
(2)甲+A反应的化学方程式为
| ||
| ||
(3)F+甲反应的离子方程式为
(4)A+D+E反应的离子方程式为
(1)D与C形成一种含有两种化学键的离子化合物,写出该离子化合物的电子式:
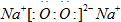
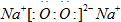
(2)甲是由A、B、C三种元素组成的相对分子质量最小的物质,且可以发生银镜反应,请写出甲的结构式:
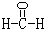
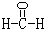
(3)由A、B两种元素组成的非极性分子有多种,其中一个分子含4个原子的为乙,已知乙的燃烧热为1300kJ/mol,乙燃烧的热化学反应方程式是:
| 1 |
| 2 |
| 1 |
| 2 |
如果用乙与C的单质在KOH作电解质溶液的条件下构成燃料电池,请写出其负极的电极反应式为:
(4)均由A、C、D、E四种元素组成的两种物质丙和丁在溶液中反应的离子方程式是:
(5)A与C形成一种物质戊,在酸性条件下,将少量戊加入淀粉KI溶液后,溶液显蓝色,反应的离子方程式是
(6)E的一种氧化物与ClO-均具有漂白性,但两者混合后的产物均不具有漂白性,请写出该反应的离子方程式:
A、B、C、D、E均为钠盐,D、E具有相同的元素组成,都是由四种元素组成的化合物。向B溶液中滴加硝酸酸化的硝酸银溶液,立即产生白色沉淀,该沉淀见光变暗至灰至黑。A、B或B、C溶液混合均无明显现象,若将A、B、E和B、C、E分别按1:5:6和1:1:2的物质的量之比混合,溶液都能产生有刺激性气味黄绿色气体甲。D、E溶液混合能产生具有漂白性的刺激性气体乙。甲与乙混合气体通入水中会产生两种酸。B与E固体混合不反应,加热则能产生有刺激性气味的气体丙。若将气体丙通入A或C溶液中均能产生气体甲。甲气体通入D溶液,颜色会消失。若将A、D、E按2:1:1物质的量之比混合,能产生黄色气体丁。
请回答下列有关问题:
⑴.完成下列反应的离子方程式并配平之。
①.A + B + E → : ▲
②.D + E → : ▲
③.甲+乙+ H2O → : ▲
④.A + D + E → : ▲
⑵.丁气体消毒漂白性比甲强,是更理想的漂白试剂。相同条件下,相同体积的丁气体处理水的能力是甲的 ▲ 倍;相同质量的丁气体处理水的能力是甲的 ▲ 倍。
⑶.历史上曾把某元素的最高价的含氧酸称为某酸,如N、P、S等。A盐中对应的酸并不是该元素的最高价的含氧酸(当时误认为是最高价)。电解技术进入化学研究领域后,通过惰性材料电解A的水溶液,产生新的含氧酸盐(M=122.5 g·mol-1),我们可以把与其对应的酸称为高某酸。取出100 mL A盐溶液进行电解(惰性电极,通直流电),数小时后,收集到的阴、阳两极气体分别为6.72L和2.24L(已经折算成标准状况下的气体体积) 。
①.阴、阳两极所发生的电极反应离子方程式为 ▲ 、 ▲ 。
②.原A盐溶液的物质的量浓度为 ▲ 。(假设溶液体积变化忽略不计)
查看习题详情和答案>>制造导弹的雷达罩和宇航员使用的氧气瓶的主要材料是透明聚酯玻璃钢,制备它的一种配方中含有下列四种物质:



(甲) (乙) (丙) (丁)
填写下列空白:
(1)甲中不含氧原子的官能团是______;甲分子_____(填“有”或“无”)顺反异构现象;下列试剂能与甲反应而褪色的是(填标号) 。
a. Br2/CCl4溶液 b. 石蕊溶液 c.酸性KMnO4溶液
(2)写出乙与足量Na反应的化学方程式 。
(3)已知:
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是 。
(4)化合物丁仅含碳、氢、氧三种元素,相对分子质量为110。丁与FeCl3溶液作用显现特征颜色,且丁分子中烃基上的一氯取代物只有一种。则丁的结构简式为 。