题目内容
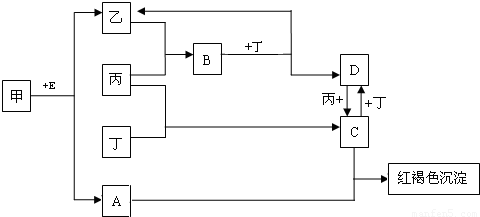
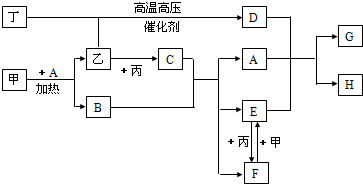
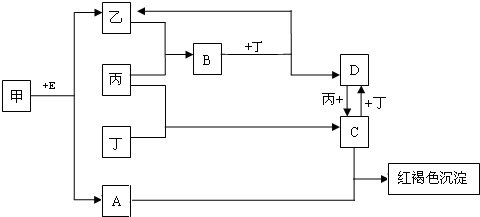
甲、乙、丙、丁为四种常见单质,常温下,乙、丙、丁为气体.丙常用于自来水消毒,甲是生活中常见金属,A在通常情况下为无色液体,B、C在溶液中反应.
(1)D的化学式为
(2)甲+A反应的化学方程式为
(3)F+甲反应的离子方程式为
(4)A+D+E反应的离子方程式为

(1)D的化学式为
NH3
NH3
;闻气体丙的正确方法是扇闻
扇闻
;取少量长期放置的丙的水溶液,滴入几滴石蕊试液,可观察到的现象是溶液变红
溶液变红
.(2)甲+A反应的化学方程式为
3Fe+4H2O
Fe3O4+4H2
| ||
3Fe+4H2O
Fe3O4+4H2
.
| ||
(3)F+甲反应的离子方程式为
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
;该反应中,证明甲适量或过量的方法是取少量反应后的溶液于试管中,滴入几滴KSCN溶液,若溶液不变色,说明甲过量或适量
取少量反应后的溶液于试管中,滴入几滴KSCN溶液,若溶液不变色,说明甲过量或适量
.(4)A+D+E反应的离子方程式为
Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+
Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+
;该反应能顺利进行,是利用了D的极易溶于水且溶于水后显碱性
极易溶于水且溶于水后显碱性
的性质;若反应在试管中进行一,则其现象为先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色
先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色
.分析:丙常用于自来水消毒,应为Cl2,A在通常情况下为无色液体,应为H2O,甲是生活中常见金属且能与水在加热条件下反应,则甲为Fe,乙为H2,B为Fe3O4,C为HCl,由转化关系可知E为
FeCl2,F为FeCl3,丁与氢气在高温、高压、催化剂作用下反应,应是合成氨的反应,则丁为N2,D为NH3,D、A、E反应生成Fe(OH)2和NH4Cl,结合物质的性质以及题目要求可解答该题.
FeCl2,F为FeCl3,丁与氢气在高温、高压、催化剂作用下反应,应是合成氨的反应,则丁为N2,D为NH3,D、A、E反应生成Fe(OH)2和NH4Cl,结合物质的性质以及题目要求可解答该题.
解答:解:丙常用于自来水消毒,应为Cl2,A在通常情况下为无色液体,应为H2O,甲是生活中常见金属且能与水在加热条件下反应,则甲为Fe,乙为H2,B为Fe3O4,C为HCl,由转化关系可知E为FeCl2,F为FeCl3,丁与氢气在高温、高压、催化剂作用下反应,应是合成氨的反应,则丁为N2,D为NH3,D、A、E反应生成Fe(OH)2和NH4Cl,
(1)由以上分析可知D为NH3,丙为Cl2,有毒,闻气味时应用手在瓶口轻轻煽动,使极少量气体飘进鼻孔,长期放置氯水,由于HClO分解生成HCl,则滴入几滴石蕊试液,溶液变红,
故答案为:NH3;扇闻;溶液变红;
(2)Fe和水在高温下发生反应生成四氧化三铁和氢气,反应的方程式为3Fe+4H2O
Fe3O4+4H2,故答案为:3Fe+4H2O
Fe3O4+4H2;
(3)F+甲为FeCl3和Fe的反应,反应的离子方程式为2Fe3++Fe=3Fe2+,如Fe过量,则溶液中不存在Fe3+,可用KSCN溶液检验,操作方法为取少量反应后的溶液于试管中,滴入几滴KSCN溶液,若溶液不变色,说明甲过量或适量,
故答案为:2Fe3++Fe=3Fe2+;取少量反应后的溶液于试管中,滴入几滴KSCN溶液,若溶液不变色,说明甲过量或适量;
(4)D、A、E反应生成Fe(OH)2和NH4Cl,反应的离子方程式为Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+,氨气极易溶于水,且溶液呈碱性,生成的白色絮状Fe(OH)2沉淀不稳定,易被空气中氧气氧化而迅速变成灰绿色,最后变成红褐色,
故答案为:Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+;极易溶于水且溶于水后显碱性;先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色.
(1)由以上分析可知D为NH3,丙为Cl2,有毒,闻气味时应用手在瓶口轻轻煽动,使极少量气体飘进鼻孔,长期放置氯水,由于HClO分解生成HCl,则滴入几滴石蕊试液,溶液变红,
故答案为:NH3;扇闻;溶液变红;
(2)Fe和水在高温下发生反应生成四氧化三铁和氢气,反应的方程式为3Fe+4H2O
| ||
| ||
(3)F+甲为FeCl3和Fe的反应,反应的离子方程式为2Fe3++Fe=3Fe2+,如Fe过量,则溶液中不存在Fe3+,可用KSCN溶液检验,操作方法为取少量反应后的溶液于试管中,滴入几滴KSCN溶液,若溶液不变色,说明甲过量或适量,
故答案为:2Fe3++Fe=3Fe2+;取少量反应后的溶液于试管中,滴入几滴KSCN溶液,若溶液不变色,说明甲过量或适量;
(4)D、A、E反应生成Fe(OH)2和NH4Cl,反应的离子方程式为Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+,氨气极易溶于水,且溶液呈碱性,生成的白色絮状Fe(OH)2沉淀不稳定,易被空气中氧气氧化而迅速变成灰绿色,最后变成红褐色,
故答案为:Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+;极易溶于水且溶于水后显碱性;先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色.
点评:本题考查无机物的推断,题目难度中等,题目的推断以物质的颜色、状态或用途作为突破口,侧重于物质的性质以及方程式的考查,要求具有较强的分析能力.

练习册系列答案
相关题目
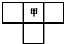 甲、乙、丙、丁为四种短周期元素,在周期表中,甲与乙、丙、丁在周期表中的位置关系如图所示(原子序数:乙>丙).丁的原子序数与乙、丙原子序数之和相等,四种元素原子的最外层电子数之和为24.下列判断正确的是( )
甲、乙、丙、丁为四种短周期元素,在周期表中,甲与乙、丙、丁在周期表中的位置关系如图所示(原子序数:乙>丙).丁的原子序数与乙、丙原子序数之和相等,四种元素原子的最外层电子数之和为24.下列判断正确的是( )