摘要:14.FeS+2Fe(OH)3+3H2SO4=S↓+3FeSO4+6H2O 88 2×107 32 m3] 1.6g m3]=10.7g 由此当Fe(OH)3过量时.FeS为4.4g. 当FeS过量时FeS为:28.3g-10.7g=17.6g.
网址:http://m.1010jiajiao.com/timu_id_3728773[举报]
下列离子方程式中,正确的是( )
A.FeS固体放入稀硝酸溶液中:FeS+2H+====Fe3++H2S↑
B.把Na2O2投入到FeCl2溶液中:2Na2O2+2Fe2++2H2O====2Fe(OH)2↓+4Na++O2↑
C.苯酚钠溶液中通入CO2:![]()
D.向Ca(HCO3)2溶液中加入含等物质的量的氢氧化钠溶液:
Ca2++2![]() +OH-====CaCO3↓+2H2O+
+OH-====CaCO3↓+2H2O+![]()
浅绿色溶液A和无色溶液B可进行下列反应,D是一种常见的盐,E是气态氢化物,G是非金属氧化物.

(1)填写下列各物质的化学式:A
(2)浅绿色溶液A与NaOH溶液反应先生成白色沉淀,此沉淀迅速变成灰绿色最后变成红褐色,写出此反应过程中的化学方程式
①
②
(3)写出沉淀C与稀盐酸反应生成浅绿色溶液A和气体E的化学方程式:
查看习题详情和答案>>

(1)填写下列各物质的化学式:A
FeCl2
FeCl2
,BNa2S
Na2S
,HFeCl3
FeCl3
;(2)浅绿色溶液A与NaOH溶液反应先生成白色沉淀,此沉淀迅速变成灰绿色最后变成红褐色,写出此反应过程中的化学方程式
①
FeCl2+2NaOH=2NaCl+2Fe(OH) 2↓
FeCl2+2NaOH=2NaCl+2Fe(OH) 2↓
;②
4Fe(OH) 2+O2+2H2O=4Fe(OH) 3
4Fe(OH) 2+O2+2H2O=4Fe(OH) 3
.(3)写出沉淀C与稀盐酸反应生成浅绿色溶液A和气体E的化学方程式:
FeS+2HCl=FeCl2+H2S↑
FeS+2HCl=FeCl2+H2S↑
.(2008?北京)常状况下,X、Y和Z是三种气态单质.X的组成元素是第三周期原子半径最小的元素(稀有气体元素除外);Y和Z均由元素R组成,反应Y+2I-+2H+═I2+Z+H2O常作为Y的滴定反应.
(1)Y与Z的关系是(选填字母)
a.同位素 b.同系物 c.同素异形体 d.同分异构体
(2)将Y和二氧化硫分别通入品红溶液,都能使品红褪色.简述用褪色的溶液区别二者的实验方法
(3)举出实例说明X的氧化性比硫单质的氧化性强(用化学方程式表示).
(4)气体(CN)2与X化学性质相似,也能与H2反应生成HCN(其水溶液是一种酸).
①HCN分子中含有4个共价键,其结构式是
②KCN溶液显碱性,原因是(用离子方程式表示)
(5)加热条件下,足量的Z与某金属M的盐MCR3(C为碳元素)完全反应生成CR2和MmRn(m、n均为正整数).若CR2质量为ω1g,MmRn质量为ω2g,M的相对原子质量为a,则MmRn中m:n=
查看习题详情和答案>>
(1)Y与Z的关系是(选填字母)
c
c
.a.同位素 b.同系物 c.同素异形体 d.同分异构体
(2)将Y和二氧化硫分别通入品红溶液,都能使品红褪色.简述用褪色的溶液区别二者的实验方法
加热褪色后的溶液,若溶液恢复红色,则原通入气体为SO2;若溶液不变红,则原通入气体是O3
加热褪色后的溶液,若溶液恢复红色,则原通入气体为SO2;若溶液不变红,则原通入气体是O3
.(3)举出实例说明X的氧化性比硫单质的氧化性强(用化学方程式表示).
2Fe+3Cl2
2FeCl3,Fe+S
FeS
| ||
| ||
2Fe+3Cl2
2FeCl3,Fe+S
FeS
.
| ||
| ||
(4)气体(CN)2与X化学性质相似,也能与H2反应生成HCN(其水溶液是一种酸).
①HCN分子中含有4个共价键,其结构式是
H-C≡N
H-C≡N
.②KCN溶液显碱性,原因是(用离子方程式表示)
CN-+H2O?HCN+OH-
CN-+H2O?HCN+OH-
.(5)加热条件下,足量的Z与某金属M的盐MCR3(C为碳元素)完全反应生成CR2和MmRn(m、n均为正整数).若CR2质量为ω1g,MmRn质量为ω2g,M的相对原子质量为a,则MmRn中m:n=
16ω1:(44ω2-aω1)
16ω1:(44ω2-aω1)
(用含ω1、ω2和a的代数式表示).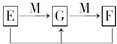 已知A、B、C、D两种短周期元素,分别属于不同的主族,其原子序数依次增大,其中A与D、B与C的原子的最外层电子数之和均为9,A原子的最外层与次外层电子数相等,A、B、C、D中只有两种金属元素.试回答下列问题:
已知A、B、C、D两种短周期元素,分别属于不同的主族,其原子序数依次增大,其中A与D、B与C的原子的最外层电子数之和均为9,A原子的最外层与次外层电子数相等,A、B、C、D中只有两种金属元素.试回答下列问题:(1)A的元素符号为
Be
Be
,C的氢化物的化学式为H2S
H2S
.(2)为比较C与D的单质的氧化性强弱,可设计实验以证实,则该实验所依据的反应的化学方程式为
Fe+S
FeS,2Fe+3Cl2
2FeCl3(或H2S+Cl2═S↓+2HCl)
| ||
| ||
Fe+S
FeS,2Fe+3Cl2
2FeCl3(或H2S+Cl2═S↓+2HCl)
.
| ||
| ||
(3)1molC的氢化物与足量C的氧化物反应,转移的电子的物质的量为
2
2
mol.(4)已知E、G、F是均含有B元素的化合物,其有关转化关系如图,请写出E与F反应生成G的离子方程式
Al3++3AlO2-+6H2O═4Al(OH)3
Al3++3AlO2-+6H2O═4Al(OH)3
.科研人员将软锰矿(MnO2含量≥65%,SiO2含量约20%,A12O3含量约4%,其余为水分)和闪锌矿(ZnS含量≥80%,FeS、CuS、SiO2含量约7%,其余为水分)同槽酸浸开发出综合利用这两种资源的新工艺,如图所示为工艺流程的一部分.
已知:ZnCO3不溶于水,但溶于酸.部分阳离子以氢氧化物形式深沉时溶液的pH见下表:
| 物质 | Fe(OH)3 | A1(OH)3 | Zn(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 3.3 | 5.4 | 7.6 | 8.3 |
| 完全沉淀pH | 4.4 | 5.2 | 8.0 | 9.6 | 9.8 |
(1)反应器I过滤所得滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、A12(CO4)3等.试完成反应器I中生成CuSO4的化学方程式(不须配平):CuS+______+H2SO4→______+______+CuSO4+H2O
(2)反应器II中发生反应的离子方程式为______.
(3)从沉淀溶解平衡的角度分析反应器III中生成A1(OH)3沉淀的原因______.检验ZnCO3是否过量的操作方法是______.
(4)反应器中IV中,试剂A可以是下列物质中______(填代号).a.氨水 b.氢氧化钠 c.MnO2 d.稀硫酸
(5)欲从反应器IV的滤液中完全沉淀出Zn(OH)2,而不析出Mn(OH)2,则滤液的pH范围为______,要将分离出沉淀后的滤液进行浓缩,需将温度控制在90℃~100℃,可采用的加热方法是______. 查看习题详情和答案>>