摘要:8.常温下浓HNO3能与Cu反应.而对Al有钝化作用.
网址:http://m.1010jiajiao.com/timu_id_3728769[举报]
下列关于浓HNO3和浓H2SO4的叙述中不正确的是( )
A. 常温下二者都可用铁制容器贮存
B. 常温下二者都能与铜较快反应
C. 露置于空气中,溶液浓度均降低
D. 浓HNO3与浓H2SO4都具有强氧化性
查看习题详情和答案>>
下列关于浓HNO3和浓H2SO4的叙述中不正确的是
- A.常温下二者都可用铁制容器贮存
- B.常温下二者都能与铜较快反应
- C.露置于空气中,溶液浓度均降低
- D.浓HNO3与浓H2SO4都具有强氧化性
浓硝酸见光或受热分解,该化学方程式为________________________.
硝酸越浓,越________分解.浓硝酸久置呈黄色,是由于________.常温下浓HNO3使________、________钝化.
浓硝酸与浓盐酸的混合物(体积比________)叫王水,能使一些不溶于硝酸的金属如________、________等溶解.
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究,A、B、C三处分别是HNO3溶液、Na2CO3溶液、Na2SiO3溶液;乙同学设计了如图2装置来验证卤族元素性质的递变规律.A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸.已知常温下浓盐酸与高锰酸钾能反应生成氯气.
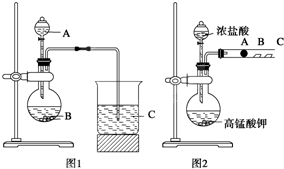
(1)写出甲同学(图1)仪器的名称:A ,B ,C_ ;
(2)图1中各反应的离子方程式分别为 ;
(3)写出乙同学设计的B处的离子方程式: .
(4)写出乙同学设计的C处的实验现象 .
查看习题详情和答案>>

(1)写出甲同学(图1)仪器的名称:A
(2)图1中各反应的离子方程式分别为
(3)写出乙同学设计的B处的离子方程式:
(4)写出乙同学设计的C处的实验现象