摘要: A:OD:Ca(钙)A2-: B2+:
网址:http://m.1010jiajiao.com/timu_id_3728677[举报]
[三选一—选修物质结构与性质]
科学新发现推动社会大发展。
(1)2010年11月,日本东京大学的几原雄一教授在研究氢与钒(V)的化合物时捕捉到了氢原子,成功拍下了世界首张氢原子的照片。如图所示是氢钒化合物的晶体构造。
科学新发现推动社会大发展。
(1)2010年11月,日本东京大学的几原雄一教授在研究氢与钒(V)的化合物时捕捉到了氢原子,成功拍下了世界首张氢原子的照片。如图所示是氢钒化合物的晶体构造。

①写出基态钒原子的核外电子排布式___________。
②该氢钒化合物的化学式为____________。
(2)2010年8月,澳大利亚悉尼大学陈敏(Min Chen)博士等研究人员发现了一种能吸收红外光谱的叶绿素-f,这是迄今为止发现的第五种叶绿素。下图是某叶绿素的结构简式。
②该氢钒化合物的化学式为____________。
(2)2010年8月,澳大利亚悉尼大学陈敏(Min Chen)博士等研究人员发现了一种能吸收红外光谱的叶绿素-f,这是迄今为止发现的第五种叶绿素。下图是某叶绿素的结构简式。

① 叶绿素中含有C、H、O、N、Mg五种元素,C、N、O三种元素的第一电离能由小到大的顺序是_______________。
②叶绿素中氮原子的杂化方式为_______________,
在下图的方框内用“→”标出Mg2+的配位键。
②叶绿素中氮原子的杂化方式为_______________,
在下图的方框内用“→”标出Mg2+的配位键。

(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。O2在其催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO-互为等电子体的分子、离子化学式分别为____________、______________(各写一种)。
(4)肼可用作火箭燃料,肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在________ (填标号)。
a.离子键 b.共价键 c.配位键 d.范德华力
查看习题详情和答案>>
(4)肼可用作火箭燃料,肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在________ (填标号)。
a.离子键 b.共价键 c.配位键 d.范德华力
下列关于元素性质的有关叙述中不正确的是( )
| A、S Cl O F的原子半径依次减小 | B、Na Mg Al Si的失电子能力依次增强 | C、C N O F的气态氢化物的稳定性依次增强 | D、Si P S Cl的最高价含氧酸的酸性依次增强 |
(2011?天津模拟)下表为元素周期表的一部分,请参照元素①一⑧在表中的位置,用化学用语回答下列问题:
Ⅰ.(1)请画出元素⑧的离子结构示意图
 .
.
(2)元素⑦中质子数和中子数相等的同位素符号是
(3)④、⑤、⑦的原子半径由大到小的顺序为
(4)⑦和⑧的最高价氧化物对应水化物的酸性强弱为
(5)④、⑤两种元素的原子按1:1组成的常见化合物的电子式为
 .
.
Ⅱ.由表中①一⑧中的一种或几种元素形成的常见物质A、B、C可发生以下反应(副产物已略去),试回答:

(1)若X是强氧性化单质,则A不可能是
a.S b.N2 c.Na d.Mg e.Al
(2)若X是一种常见过渡金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属离子的化学试剂和现象分别是
(3)若A,B、C为含有同一金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为
查看习题详情和答案>>
| 族 周期 |
IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||


(2)元素⑦中质子数和中子数相等的同位素符号是
1632S
1632S
.(3)④、⑤、⑦的原子半径由大到小的顺序为
Na>S>O
Na>S>O
.(4)⑦和⑧的最高价氧化物对应水化物的酸性强弱为
HClO4
HClO4
>H2SO4
H2SO4
.(5)④、⑤两种元素的原子按1:1组成的常见化合物的电子式为


Ⅱ.由表中①一⑧中的一种或几种元素形成的常见物质A、B、C可发生以下反应(副产物已略去),试回答:

(1)若X是强氧性化单质,则A不可能是
de
de
(填序号).a.S b.N2 c.Na d.Mg e.Al
(2)若X是一种常见过渡金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属离子的化学试剂和现象分别是
KSCN溶液和氯水;滴加KSCN溶液不显红色,再加入氯水显红色(或者加NaOH溶液,先产生白色沉淀,迅速变成灰绿色,最后变成红褐色)
KSCN溶液和氯水;滴加KSCN溶液不显红色,再加入氯水显红色(或者加NaOH溶液,先产生白色沉淀,迅速变成灰绿色,最后变成红褐色)
;又知在酸性溶液中该金属离子能被双氧水氧化,写出该反应的离子方程式H2O2+2Fe2++2H+═2Fe2++2H2O
H2O2+2Fe2++2H+═2Fe2++2H2O
.(3)若A,B、C为含有同一金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为
Al(OH)3
Al(OH)3
,写出A与C两溶液反应的离子方程式Al3++3AlO2-+6H2O═4Al(OH)3↓
Al3++3AlO2-+6H2O═4Al(OH)3↓
.测定有机物中碳和氢的质量分数,常用燃烧分析法,在750°C左右使有机物在氧气流中全部氧化成CO2和H2O;分别用装有固体NaOH和Mg(ClO4)2的吸收管吸收CO2和H2O.某课外活动小组,设计利用如图所示装置取纯净的乙烯,并测定乙烯分子中碳、氢原子的个数比;甲为燃烧管,当乙烯和氧气通过时,由于催化剂的存在而不会发生爆炸,乙烯被氧化成CO2和H2O.请回答下列问题: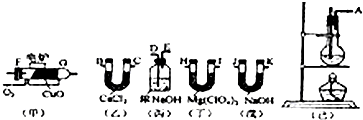
(1)已知整套装置的连接顺序(按气流方向从左到右填写仪器的接口字母):A接D,E接B,C接F,G接H,I接J…则丙装置的作用 .丁装置的作用 甲装置中CuO的作用是
(2)烧瓶中发生反应的化学方程式是:
(3)实验时应使烧瓶中溶液的温度迅速升至170°C,原因是 ;
(4)若测得的比值偏高,导致这种误差的可能的原因是 .
A.乙烯中混有少量的乙醚(C2H5OC2H5)
B.乙烯进入燃烧管时,含有少量的水蒸气
C.乙烯中混有少量的CO
D.乙烯进入燃烧管时,含有少量的CO2
(5)若准确称取0.90g样品(只含C、H、O三种元素中的两种或三种)经充分燃烧后,戊质量增加1.32g,丁质量增加0.54g,则该有机物的最简式为 .
查看习题详情和答案>>
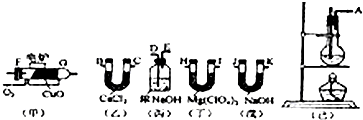
(1)已知整套装置的连接顺序(按气流方向从左到右填写仪器的接口字母):A接D,E接B,C接F,G接H,I接J…则丙装置的作用
(2)烧瓶中发生反应的化学方程式是:
(3)实验时应使烧瓶中溶液的温度迅速升至170°C,原因是
(4)若测得的比值偏高,导致这种误差的可能的原因是
A.乙烯中混有少量的乙醚(C2H5OC2H5)
B.乙烯进入燃烧管时,含有少量的水蒸气
C.乙烯中混有少量的CO
D.乙烯进入燃烧管时,含有少量的CO2
(5)若准确称取0.90g样品(只含C、H、O三种元素中的两种或三种)经充分燃烧后,戊质量增加1.32g,丁质量增加0.54g,则该有机物的最简式为
在一百多种化学元素中,非金属占了23种。80%的非金属元素在社会中占重要位置。如C、N、O、Si、Cl等。
(1)氯元素原子最外电子层上有 种能量不同的电子,该元素的简单阴离子核外电子排布式是 。
(2)由氮元素与硅元素组成的物质,可用于制造发动机的耐热部件,因为它属于 晶体,请写出该化合物的化学式 。
(3)下列事实能说明氯与氧两元素非金属性相对强弱的有 。(选填编号)
a.Cl原子最外层电子数比氧多
b.酸性:HCl>H2O
c.ClO2中氯元素为+4价,氧元素为−2价
d.沸点:H2O>HCl
与Cl2相比较,ClO2处理水时被还原成Cl-,不生成有机氯代物等有害物质。工业上可用亚氯酸钠和稀盐酸为原料制备ClO2,反应如下:NaClO2 +HCl ClO2↑+___________________(没有配平)
ClO2↑+___________________(没有配平)
(4)上述方程式中,缺项物质是___________,配平方程式,并在下面补全反应物系数。____NaClO2 +____HCl
(5)该反应中氧化剂和还原剂的物质的量之比是 。生成0.2 mol ClO2转移电子的物质的量为 _______ mol。
(6)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某污水中含CN-a mg/L,现用ClO2将CN-氧化,只生成两种无毒气体。处理100m3这种污水,至少需要ClO2 _______ mol 。
查看习题详情和答案>>