摘要:11.具有相同电子层结构的三种微粒An+.Dn-.C.下列分析正确的一组是 ( ) A.原子序数关系是C>B>A B.微粒半径的关系是Bn->An+ C.C一定是稀有气体元素的一种原子 D.原子半径的关系是A<C<B
网址:http://m.1010jiajiao.com/timu_id_3722311[举报]
元素周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,表中所列字母A、D、F、G、Q、M、R、N、T分别代表某种化学元素.请依据这9种元素回答下列问题.

(1)表中T的元素符号为
(2)元素的非金属性:M
(3)R的最高价氧化物对应水化物的化学式是
(4)F、G两元素形成的淡黄色固体物质的电子式为
 ,该物质含有的化学键的类型是
,该物质含有的化学键的类型是
(5)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是
(6)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
 .
.
(7)A与D形成分子的空间结构可能是(填序号)
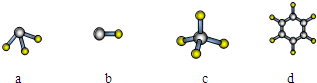
查看习题详情和答案>>

(1)表中T的元素符号为
Fe
Fe
,金属性最强的元素是K
K
(填元素符号).(2)元素的非金属性:M
<
<
R(填“>”或“<”).(3)R的最高价氧化物对应水化物的化学式是
HClO4
HClO4
.(4)F、G两元素形成的淡黄色固体物质的电子式为


离子键、非极性共价键
离子键、非极性共价键
.(5)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是
S2->Cl->K+
S2->Cl->K+
(填离子符号).(6)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为


(7)A与D形成分子的空间结构可能是(填序号)
cd
cd
.
A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大2,C原子的电子总数比B原子电子总数多4.1molA的单质和足量盐酸反应可置换出11.2L(标准状况下)氢气,这时A转化成与氖原子具有相同电子层结构的离子.试回答:
(1)A是
(2)分别写出A、B的最高价氧化物对应的水化物分别和C的气态氢化物的水溶液反应的离子方程式:
(3)A离子的氧化性比B离子的氧化性
查看习题详情和答案>>
(1)A是
Na
Na
元素,B是Al
Al
元素,C是Cl
Cl
元素.(2)分别写出A、B的最高价氧化物对应的水化物分别和C的气态氢化物的水溶液反应的离子方程式:
H++OH-=H2O
H++OH-=H2O
、Al(OH)3+3H+=Al3++3H2O
Al(OH)3+3H+=Al3++3H2O
(3)A离子的氧化性比B离子的氧化性
弱
弱
.下面是元素周期表的一部分,表中所列字母A、D、E、G、Q、M、R、T分别代表某一化学元素.请用所给元素回答下列问题.
(1)某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为 ;与Ar原子具有相同电子层结构的简单离子中半径由大到小的顺序是(用离子符号表示) .
(2)M、D两种元素形成的化合物含有的化学键类型是 ,分子的电子式为: ;
A与D形成分子的空间结构可能是如图1的(填序号) .
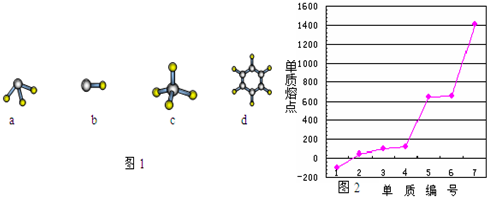
(3)保存T元素的二价硫酸盐需采取的措施是和理由是 ;所给元素中组成合适的反应物,用离子方程式表明元素M、R的非金属性强弱 .
(4)第三周期主族元素(零族除外)单质熔点高低的顺序如图2所示,“1”所代表物质的化学式是 ,“7”所对应的元素形成最高价氧化物的化学式是 .
查看习题详情和答案>>
| A | |||||||||||||||||
| D | E | ||||||||||||||||
| G | Q | M | R | ||||||||||||||
| T | |||||||||||||||||
(2)M、D两种元素形成的化合物含有的化学键类型是
A与D形成分子的空间结构可能是如图1的(填序号)

(3)保存T元素的二价硫酸盐需采取的措施是和理由是
(4)第三周期主族元素(零族除外)单质熔点高低的顺序如图2所示,“1”所代表物质的化学式是