摘要:2溶液中存在溶解平衡 Ca(OH)2(s)Ca2++2OH-.增加OH-的浓度.平衡向左移动.出现浑浊.(2)先浑浊后澄清.CO2+Ca2++2OH-=CaCO3↓+H2O.CaCO3+CO2+H2O=Ca(HCO3)2 (3)产生白色沉淀 Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O 讲析:25.混合气体通过浓H2SO4体积减少40mL.为NH3.有NH3就无HCl.通过Na2O2体积减小40mL.有80mLCO2.同时通过反应生成40mLO2.引燃混合气体有70mLH2与35mLO2发生反应.从而剩余O25mL.原混合气体中无NO.O2.
网址:http://m.1010jiajiao.com/timu_id_3715187[举报]
常温下Ca(OH)2溶于水达到饱和时存在如下平衡:Ca(OH)2(s) Ca2++2OH-,饱和石灰水的密度为d g/cm3,溶液pH=12。下列有关叙述中,不正确的是
Ca2++2OH-,饱和石灰水的密度为d g/cm3,溶液pH=12。下列有关叙述中,不正确的是
| A.加热至50℃,溶液的Ca2+的浓度增大 |
B.该温度下Ca(OH)2的溶解度为 (g/100gH2O) (g/100gH2O) |
| C.该饱和石灰水中,水电离出的OH-的浓度为10-12mol/L |
D.加入生石灰并恢复至常温后, 值不变 值不变 |
有固体存在的Ca(OH)2饱和溶液中有如下平衡:Ca(OH)2(s)?Ca2+(aq)+20H-(aq);△H<0
(1)向该饱和溶液中加入少量固体CH3COONa时,固体Ca(OH)2的质量 (填“变大”、“变小’’或“不变”,后同),加入少量冰醋酸时,固体Ca(OH)2的质量 ;
(2)Ca(OH)2饱和溶液中的电荷守恒式为
(3)常温下,Ca(OH)2饱和溶液中离子浓度由大到小的顺序是 ;
(4)将0.5molCa(OH)2固体与1mol稀HCl混合,放出热量75.6kJ.该反应的热化学方程式为 ;该反应放出热量大于57.3kJ的原因是 ;
(5)某温度下,pH=13的Ca(OH)2饱和溶液中Kw=1.0×10-16,则该温度下Ca(OH)2的饱和溶液的物质的量浓度为 .
查看习题详情和答案>>
(1)向该饱和溶液中加入少量固体CH3COONa时,固体Ca(OH)2的质量
(2)Ca(OH)2饱和溶液中的电荷守恒式为
(3)常温下,Ca(OH)2饱和溶液中离子浓度由大到小的顺序是
(4)将0.5molCa(OH)2固体与1mol稀HCl混合,放出热量75.6kJ.该反应的热化学方程式为
(5)某温度下,pH=13的Ca(OH)2饱和溶液中Kw=1.0×10-16,则该温度下Ca(OH)2的饱和溶液的物质的量浓度为
 如图为一定量饱和Ca(OH)2溶液中通入二氧化碳气体后,产生CaCO3白色沉淀的质量与二氧化碳体积之间的关系曲线.试回答:
如图为一定量饱和Ca(OH)2溶液中通入二氧化碳气体后,产生CaCO3白色沉淀的质量与二氧化碳体积之间的关系曲线.试回答:OA段曲线和AB段曲线所表示的反应方程式是:
OA段
Ca(OH)2+CO2=CaCO3↓+H2O
Ca(OH)2+CO2=CaCO3↓+H2O
;AB段Ca(HCO3)2=CaCO3↓+CO2↑+H2O
Ca(HCO3)2=CaCO3↓+CO2↑+H2O
;OA段=AB段原因是生成CaCO3沉淀和CaCO3沉淀溶解所消耗的二氧化碳的量相等
生成CaCO3沉淀和CaCO3沉淀溶解所消耗的二氧化碳的量相等
B处溶液中存在的浓度较大的两种离子是
Ca2+
Ca2+
和HCO3-
HCO3-
(填离子符号)将B处生成的溶液煮沸,可见到的现象是
有白色沉淀生成
有白色沉淀生成
.难溶性杂卤石(K2SO4·MgSO4·2CaSO4·2H2O)属于“呆矿”,在水中存在如下平衡
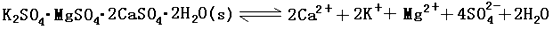
为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如下:
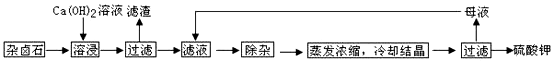
(1)滤渣主要成分有_______和_______以及未溶杂卤石。
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:__________。
(3)“除杂”环节中,先加入_______溶液,经搅拌等操作后,过滤,再加入_______溶液调滤液PH至中性。
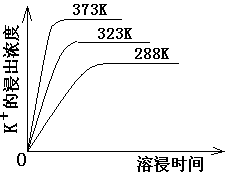
(4)不同温度下,K+的浸出浓度与溶浸时间的关系如下图,由图可得,随着温度升高,
①________________________②____________________
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:__________。
(3)“除杂”环节中,先加入_______溶液,经搅拌等操作后,过滤,再加入_______溶液调滤液PH至中性。
(4)不同温度下,K+的浸出浓度与溶浸时间的关系如下图,由图可得,随着温度升高,
①________________________②____________________
(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:
 已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此温度下该反应的平衡常数K(计算结果保留三位有效数字)。
已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此温度下该反应的平衡常数K(计算结果保留三位有效数字)。
查看习题详情和答案>>
 已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此温度下该反应的平衡常数K(计算结果保留三位有效数字)。
已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此温度下该反应的平衡常数K(计算结果保留三位有效数字)。海水中含有丰富的化学元素,下面是某化工厂从海水中提取NaCl、Mg(以MgCl2形式存在)和Br2(以NaBr的形式存在)及综合利用的生产流程简图(如图1):
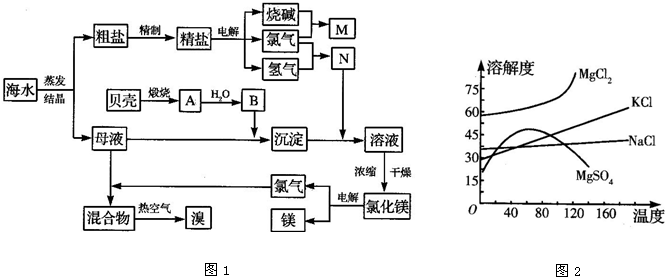
请回答下列问题:
(1)向Mg(OH)2中加入盐酸后,要获得MgCl2?6H2O晶体,需要进行的实验操作依次为
A.蒸馏 B.灼烧 C.过滤
D.蒸发 E.冷却结晶
(2)目前工业上主要采用隔膜法电解饱和食盐水,下列关于隔膜电解槽的叙述错误的是
A.隔膜的作用,防止氯气和氢氧化钠、氯气和氢气接触而发生反应
B.电解之前应除去Ca、Mg,以防止电解时生成Ca(OH)2、Mg(OH)2,从而堵塞隔膜
C.阴极产物为氢氧化钠和氢气
D.电解槽的阳极用金属铁网制成
(3)母液中常含有MgCl2、NaCl、MgSO4、KCl等(其溶解度曲线如图2所示),可进一步加工制得一些重要的产品.若将母液加热升温到60℃以上,随着水分的蒸发,会逐渐析出晶体,此晶体的主要成分是
查看习题详情和答案>>

请回答下列问题:
(1)向Mg(OH)2中加入盐酸后,要获得MgCl2?6H2O晶体,需要进行的实验操作依次为
DEC
DEC
(填序号).A.蒸馏 B.灼烧 C.过滤
D.蒸发 E.冷却结晶
(2)目前工业上主要采用隔膜法电解饱和食盐水,下列关于隔膜电解槽的叙述错误的是
D
D
(填序号).A.隔膜的作用,防止氯气和氢氧化钠、氯气和氢气接触而发生反应
B.电解之前应除去Ca、Mg,以防止电解时生成Ca(OH)2、Mg(OH)2,从而堵塞隔膜
C.阴极产物为氢氧化钠和氢气
D.电解槽的阳极用金属铁网制成
(3)母液中常含有MgCl2、NaCl、MgSO4、KCl等(其溶解度曲线如图2所示),可进一步加工制得一些重要的产品.若将母液加热升温到60℃以上,随着水分的蒸发,会逐渐析出晶体,此晶体的主要成分是
NaCl和MgSO4
NaCl和MgSO4
;过滤上述晶体后,将滤液降温到30℃以下,又逐渐析出晶体,用一定量的冷水洗涤该晶体,最后可得到比较纯净的KCl
KCl
晶体.