摘要:原子结构示意图: 圈内+16表示S的原子核内有16个带正电荷的质子 弧线表示电子层 弧线上的数字表示该电子层上的电子数 S 典型例题 [例]右图是某粒子的结构示意图.下列说法不正确的是( ) A.该元素原子的原子核外有2个电子层 B.该粒子是阳离子 C.该元素是一种金属元素 D.该粒子具有稳定的结构 [解析]由所给的粒子的结构示意图知.该原子核内有13个质子.核外有10个电子.为铝离子.结构稳定.其原子的原子核外有3个电子层. [答案] A [方法技巧] 原子结构示意图和离子结构示意图的比较:以Cl和Cl-,Na和Na+为例 Cl Cl- Na Na+ 基础过关 第2课时 表示物质结构的化学用语
网址:http://m.1010jiajiao.com/timu_id_3712553[举报]
(2010?辽宁二模)A、B、C、D、E五种单质均由短周期元素组成,在化学反应中均能形成简单的阳离子或阴离子,且B、D、E离子具有相同的电子层结构,离子半径CBDEA.常温时,A、B为气态,A和B两元素可形成2:1或1:1的共价化合物M或N.它们之间的部分转化关系如下:其中F、P和E的最高价氧化物的水化物都具有相同的摩尔质量.

请回答下列问题:
(1)E的原子结构示意图为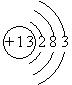
 ,F的电子式是
,F的电子式是
 ;
;
(2)以铂作电极,Q为电解质溶液,通入A、B单质形成原电池,通入气体A的电极是
(3)N与P的化学性质具有一定的相似性,其最典型的共性是
(4)写出E与Q溶液反应的离子方程式,并指出电子转移的方向和数目
 .
.
(5)已知:4D(s)+B(g)=2G(s)△H=-akJ?mol--12D(s)+B(g)=P(s)△H=-bkJ?mol-1用化学式表示B与G反应生成P的热化学方程式
查看习题详情和答案>>

请回答下列问题:
(1)E的原子结构示意图为




(2)以铂作电极,Q为电解质溶液,通入A、B单质形成原电池,通入气体A的电极是
负
负
极,正极的电极反应式为2H2O+O2+4e-═4OH-
2H2O+O2+4e-═4OH-
.(3)N与P的化学性质具有一定的相似性,其最典型的共性是
强氧化性
强氧化性
.(4)写出E与Q溶液反应的离子方程式,并指出电子转移的方向和数目


(5)已知:4D(s)+B(g)=2G(s)△H=-akJ?mol--12D(s)+B(g)=P(s)△H=-bkJ?mol-1用化学式表示B与G反应生成P的热化学方程式
2Na2O(s)+O2(g)2=Na2O2(s)△H=(a-2b)kJ/mol
2Na2O(s)+O2(g)2=Na2O2(s)△H=(a-2b)kJ/mol
. W、X、Y、Z四种短周期元素在元素周期表中的位置如图所示,其中Z位于ⅦA族.请回答下列问题.
W、X、Y、Z四种短周期元素在元素周期表中的位置如图所示,其中Z位于ⅦA族.请回答下列问题.(1)W的原子结构示意图为


酸性强弱为HClO4>H3PO4
酸性强弱为HClO4>H3PO4
(举一例).(2)W、Y和氢3种元素所形成的一种化合物,其75%(体积分数)的溶液常用于医疗消毒,该化合物的结构简式为
CH3CH2OH
CH3CH2OH
.(3)电解NaZ水溶液时,阴极的电极反应式为
2H++2e-=H2↑
2H++2e-=H2↑
.工业上,以上述反应的阳极产物和Ca(OH)2为原料,制备漂白粉反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
.(4)已知:298K时,金属钠与Y2气体反应,生成1mol Na2Y固体时,放出热量414kJ;生成1mol Na2Y2固体时,放出热量511kJ.由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为
Na2O(s)+
O2(g)=Na2O2(s);△H=-97kJ/mol
| 1 |
| 2 |
Na2O(s)+
O2(g)=Na2O2(s);△H=-97kJ/mol
.| 1 |
| 2 |
A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和A与X均可形成10个电子化合物;B与Z的最外层电子数之比为2:3,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红.请回答下列问题.
(1)Z的原子结构示意图为
 ; Z在周期表中的位置是
; Z在周期表中的位置是
(2)化合物Y2X2的电子式为
 ;它含有的化学键类型有
;它含有的化学键类型有
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应生成Z的化学方程式为
(4)A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正极通入
(5)1980年我国首次制成一辆燃氢汽车,乘员12人,以50km/h行驶了40km.为了有效发展民用氢能源,首先必须制得廉价的氢气.下列可供开发又较低经济的制氢方法是
①电解水 ②锌和稀硫酸反应 ③光解海水
其次,制得纯氢气后,还需要解决的问题是
查看习题详情和答案>>
(1)Z的原子结构示意图为


第三周期ⅥA族
第三周期ⅥA族
;B元素的名称为碳
碳
.(2)化合物Y2X2的电子式为


A、C
A、C
(填序号).A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应生成Z的化学方程式为
H2O2+H2S=S↓+2H2O
H2O2+H2S=S↓+2H2O
.(4)A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正极通入
氧气
氧气
(填物质名称);负极电极反应式为H2-2e-+2OH-═2H2O
H2-2e-+2OH-═2H2O
.(5)1980年我国首次制成一辆燃氢汽车,乘员12人,以50km/h行驶了40km.为了有效发展民用氢能源,首先必须制得廉价的氢气.下列可供开发又较低经济的制氢方法是
③
③
(填写编号)①电解水 ②锌和稀硫酸反应 ③光解海水
其次,制得纯氢气后,还需要解决的问题是
氢气的液化、氢气的安全储存等
氢气的液化、氢气的安全储存等
.(写出其中的一个)现有部分元素的原子结构特点如表:
(1)画出W原子结构示意图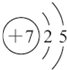
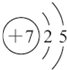 .
.
(2)元素X与元素Z相比,非金属性较强的是
(3)X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为
(4)元素X和元素Y以原子个数比1:1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等.以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,写出该反应的化学方程式
查看习题详情和答案>>
| X | L层电子数是K层电子数的3倍 |
| Y | 核外电子层数等于原子序数 |
| Z | L层电子数是K层和M层电子数之和 |
| W | 最外层电子数是次外层电子数的2.5倍 |
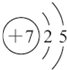
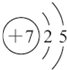
(2)元素X与元素Z相比,非金属性较强的是
X(或氧)
X(或氧)
,写出一个能表示X、Z非金属性强弱关系的化学反应方程式S+O2
SO2或2H2S+O2═2H2O+2S
| ||
S+O2
SO2或2H2S+O2═2H2O+2S
.
| ||
(3)X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为
NH4HSO4
NH4HSO4
.(4)元素X和元素Y以原子个数比1:1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等.以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,写出该反应的化学方程式
N2H4+2H2O2
N2+4H2O
| ||
N2H4+2H2O2
N2+4H2O
.
| ||
针对下面10种元素,完成以下各小题。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 |
|
|
| C | N | O |
| Ne |
| 3 | Na | Mg | Al | Si |
| S | Cl | m] |
(1)地壳中含量最多的元素是 (填名称)。
(2)化学性质最不活泼的元素是 (填元素符号)。
(3)Al的原子结构示意图为 。
(4)C与N相比,原子半径较小的是 。
(5)最高价氧化物对应的水化物碱性最强的是 (填化学式)。
(6)MgO和Al2O3中,属于两性氧化物的是 。
(7)S和Cl相比,元素非金属性较强的是 。
(8)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式 。
查看习题详情和答案>>