题目内容
现有部分元素的原子结构特点如表:
(1)画出W原子结构示意图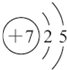
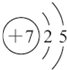 .
.
(2)元素X与元素Z相比,非金属性较强的是
(3)X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为
(4)元素X和元素Y以原子个数比1:1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等.以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,写出该反应的化学方程式
| X | L层电子数是K层电子数的3倍 |
| Y | 核外电子层数等于原子序数 |
| Z | L层电子数是K层和M层电子数之和 |
| W | 最外层电子数是次外层电子数的2.5倍 |
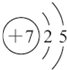
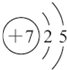
(2)元素X与元素Z相比,非金属性较强的是
X(或氧)
X(或氧)
,写出一个能表示X、Z非金属性强弱关系的化学反应方程式S+O2
SO2或2H2S+O2═2H2O+2S
| ||
S+O2
SO2或2H2S+O2═2H2O+2S
.
| ||
(3)X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为
NH4HSO4
NH4HSO4
.(4)元素X和元素Y以原子个数比1:1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等.以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,写出该反应的化学方程式
N2H4+2H2O2
N2+4H2O
| ||
N2H4+2H2O2
N2+4H2O
.
| ||
分析:X元素原子的L层电子数是K层电子数的3倍,根据核外电子排布规律,可知L层为6个电子,所以X为氧元素,Y元素原子的核外电子层数等于原子序数,Y只能是H元素,Z 元素原子的L层电子数是K层和M层电子数之和,其M层电子数为6,所以Z是S元素,W元素原子的最外层电子数是次外层电子数的2.5倍,其次外层只能是K层,所以W为N元素,结合对应单质、化合物的性质以及题目要求解答该题.
解答:解:X元素原子的L层电子数是K层电子数的3倍,根据核外电子排布规律,可知L层为6个电子,所以X为氧元素,Y元素原子的核外电子层数等于原子序数,Y只能是H元素,Z 元素原子的L层电子数是K层和M层电子数之和,其M层电子数为6,所以Z是S元素,W元素原子的最外层电子数是次外层电子数的2.5倍,其次外层只能是K层,所以W为N元素,
(1)W为N元素,原子核外有2个电子层,最外层电子数为5,原子结构示意图为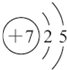 ,
,
故答案为: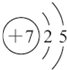 ;
;
(2)X为O,Z为S,位于同一主族,非金属性O>S,可根据反应S+O2
SO2或2H2S+O2═2H2O+2S证明,
故答案为:X(或氧);S+O2
SO2或2H2S+O2═2H2O+2S;
(3)X、Y、Z、W四种元素形成的一种离子化合物,可为(NH4)2SO4或NH4HSO4,其水溶液显强酸性,应为NH4HSO4,故答案为:NH4HSO4;
(4)元素X和元素Y以原子个数比1:1化合形成的化合物Q,为H2O2,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等,应为N2H4,以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,应生成氮气和水,反应的化学方程式为N2H4+2H2O2
N2+4H2O,
故答案为:N2H4+2H2O2
N2+4H2O.
(1)W为N元素,原子核外有2个电子层,最外层电子数为5,原子结构示意图为
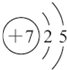 ,
,故答案为:
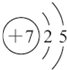 ;
;(2)X为O,Z为S,位于同一主族,非金属性O>S,可根据反应S+O2
| ||
故答案为:X(或氧);S+O2
| ||
(3)X、Y、Z、W四种元素形成的一种离子化合物,可为(NH4)2SO4或NH4HSO4,其水溶液显强酸性,应为NH4HSO4,故答案为:NH4HSO4;
(4)元素X和元素Y以原子个数比1:1化合形成的化合物Q,为H2O2,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等,应为N2H4,以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,应生成氮气和水,反应的化学方程式为N2H4+2H2O2
| ||
故答案为:N2H4+2H2O2
| ||
点评:本题考查原子结构和元素周期律的相互关系,题目难度中等,注意正确推断元素的种类为解答该题的关键,注意把握元素周期律的递变规律.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
