摘要:5.根据元素在周期表中的位置和性质递变规律分析: (1)氢氟酸为弱酸.水为中性.推断氨水的酸碱性强弱 . (2)从PH3能自燃.H2S可燃.推断Si H4燃烧的难易 . (3)As的最高氧化物的化学式是 .氢化物的化学式是 .砷在它的最高价氧化物的含量是65.2%.砷的原子量是 计算式: . (此题考查同周期.同主族元素性质变化规律的运用.)
网址:http://m.1010jiajiao.com/timu_id_3706928[举报]
 元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分.(1)元素Si在元素周期表中的位置为:第
三
三
周期第IVA
IVA
族.(2)热稳定性:H2O
>
>
H2S(填“>”、“<”或“=”).(3)可在图中分界线(虚线部分)附近寻找
B
B
.(填序号)A.优良的催化剂 B.半导体材料 C.合金材料 D.农药
(4)根据元素周期律,预测:
①阴影部分元素中最高价氧化物对应水化物的酸性最强的是
Cl
Cl
元素.(填元素符号)②H3AsO4、H2SeO4 的酸性强弱:H3AsO4
<
<
H2SeO4(填“>”、“<”或“=”). 元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分.(1)阴影部分元素N在元素周期表中的位置为
第二周期第VA族
第二周期第VA族
.根据元素周期律,请你预测:H3AsO4、H3PO4的酸性强弱:H3AsO4
<
<
H3PO4.(用“>”、“<”或“=”表示)(2)元素S的最高正价和最低负价分别为
+6
+6
、-2
-2
,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断在相同条件下,等物质的量的S和Se分别与等量的H2反应,生成气态氢化物的物质的量(b)
(b)
.(a) H2S<H2Se (b) H2S>H2Se (c) H2S=H2Se
(3)羰基硫(COS)分子结构与二氧化碳分子结构相似,所有原子的最外层都满足8电子结构.用电子式表示羰基硫分子的形成过程:


(4)试在表上画出金属和非金属的分界线


 元素在周期表中的位置,反映了元素的原子结构和元素的性质.右图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.右图是元素周期表的一部分.(1)阴影部分元素N在元素周期表中的位置为第
二
二
周期第ⅤA
ⅤA
族.根据元素周期律,预测:酸性强弱 H3AsO4
<
<
H3PO4.(用“>”或“<”表示)(2)元素S的最高正价和最低负价的代数和为
4
4
,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的限度比S与H2反应限度更小
更小
.(选填“更大”、“更小”或“相同”)(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是
H+,Br-,SO42-
H+,Br-,SO42-
.(4)下列说法正确的是
ABD
ABD
A.C、N、O、F的原子半径随着原子序数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.
(1)Si在元素周期表中的位置为
性强弱为
(2)上表元素中,原子半径最小的是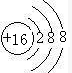
 .
.
(3)能证明Br2比I2的氧化性强的事实是
查看习题详情和答案>>
(1)Si在元素周期表中的位置为
第三周期ⅣA
第三周期ⅣA
,根据元素周期律,请你预测:H3AsO4、H3PO4的酸性强弱为
H3PO4>H3AsO4
H3PO4>H3AsO4
.(2)上表元素中,原子半径最小的是
F
F
,画出硫离子结构示意图

(3)能证明Br2比I2的氧化性强的事实是
Br2+2NaI=2NaBr+I2
Br2+2NaI=2NaBr+I2
(用化学方程式表示).| C | N | O | F | ||
| Si | P | S | Cl | ||
| Ge | As | Se | Br | ||
| Sn | Sb | Te | I | ||
 元素在周期表中的位置,反映了元素的原子结构和元素的性质.右图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.右图是元素周期表的一部分.(1)阴影部分元素N的最高价氧化物为
N2O5
N2O5
.根据元素周期律,请你预测:H3AsO4、H3PO4的酸性强弱:H3AsO4<
<
H3PO4.(用“>”、“<”或“=”表示)(2)元素S的最高正价和最低负价分别为
+6
+6
、-2
-2
,(3)在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断在相同条件下Se与H2反应的限度
更小
更小
(选填“更大”、“更小”或“相同”).(4)羰基硫(COS)分子结构与二氧化碳分子结构相似,所有原子的最外层都满足8电子结构.请写出羰基硫分子的电子式


(5)单质砷和热的浓H2SO4反应,生成As2O3,反应的化学方程式为
2As+3H2SO4(浓)
As2O3+3SO2↑+3H2O
| ||
2As+3H2SO4(浓)
As2O3+3SO2↑+3H2O
.
| ||