摘要: Cu+ +NO2-+2H+=Cu2++NO+H2O (3)3NO=N2O+NO2 (4)2NO2 N2O4
网址:http://m.1010jiajiao.com/timu_id_3706120[举报]
某化学小组在实验室模拟用软锰矿(主要成分MnO2,杂质为铁及铜的化合物等)制备高纯碳酸锰,过程如下(部分操作和条件略):
①缓慢向烧瓶中(见图a)通入过量混合气进行“浸锰”操作,主要反应原理为:
SO2+H2O=H2SO3
MnO2+H2SO3=MnSO4+H2O
(铁浸出后,过量的SO2会将Fe3+还原为Fe2+)
②向“浸锰”结束后的烧瓶中加入一定量纯MnO2粉末.
③再用Na2CO3溶液调节pH为3.5左右,过滤.
④调节滤液pH为6.5~7.2,加入NH4HCO3,有浅红色的沉淀生成,过滤、洗涤、干燥,得到高纯碳酸锰.

回答:
(1)“浸锰”反应中往往有副产物MnS2O6的生成,温度对“浸锰”反应的影响如图b,为减少MnS2O6 的生成,“浸锰”的适宜温度是 .
(2)查阅表1,③中调pH为3.5时沉淀的主要成分是 .②中加入一定量纯MnO2粉末的主要作用是 ,相应反应的离子方程式为 .
表1:生成相应氢氧化物的pH
(3)③中所得的滤液中含有Cu2+,可添加过量的难溶电解质MnS除去Cu2+,经过滤,得到纯净的MnSO4.用平衡移动原理解释加入MnS的作用 .
(4)④中加入NH4HCO3后发生反应的离子方程式是 .
(5)检验④中沉淀是否洗涤干净的方法是 .
查看习题详情和答案>>
①缓慢向烧瓶中(见图a)通入过量混合气进行“浸锰”操作,主要反应原理为:
SO2+H2O=H2SO3
MnO2+H2SO3=MnSO4+H2O
(铁浸出后,过量的SO2会将Fe3+还原为Fe2+)
②向“浸锰”结束后的烧瓶中加入一定量纯MnO2粉末.
③再用Na2CO3溶液调节pH为3.5左右,过滤.
④调节滤液pH为6.5~7.2,加入NH4HCO3,有浅红色的沉淀生成,过滤、洗涤、干燥,得到高纯碳酸锰.

回答:
(1)“浸锰”反应中往往有副产物MnS2O6的生成,温度对“浸锰”反应的影响如图b,为减少MnS2O6 的生成,“浸锰”的适宜温度是
(2)查阅表1,③中调pH为3.5时沉淀的主要成分是
表1:生成相应氢氧化物的pH
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 | 4.7 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 | 6.7 |
(4)④中加入NH4HCO3后发生反应的离子方程式是
(5)检验④中沉淀是否洗涤干净的方法是
三星堆遗址考古的重大发现,揭开了川西平原早期蜀国的面纱,将蜀国的历史推前了两千多年,填补了中国考古学、青铜文化、青铜艺术史上的诸多空白.而硫酸铜是湿法冶金应用极早的一种化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图1、2所示)
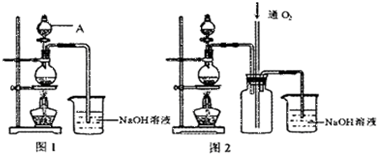
(1)图1烧瓶中发生反应的离子方程式为
(2)图2是图1的改进装置,其优点有
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
方案1:以空气为氧化剂.将铜粉在①坩埚中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应.
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应.向反应液中加FeSO4或Fe2(SO4)3,即发生反应.反应完全后向其中加物质甲调节pH到3~4,产生Fe(OH)3沉淀,过滤、蒸发、结晶,滤渣作催化剂循环使用.[已知Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为:3.7、6.4.]请回答下列问题:
①方案2中甲物质是
第二组:过氧化氢为氧化剂法
将3.2g铜丝放到45mL 1.5mol?L-1的稀硫酸中,控温在50℃.加入18mL 10%的H2O2,反应0.5h后,升温到60℃,持续反应1h后,过滤、蒸发结晶、减压抽滤等,用少量95%的酒精淋洗后晾干,得到CuSO4?5H2O的质量为10.6g.
请回答下列问题:
②加热时温度不宜过高的原因是
查看习题详情和答案>>

(1)图1烧瓶中发生反应的离子方程式为
Cu+4H++2NO3-═Cu2++2NO2↑+2H2O或3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
Cu+4H++2NO3-═Cu2++2NO2↑+2H2O或3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
;(2)图2是图1的改进装置,其优点有
防止倒吸;NO、NO2有毒气体能被完全吸收
防止倒吸;NO、NO2有毒气体能被完全吸收
;(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
方案1:以空气为氧化剂.将铜粉在①坩埚中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应.
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应.向反应液中加FeSO4或Fe2(SO4)3,即发生反应.反应完全后向其中加物质甲调节pH到3~4,产生Fe(OH)3沉淀,过滤、蒸发、结晶,滤渣作催化剂循环使用.[已知Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为:3.7、6.4.]请回答下列问题:
①方案2中甲物质是
b
b
(填字母序号). a.CaO b.CuCO3 c.CaCO3第二组:过氧化氢为氧化剂法
将3.2g铜丝放到45mL 1.5mol?L-1的稀硫酸中,控温在50℃.加入18mL 10%的H2O2,反应0.5h后,升温到60℃,持续反应1h后,过滤、蒸发结晶、减压抽滤等,用少量95%的酒精淋洗后晾干,得到CuSO4?5H2O的质量为10.6g.
请回答下列问题:
②加热时温度不宜过高的原因是
防止双氧水分解
防止双氧水分解
,根据有关数据计算出制取CuSO4?5H2O的产率(实际产量与理论产量的百分比)=84.8%
84.8%
.盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂.请回答下列问题:
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有
(2)硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜.下列制备方法符合“绿色化学”思想的是
①Cu+HNO3(浓)→Cu(NO3)2
②Cu+HNO3(稀)→Cu(NO3)2
③Cu△
CuO
Cu(NO3)2
(3)①在100mL 18mol?L-1的浓硫酸中加入过量的铜片,加热使之充分反应,测得产生的气体在标准状况下的体积可能是
A.40.32L B.30.24L C.20.16L D.13.44L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
(4)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水.该反应的化学方程式为
查看习题详情和答案>>
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有
强氧化
强氧化
性.用玻璃棒蘸取浓硫酸滴在纸上,纸逐渐变黑,说明浓硫酸具有脱水性
脱水性
性.(2)硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜.下列制备方法符合“绿色化学”思想的是
③
③
(填序号).①Cu+HNO3(浓)→Cu(NO3)2
②Cu+HNO3(稀)→Cu(NO3)2
③Cu△
| 空气 |
| △ |
| HNO3(稀) |
(3)①在100mL 18mol?L-1的浓硫酸中加入过量的铜片,加热使之充分反应,测得产生的气体在标准状况下的体积可能是
D
D
.A.40.32L B.30.24L C.20.16L D.13.44L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.(4)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水.该反应的化学方程式为
Cu+2HCl+H2O2=CuCl2+2H2O
Cu+2HCl+H2O2=CuCl2+2H2O
.有机物A( )是合成高分子化合物HPMA的中间体,HPMA可用于锅炉阻垢剂.
)是合成高分子化合物HPMA的中间体,HPMA可用于锅炉阻垢剂.
(1)有机物A能够发生的反应有: (填写字母).
a.取代反应b.加成反应 c.消去反应d.酯化反应
(2)有机物A在Cu做催化剂和加热条件下,与氧气反应生成有机物B.B中含有的官能团除-Cl以外,还含有的官能团是 .
(3)有机物B经氧化后生成有机物C,C可有如下图所示的转化关系:写出E的结构简式: .
(4)D在高温、高压和催化剂作用下反应生成HPMA,写出反应的化学方程式: .
(5)F是E的一种同分异构体.0.1mol F与足量金属Na反应放出3.36L H2(标准状况下);0.1mol F与足量NaHCO3反应放出2.24L CO2(标准状况下);F能发生银镜反应.F的结构简式可能是: 、 .
查看习题详情和答案>>
 )是合成高分子化合物HPMA的中间体,HPMA可用于锅炉阻垢剂.
)是合成高分子化合物HPMA的中间体,HPMA可用于锅炉阻垢剂.(1)有机物A能够发生的反应有:
a.取代反应b.加成反应 c.消去反应d.酯化反应
(2)有机物A在Cu做催化剂和加热条件下,与氧气反应生成有机物B.B中含有的官能团除-Cl以外,还含有的官能团是
(3)有机物B经氧化后生成有机物C,C可有如下图所示的转化关系:写出E的结构简式:
(4)D在高温、高压和催化剂作用下反应生成HPMA,写出反应的化学方程式:
(5)F是E的一种同分异构体.0.1mol F与足量金属Na反应放出3.36L H2(标准状况下);0.1mol F与足量NaHCO3反应放出2.24L CO2(标准状况下);F能发生银镜反应.F的结构简式可能是:
