网址:http://m.1010jiajiao.com/timu_id_3705094[举报]
(18分)某同学设计了如下装置用于制取SO2和验证SO2的性质。分流漏斗内装75%的浓硫酸,锥形瓶内装固体Na2SO3。试回答以下问题:

⑴锥形瓶内发生的反应的化学方程式为: 。
⑵实验过程中,品红试液的颜色变为: ;石蕊试液的颜色变化为: 。实验后加热烧瓶,品红试液的颜色变化为: 。
⑶溴水与SO2反应的离子方程式为: 。
⑷导管①的作用是: ;倒置漏斗的作用是 。
⑸方框内装置能否换成启普发生器? (回答“能”或“不能”)。
查看习题详情和答案>>(18分)某同学设计了如下装置用于制取SO2和验证SO2的性质。分流漏斗内装75%的浓硫酸,锥形瓶内装固体Na2SO3。试回答以下问题:

⑴锥形瓶内发生的反应的化学方程式为: 。
⑵实验过程中,品红试液的颜色变为: ;石蕊试液的颜色变化为: 。实验后加热烧瓶,品红试液的颜色变化为: 。
⑶溴水与SO2反应的离子方程式为: 。
⑷导管①的作用是: ;倒置漏斗的作用是 。
⑸方框内装置能否换成启普发生器? (回答“能”或“不能”)。
查看习题详情和答案>>
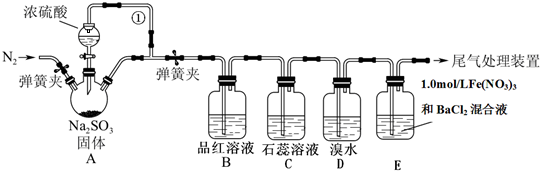
(1)装置A中用于添加浓硫酸的仪器名称为
(2)B、C、D三个装置分别先后验证了SO2的哪些性质
A.吸附性、酸性、还原性 B.还原性、酸性、还原性
C.漂白性、酸性、还原性 D.漂白性、酸性、氧化性.
(3)SO2和品红反应的原理是
(4)实验前鼓入N2的目的是
(5)装置E中产生了白色沉淀,其成分是
可能①:
可能②:
(6)若用2.0mol/L的NaOH溶液吸收SO2尾气,请画出该尾气吸收装置. 查看习题详情和答案>>
某同学为了探究SO2与Na2O2的反应是否类似于CO2,设计反应装置见图.

(1)选择制取SO2的合适试剂______;
a.10%的H2SO4溶液 b.80%的H2SO4溶液 c.Na2SO3固体 d.CaSO3固体
(2)装置C中NaOH溶液的作用是______;
(3)上述反应装置有些不足之处,为完善该装置,请从供选择的装置中选择需要的装置______(填编号),说明所选装置在整套装置中的位置______;
(4)移开棉花,将带火星的木条放在C试管口,木条不复燃,该同学认为SO2与Na2O2的反应不同于CO2,请据此写出反应的化学方程式______;
(5)为检验是否有Na2SO4生成,设计如下方案

上述方案______(填“合理”、“不合理”),理由:______;
(6)Na2O2反应完全后,为确定所得固体的组成,可进行如下操作:称取样品m g并溶于适量的水中,______(选择下列操作的编号按操作顺序填入),烘干,称量,干燥沉淀质量为n g,计算含量.
a.加足量盐酸酸化的氯化钡溶液;b.加足量硫酸酸化的氯化钡溶液;c.过滤;d.洗涤; e.蒸发结晶.
查看习题详情和答案>>

(1)选择制取SO2的合适试剂
a.10%的H2SO4溶液 b.80%的H2SO4溶液 c.Na2SO3固体 d.CaSO3固体
(2)装置C中NaOH溶液的作用是
(3)上述反应装置有些不足之处,为完善该装置,请从供选择的装置中选择需要的装置
(4)移开棉花,将带火星的木条放在C试管口,木条不复燃,该同学认为SO2与Na2O2的反应不同于CO2,请据此写出反应的化学方程式
(5)为检验是否有Na2SO4生成,设计如下方案

上述方案
(6)Na2O2反应完全后,为确定所得固体的组成,可进行如下操作:称取样品m g并溶于适量的水中,
a.加足量盐酸酸化的氯化钡溶液;b.加足量硫酸酸化的氯化钡溶液;c.过滤;d.洗涤; e.蒸发结晶.