网址:http://m.1010jiajiao.com/timu_id_3704056[举报]
(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:
Cd+2NiO(OH)+2H2O
| 放电 |
| 充电 |
已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是
①以上电池反应是在非水溶液中进行的 ②以上电池反应是在强碱溶液中进行的
③以上电池反应不需要电解质就能进行 ④电池工作时是化学能转变为电能
A.①③B.②④C.①④D.②③
(2)另一种常用的电池是锂电池由于它的容量特别大而广泛应用于心脏起搏器,一般使用时间可长达十年.电池总反应可表示为:Li+MnO2=LiMnO2,它的负极材料是
(3)铅蓄电池是典型的可充型电池,电池总反应式为:
Pb+PbO2+4H++2SO
2- 4 |
| 放电 |
| 充电 |
放电时电解液中H2SO4的浓度将变
(4)随着人们生活质量的不断提高,废弃的电池必须进行集中处理的问题被提到议事日程,其首要原因是
(1)某小组设计如图1所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质.

①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?______(填“相同”或“不相同”);若装置D中装的是V2O5(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为______.
②SO2通入B中,溶液颜色退去,则该反应的离子方程式为______.
(2)某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母)______,仍然无法观察到沉淀产生.
A.氨水 B.稀盐酸 C.硝酸钾溶液 D.硫化钠溶液
(3)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生.写出Cl2与含X的溶液反应的离子方程式______.
(4)某科研单位利用电化学原理用SO2来制备硫酸,装置如图2,含有某种催化剂,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触.通入SO2的电极为______极,其电极反应式为______;电池的总反应式______

Ⅱ实验是化学研究的基础,关于下列各装置图的叙述正确的是______(填序号)

A.装置①可完成多种气体的发生、净化和收集,如铜屑与稀硝酸反应
B.装置②中,a为正扳,d为阳极
C.装置③可用于收集H2、NH3、Cl2,、HCl、NO2等
D.装置④能用于测量气体体积
Ⅲ用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图4所示(a、b为石墨电极).下列说法中正确的是______(填序号)

A.铅蓄电池负极的反应式为:Pb-2e-=Pb2+
B.铅蓄电池放电时,B极质量减轻,A极质量增加
C.铅蓄电池充电时,A极应与外电源负极相连
D.电解苦卤水时,a电极首先放电的是Br-.
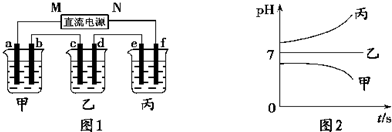
图1装置中,甲、乙、丙三个烧杯中依次盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为铂电极.接通电源,经过一段时间后,测得甲中b电极质量增加了43.2g.常温下各烧杯中溶液pH与电解时间t关系如图2.请回答下列问题:

(1)写出三种强电解质的化学式:A______;B______;C______.
(2)写出乙烧杯c电极发生的电极反应为______,甲烧杯中的总反应的化学方程式为______.
(3)计算丙烧杯e电极上生成的气体在标准状况下的体积为______,甲烧杯中溶液体积为400ml,pH=______.
(4)要使甲烧杯中的A溶液恢复到电解前的状态,需要加入的物质是______,其质量为______.
(5)若直流电源使用的是铅蓄电池,铅蓄电池的正极材料是PbO2,负极材料是Pb,电解质溶液时H2SO4,则放电时N级上发生的电极反应为______,M级附近溶液的pH______(选填“升高”或“降低”或“不变”).铅蓄电池充电时,若阳极和阴极之间用阳离子交换膜(只允许H+通过)隔开,则当外电路通过0.2mol电子时,由阳极室通过阳离子交换膜进入阴极室的阳离子有______mol.
图1装置中,甲、乙、丙三个烧杯中依次盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为铂电极.接通电源,经过一段时间后,测得甲中b电极质量增加了43.2g.常温下各烧杯中溶液pH与电解时间t关系如图2.请回答下列问题:
(1)写出三种强电解质的化学式:A
(2)写出乙烧杯c电极发生的电极反应为
| ||
| ||
(3)计算丙烧杯e电极上生成的气体在标准状况下的体积为
(4)要使甲烧杯中的A溶液恢复到电解前的状态,需要加入的物质是
(5)若直流电源使用的是铅蓄电池,铅蓄电池的正极材料是PbO2,负极材料是Pb,电解质溶液时H2SO4,则放电时N级上发生的电极反应为
A、B、C三种强电解质,它们溶于水在水中电离出的阳离子有K+、Ag+,阴离子有NO3-、OH-(电解质电离的离子有重复)。
图1装置中,甲、乙、丙三个烧杯中依次盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为铂电极。接通电源,经过一段时间后,测得甲中b电极质量增加了43.2g。常温下各烧杯中溶液pH与电解时间t关系如图2。请回答下列问题:
(1)写出三种强电解质的化学式:A ;B ;C 。
(2)写出乙烧杯c电极发生的电极反应为__________________________,甲烧杯中的总反应的化学方程式为___________________________________________。
(3)计算丙烧杯e电极上生成的气体在标准状况下的体积为________________,甲烧杯中溶液的pH= 。(假设溶液体积是400ml)
(4)要使甲烧杯中的A溶液恢复到电解前的状态,需要加入的物质是_____________,其质量为 。
(5)若直流电源使用的是铅蓄电池,铅蓄电池的正极材料是PbO2,负极材料是Pb,电解质溶液时H2SO4,则放电时N级上发生的电极反应为________________________________
____________________,M级附近溶液的pH (选填“升高”或“降低”或“不变”)。
铅蓄电池充电时,若阳极和阴极之间用阳离子交换膜(只允许H+通过)隔开,则当外电路通过0.2mol电子时,由阳极室通过阳离子交换膜进入阴极室的阳离子有 mol。